 产业资讯
产业资讯
 Insight数据库
Insight数据库  2022-04-11
2022-04-11
 5329
5329
3 月份
获批临床报告
◆ 3 月获批临床的新药共有 230 个受理号,涉及 145 个品种(附名单)
本报告数据来源:Insight 数据库、CDE 药物临床试验登记与信息公示
3月获批临床新药品种
Insight 数据库申报进度库显示,2022 年 3 月获批临床的新药共有 230 个受理号,涉及 145 个品种,下图为具体名单:
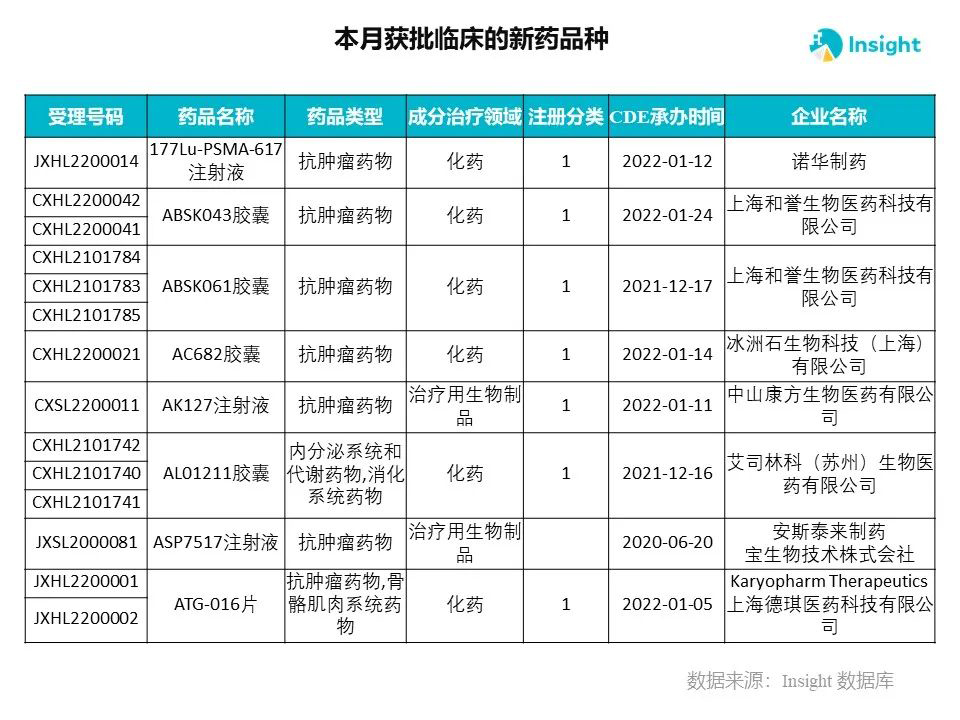
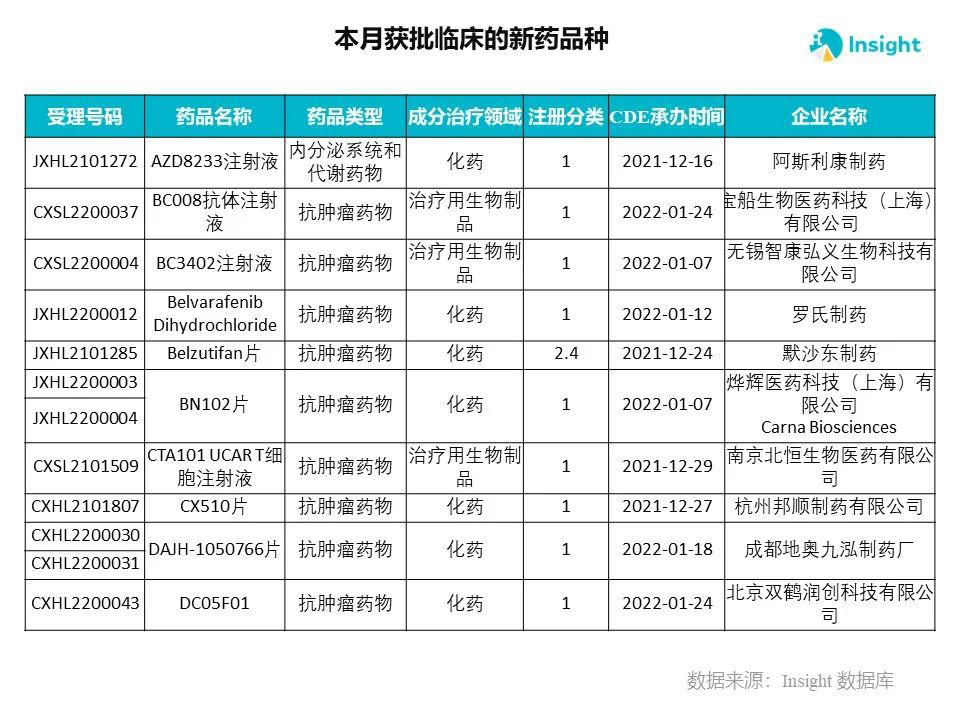
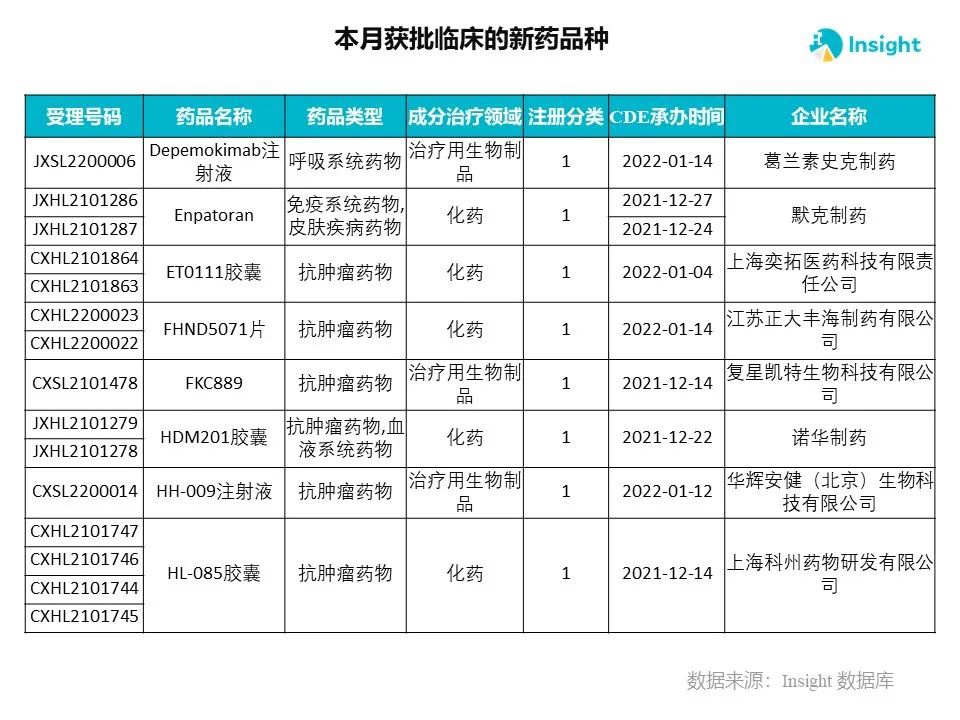
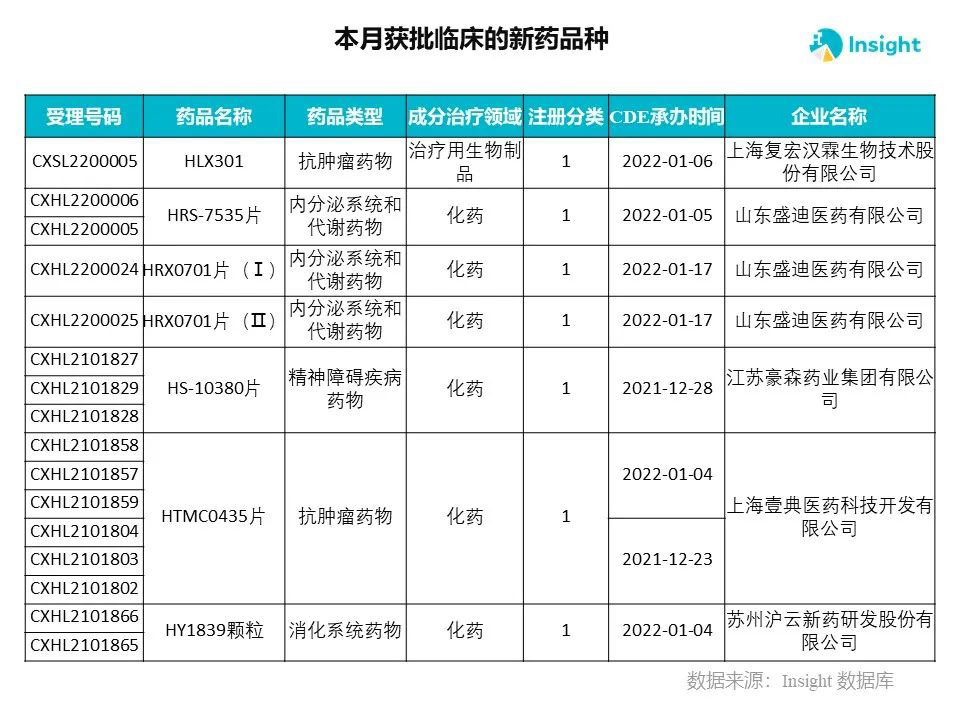

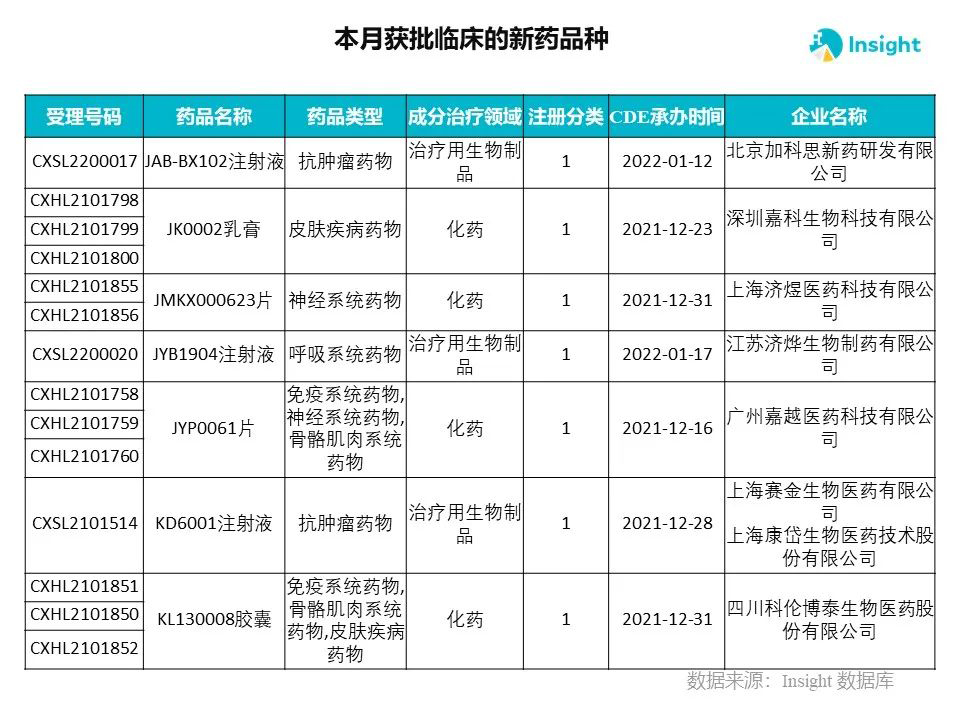
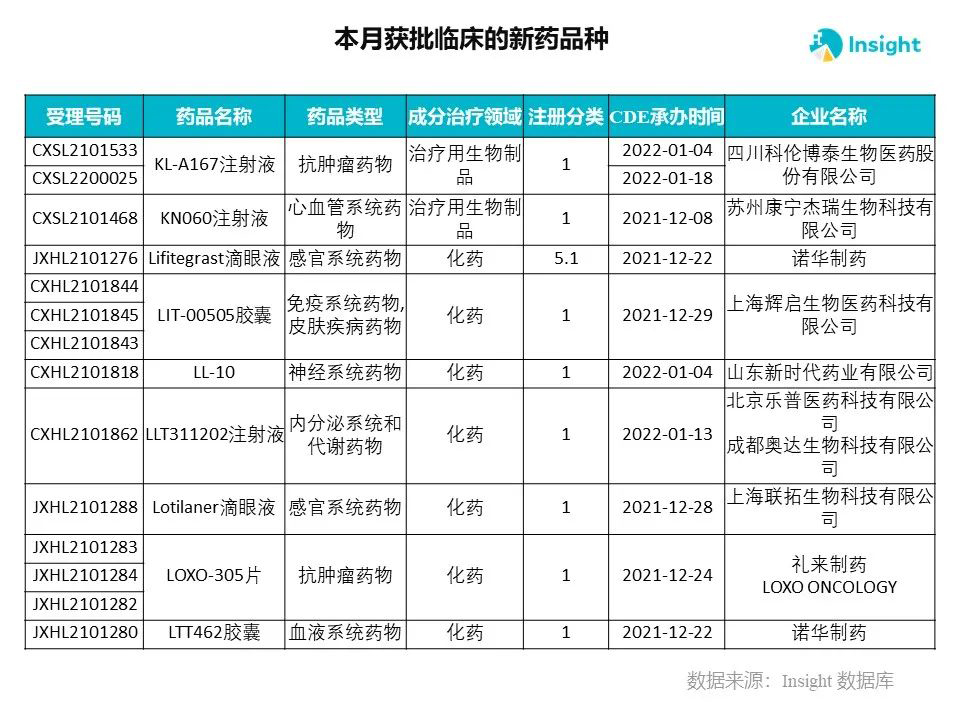
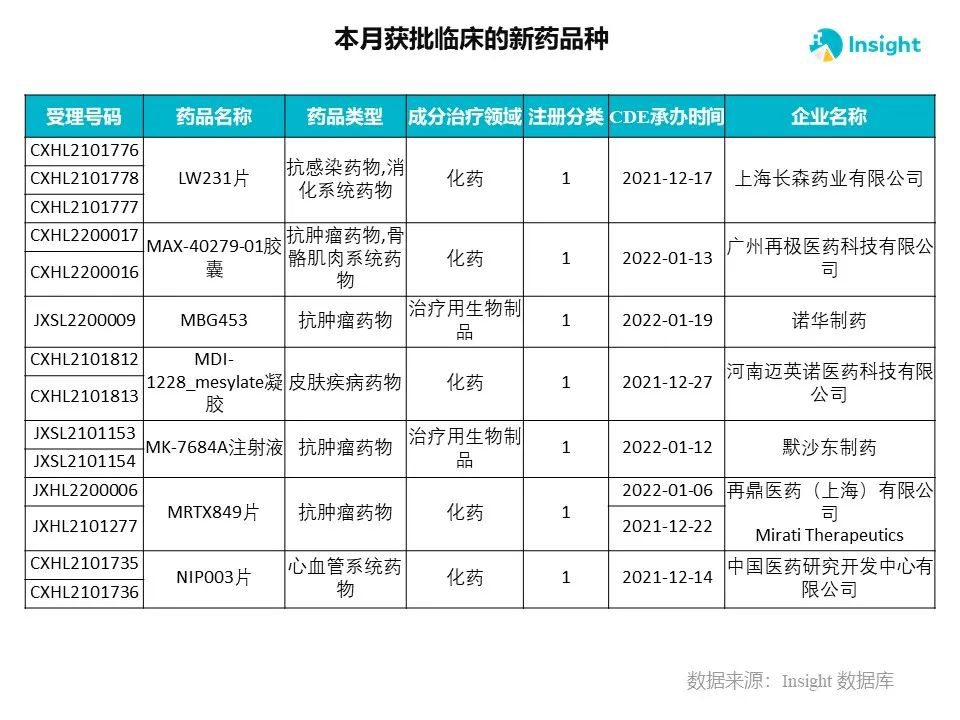
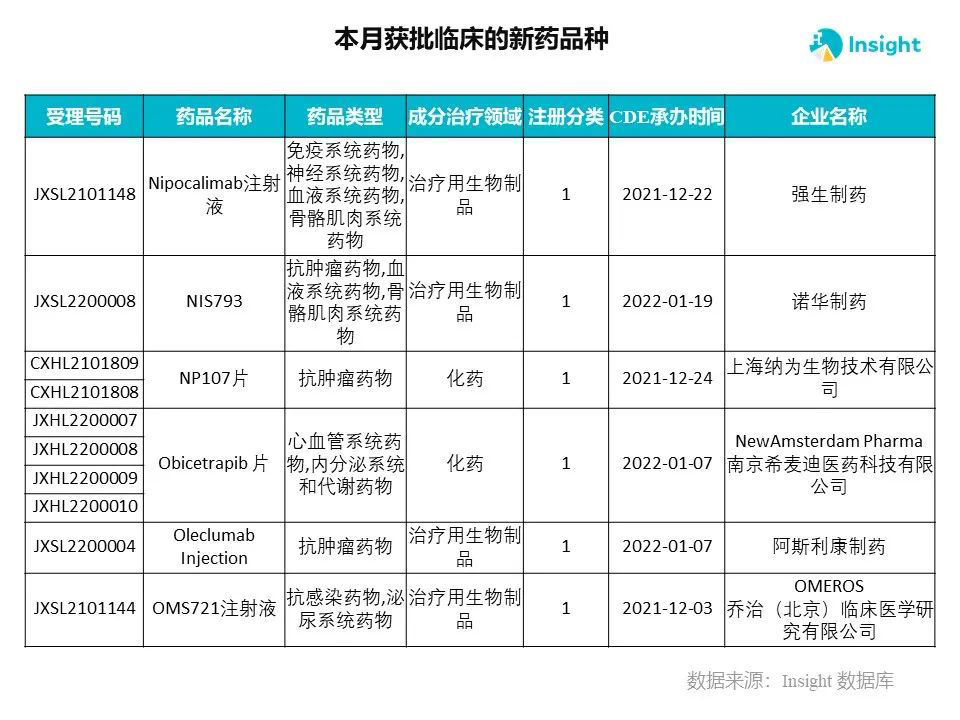
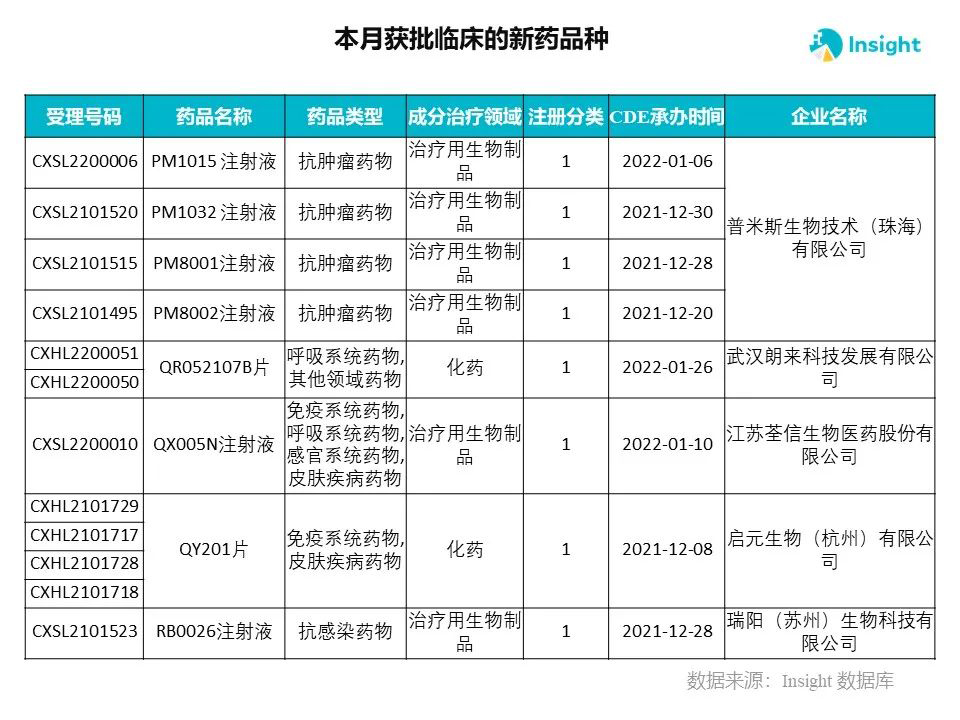
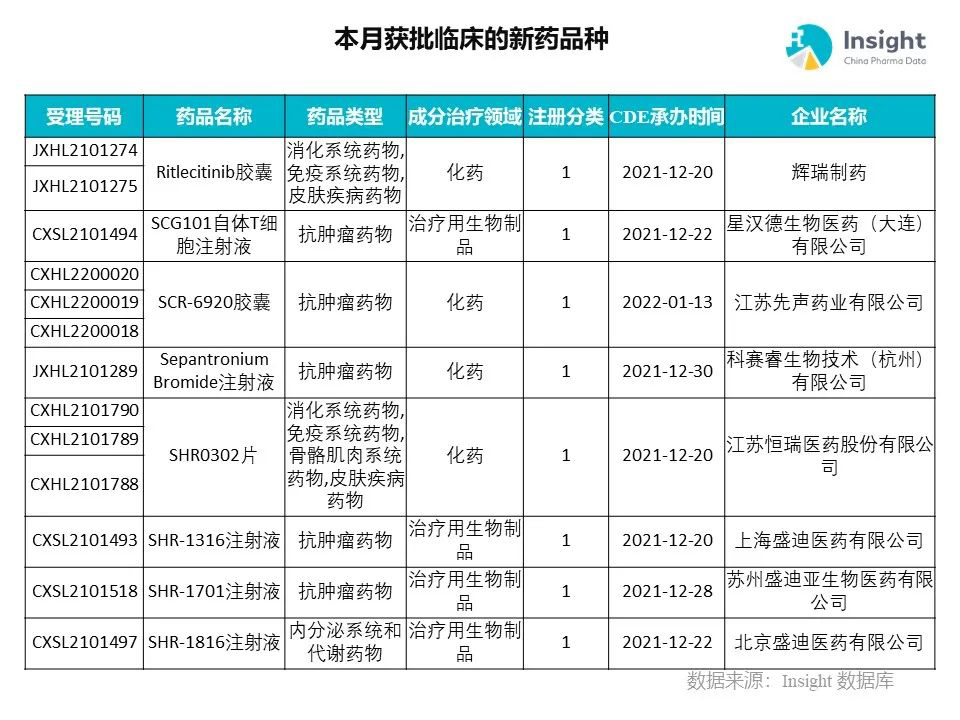
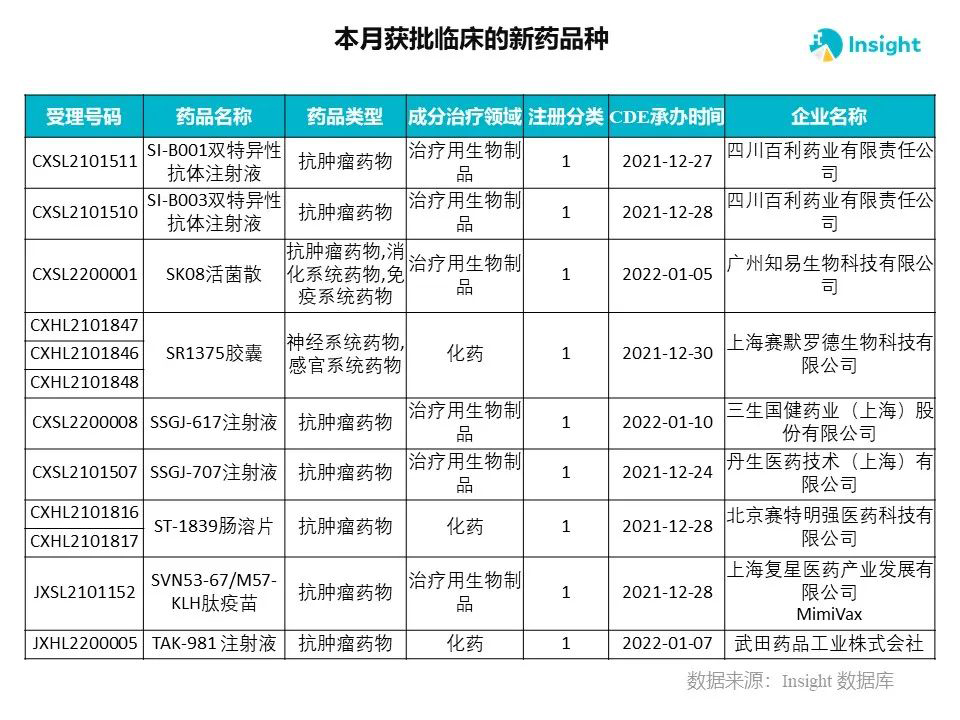
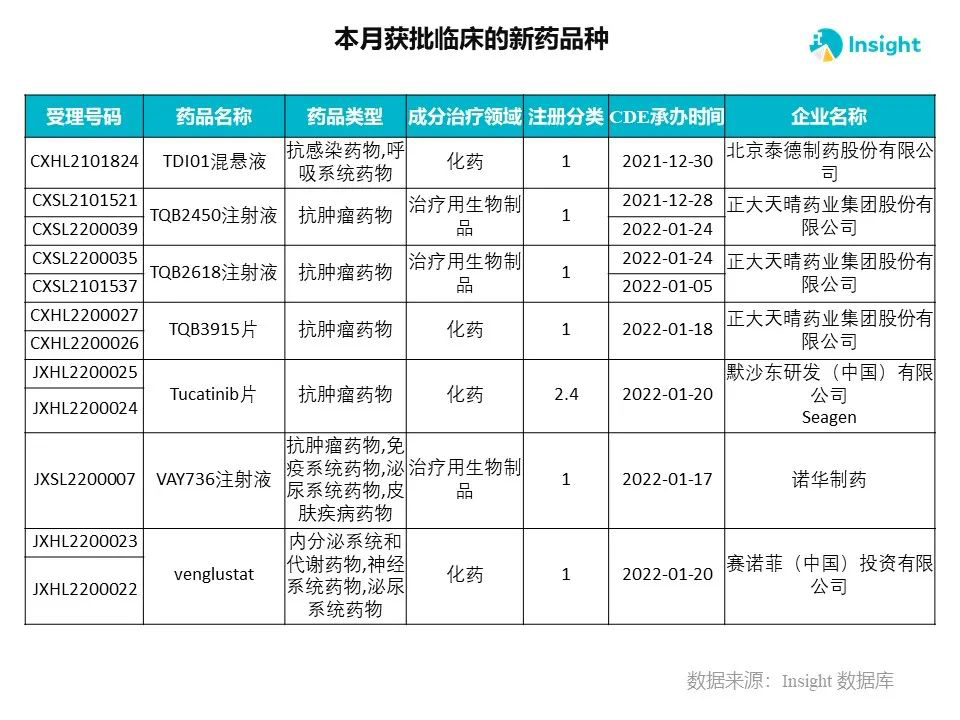
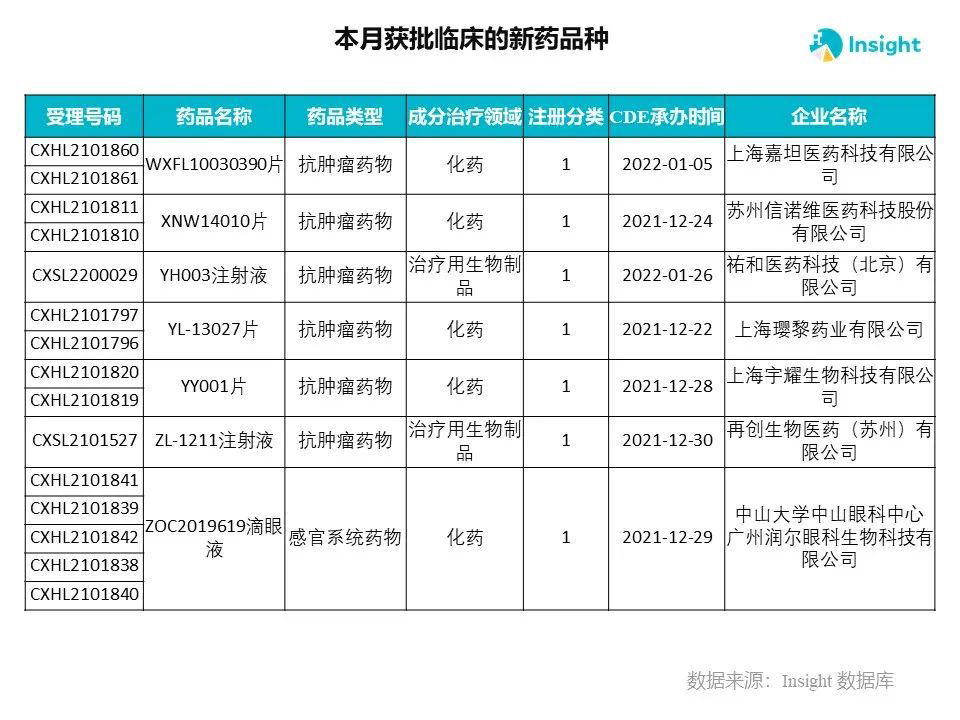
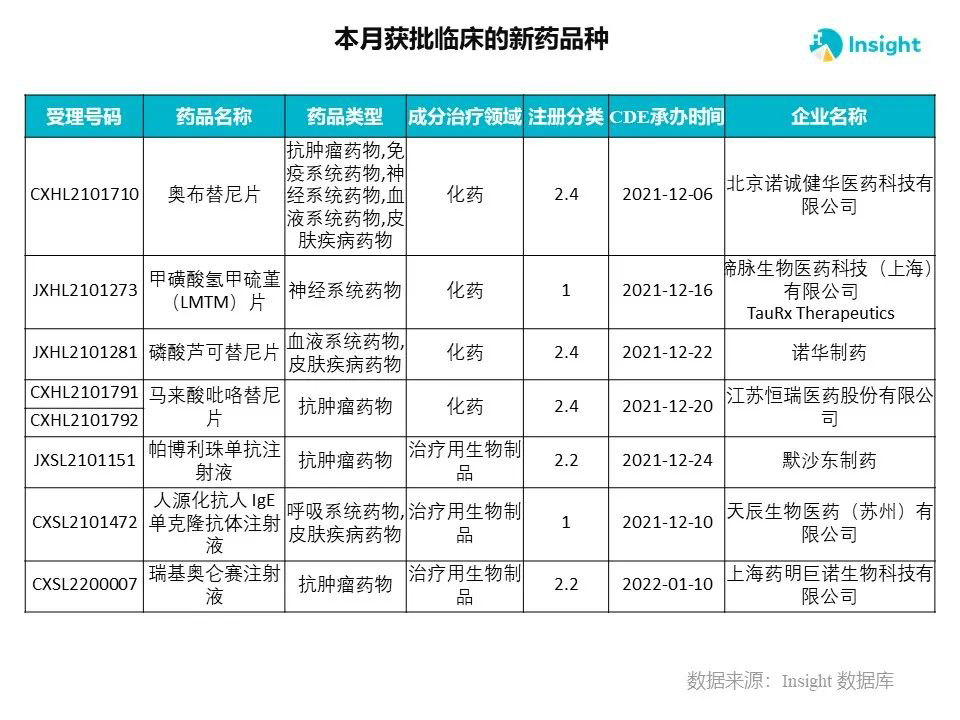
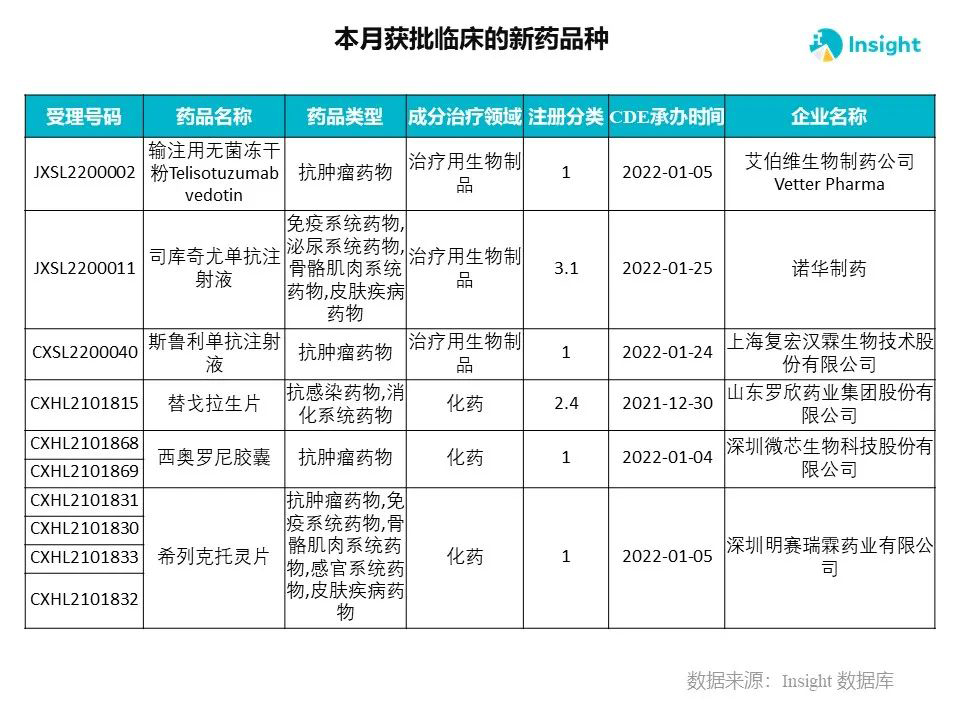
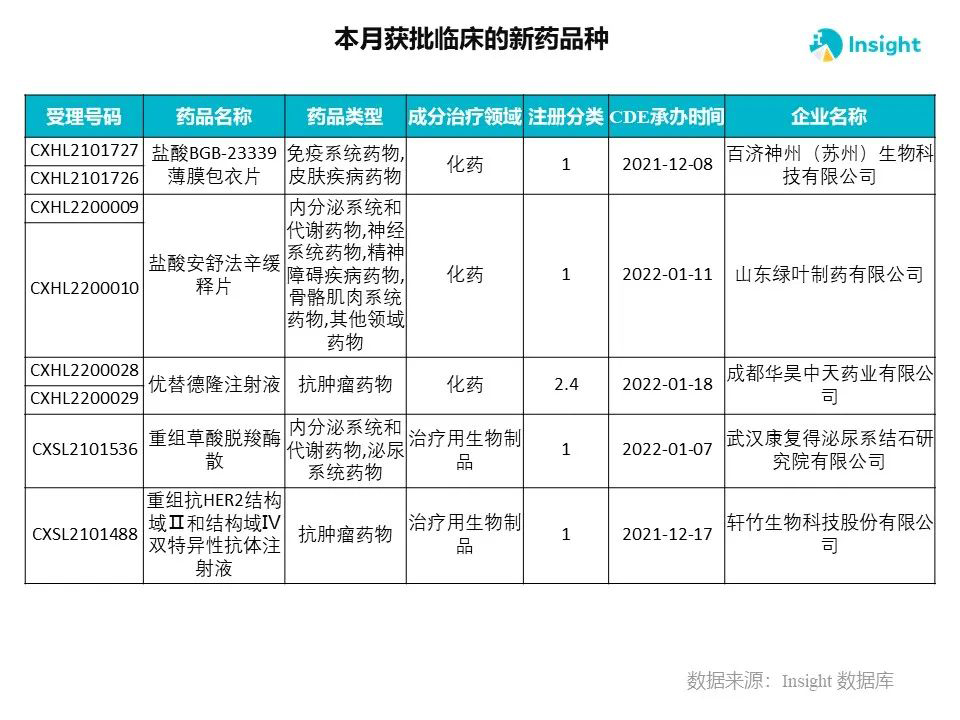
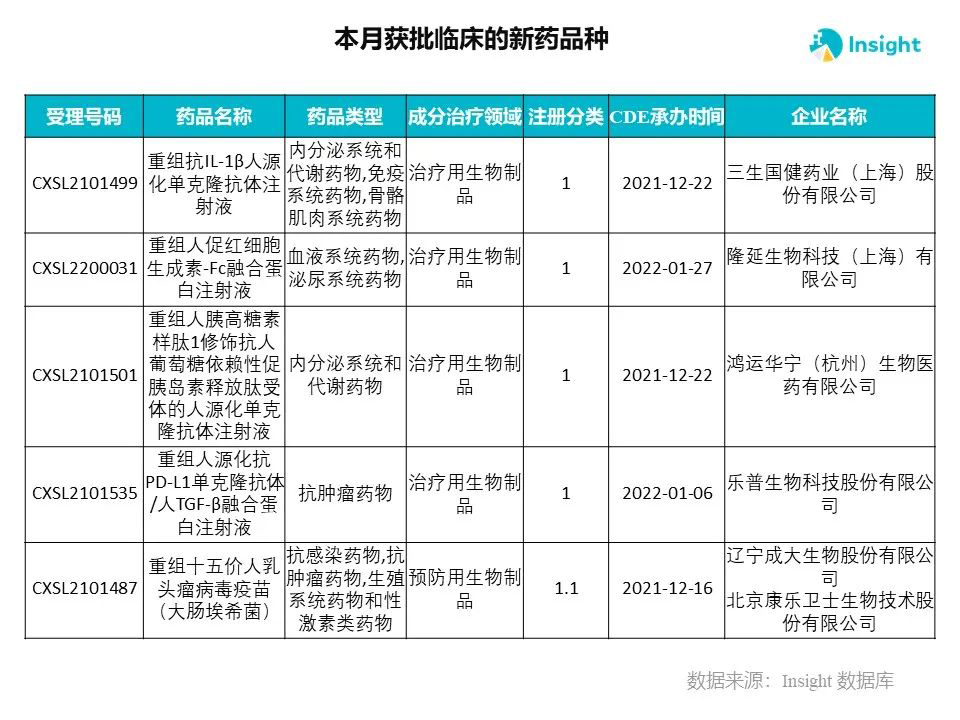
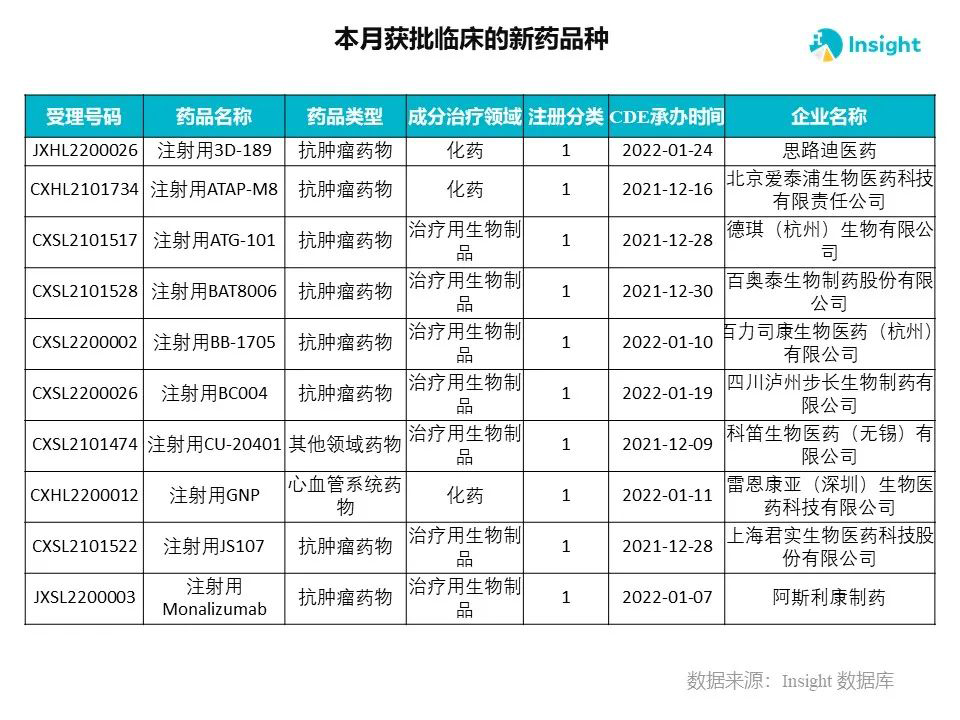
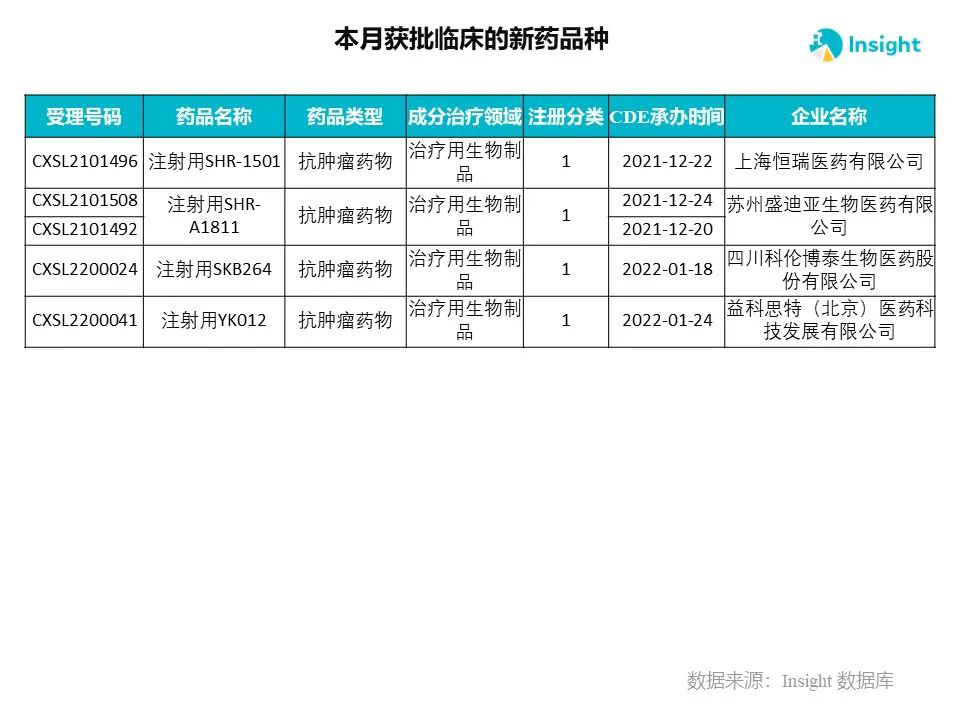
下面是3月获批临床品种的部分重点产品介绍,文章略长,可选择性阅读。
获批临床新药品种介绍
3 月新药获批临床的受理号共 230 个,涉及 145 个品种,部分产品介绍如下。
药品名称:ABSK043 胶囊
企业名称:和誉生物
ABSK043 是一款全新具备较好活性、选择性的小分子 PD-L1 抑制剂。它可与 PD-L1 特异性结合并诱导其从细胞表面内吞,有效抑制 PD-1/PD-L1 的相互作用,恢复 PD-L1 介导的 T 细胞活化抑制。在多个临床前模型中,ABSK043 展现出与已获批抗 PD-L1 抗体相当的抗肿瘤功效。此外,和誉医药还将探索这款口服小分子 PD-L1 抑制剂与其他药物的联合治疗潜力。
药品名称:ABSK061 胶囊
企业名称:和誉生物
ABSK061 是和誉生物原创且拥有全球专利权益的一款 FGFR2/3 选择性抑制剂。通过降低对 FGFR1 的抑制,以及保持对 FGFR2/3 的高活性,ABSK061 有望成为第二代 FGFR 抑制剂,具备比泛 FGFR 抑制剂更佳的安全窗和疗效
药品名称:AC682 胶囊
企业名称:冰洲石生物
AC682 是冰洲石生物基于 AI 药物发现平台开发的一款雌激素受体 α(ERα)降解剂,是一种口服生物可利用的嵌合降解分子,也是国内首款获批临床的 ER PROTAC。本次获批的适应症为 ER+/HER2-局部进展期或转移性乳腺癌。
药品名称:ASP7517 注射液
企业名称:安斯泰来制药
ASP7517 为一款载有 WT1 的人工佐剂载体细胞(aAVC)项目,为安斯泰来与 Riken 公司合作开发。WT1 蛋白是威尔姆斯瘤 1 基因(WT1)编码的转录因子,已有研究显示,它可能在白血病、乳腺癌、卵巢癌等血液癌症和实体瘤中起到致癌作用。
药品名称:AZD8233 注射液
企业名称:阿斯利康制药
AZD8233 是一款靶向 PCSK9 的反义寡核苷酸疗法(ASO),由阿斯利康与 Ionis Pharmaceuticals 公司联合开发。在1期临床试验中,单剂 AZD8233 注射能够将 PCSK9 水平降低超过 90%,将 LDL-C 水平降低高达 70%。目前,AZD8233 正在 2 期临床试验中接受检验。阿斯利康曾在 2021 年的投资者会议上介绍,这款 ASO 疗法可能为患者提供一种在家中可以接受治疗的选择。
药品名称:BC008 抗体注射液
企业名称:宝船生物
BC008 抗体注射液是宝船生物自主研发的抗 CLDN18.2 人源化纳米抗体融合蛋白,能够特异性靶向结合细胞表面 CLDN18.2 分子,激活机体 NK 细胞活性,通过抗体依赖细胞毒作用(ADCC)、补体依赖细胞毒作用(CDC)等 Fc 端功能对 CLDN18.2 阳性肿瘤细胞进行特异性杀伤,发挥抗肿瘤作用。
药品名称:CTA101 UCAR T 细胞注射液
企业名称:北恒生物
CTA101 是被批准进行人体试验的国内首款 UCAR-T 细胞治疗产品,用于治疗成人复发或难治性 B 细胞急性淋巴细胞白血病。UCAR-T 细胞治疗产品是使用健康人的 T 细胞制备完成。相比自体 CAR-T 疗法具有 抗肿瘤活性高、可及性高 等优势。这种细胞治疗产品无需配型,可「现货」存储,即时使用,显著降低患者治疗周期,且一位健康捐献者可制备成百上千人份「现货」,可显著提高细胞治疗可及性。
药品名称:Depemokimab 注射液
企业名称:葛兰素史克制药
Depemokimab 是一款长效 IL-5 拮抗剂,有望实现每 6 个月注射一次就可控制患者症状。该药的独特之处在于对 IL-5 的高亲和力,能够长期抑制 IL-5 的活性。正在进行的 3 期临床研究表明,该药只需要每隔 6 个月接受一次皮下注射就可以帮助重度嗜酸性粒细胞性哮喘患者控制症状,也有可能成为首款治疗重度嗜酸性粒细胞性哮喘的长效生物制品。
药品名称:HY1839 颗粒
企业名称:沪云新药
HY1839 颗粒拟用于治疗炎症性肠病(IBD),包括溃疡性结肠炎(UC)和克罗恩病(CD)。IBD 是一种以上皮损伤和肠道炎症为病理特征的累及消化道的慢性、复发性、炎症性疾病,对患者生命健康和生活质量造成严重的影响。IBD 确切病因与发病机制尚未完全阐明,在疾病发生发展中,遗传、环境、心理等各种因素导致人体肠黏膜屏障功能受损。临床前动物药效模型显示,HY1839 能够显著上调肠道上皮细胞紧密连接蛋白表达,促进粘膜修复,明显改善疾病症状;非临床安全性评价结果显示,本品安全性良好。
药品名称:ICP-488 片
企业名称:诺诚健华
ICP-488 是一种强效的高选择性 TYK2(酪氨酸激酶 2)变构抑制剂,通过结合 TYK2 JH2 结构域,阻断 IL-23、IL-12 和 I 型干扰素等炎性细胞因子的信号转导,从而抑制自身免疫性疾病和炎症性疾病的病理过程。ICP-488 是诺诚健华具有全球自主知识产权的 1 类创新药,是新型口服 TYK2 变构抑制剂,将开发用于治疗银屑病和炎症性肠病(IBD)等免疫炎症性疾病。
药品名称:IMG-020 注射液
企业名称:创响生物
IMG-020 又称 ABY-035,通用名为 izokibep,是 Affibody 公司开发的一种可靶向 IL-17A 的新型双特异性分子。2020 年 5 月,创响生物通过合作获得了该候选药在大中华区、韩国等国家和地区的独家权益,此项合作首付款和里程碑付款高达 2.25 亿美元。
药品名称:JMKX000623 片
企业名称:济煜医药
JMKX000623 是上海济煜自主研发的一款高选择性离子通道阻滞剂,通过阻滞钠离子内流而阻止痛觉发生和传递,有望为各种疼痛患者提供治疗上的有效缓解。
药品名称:PM1015 注射液
企业名称:普米斯生物
PM1015 是普米斯生物开发的人源化抗 CD73 单克隆抗体。据普米斯生物早先新闻稿介绍,与大多数抗 CD73 在研产品不同,PM1015 拥有特殊的结合表位,能在多种表达 CD73 的肿瘤细胞系上完全阻断膜型 CD73 酶活性。本次,该药获批在晚期实体瘤受试者中开展临床试验。
药品名称:PM1032 注射液
企业名称:普米斯生物
PM1032 是普米斯团队自主研发并拥有完整知识产权的抗 Claudin18.2/4-1BB 双特异性抗体,由人源化抗 CLDN18.2 单克隆抗体的 Fc 的 C 端经柔性肽稳定连接抗 4-1BB 人源化单域抗体后获得。PM1032 能够在高表达 Claudin18.2 的肿瘤局部,通过一端结合 Claudin18.2 另一端同时结合 4-1BB 进而特异性地介导激活 4-1BB 信号通路,从而达到增强肿瘤微环境中的 T 细胞活性以及诱导肿瘤抗原特异性的记忆 T 细胞的生成。
药品名称:SCR-6920 胶囊
企业名称:先声药业
SCR-6920 是由先声药业自主研发的一款口服蛋白精氨酸甲基转移酶 5(PRMT5)抑制剂,与甲硫腺苷磷酸化酶 (MTAP) 共同构成一对合成致死基因。合成致死就是单独一种基因失活并不影响细胞生存,但如果两个基因都失活则会导致细胞死亡。
药品名称:SR1375 胶囊
企业名称:赛默罗德
SR1375 胶囊是赛默罗德生物自主研发的糖尿病性视网膜病变治疗候选药。据赛默罗德生物新闻稿介绍,这是一款神经炎性机制小分子抑制剂。它具有全新作用机制,而且可以口服给药,打破了 Anti-VEGF 必须经由玻璃体注射带来的临床应用限制。在动物模型中,SR1375 展现了和 Anti-VEGF 可比的药效,有望为相应的患者提供更方便、安全、有效的用药选择。
药品名称:SSGJ-617 注射液
企业名称:三生国健
SSGJ-617 是国内首款以 PSGL-1 为靶标的拮抗型抗体,可诱导 M2 样巨噬细胞功能重编后转换为 M1 样表型,进而产生抗肿瘤的促炎性免疫应答。其中,PSGL-1(P-选凝素糖蛋白配基-1) 是一种粘附分子,参与响应组织损伤或炎症的免疫细胞运送。巨噬细胞可以响应其微环境中的信号而发挥不同的功能作用,包括指导促炎性和抗炎性免疫反应的能力。
药品名称:ZL-1211 注射液
企业名称:再创生物
ZL-1211 是一款人源化单克隆抗体,能够特异性地与 Claudin 18.2(CLDN18.2)高亲和力结合。ZL-1211 在与表达 CLDN18.2 的癌细胞结合后,可以募集并激活自然杀伤(NK)细胞,从而高效地诱导抗体依赖性细胞介导的细胞毒作用(ADCC)。此外,ZL-1211 与表达 CLDN18.2 的癌细胞结合可激活补体依赖性细胞毒作用(CDC)。本次,该药获批在晚期实体瘤患者中开展临床试验。
药品名称:注射用 3D-189
企业名称:思路迪医药
3D189 为新一代靶向 WT1 蛋白的多肽肿瘤疫苗,属于 First-in-class 创新药。在过度表达 WT1 蛋白的超过 20 种癌症(包括肺癌及结直肠癌)中具备靶向治疗潜质,可诱导产生强大的 T 细胞介导免疫应答的刺激作用,用于预防/延迟复发(通过延长无疾病进展期)及最终有望延长该等患者的生存期。
药品名称:注射用 ATG-101
企业名称:德琪医药
ATG-101 是德琪医药研发的 PD-L1/4-1BB 双特异抗体,此前已分别在澳大利亚和美国获批开展 1 期临床试验。作为一款新型 PD-L1/4-1BB 双特异性抗体,ATG-101 可形成一种基于细胞-抗体-细胞结构的三聚体,阻断 PD-L1/PD-1 结合以及激活 4-1BB 共刺激信号,从而激活抗肿瘤免疫效应细胞,并有效降低肝毒性。
药品名称:注射用 BAT8006
企业名称:百奥泰生物
BAT8006 是百奥泰开发的靶向叶酸受体α(FRα) 的抗体药物偶联物 (ADC),拟开发用于实体肿瘤治疗。由重组人源化抗 FRα抗体与毒性小分子拓扑异构酶 I 抑制剂,通过自主研发的可剪切连接子连接而成。BAT8006 具有高效的抗肿瘤活性,毒素小分子有很强的细胞膜渗透能力,在 ADC 杀伤癌细胞后能释放并杀死附近的癌细胞,产生旁观者效应,有效克服肿瘤细胞的异质性。
药品名称:注射用 BC004
企业名称:步长生物
注射用 BC004 为重组抗 HER2/CD3 人源化双特异性抗体药物,主要用于治疗 HER2 阳性晚期实体瘤,包括 HER2 阳性乳腺癌、胃癌/胃食管交界处腺癌等。
药品名称:注射用 JS107
企业名称:君实生物
JS107 是由君实生物自主研发的注射用重组人源化抗 Claudin18.2 单克隆抗体 MMAE(Monomethyl auristatin E) 偶联剂,是靶向肿瘤相关蛋白 Claudin18.2 的抗体偶联药物 (ADCs),拟用于治疗胃癌和胰腺癌等晚期恶性肿瘤。JS107 可以与肿瘤细胞表面的 Claudin18.2 结合,通过内吞作用进入肿瘤细胞内,释放小分子毒素 MMAE,对肿瘤细胞产生强大的杀伤力。
药品名称:注射用 SHR-1501
企业名称:恒瑞医药
SHR-1501 为白细胞介素-15(IL-15) 融合蛋白,可以刺激体内 T 细胞、B 细胞和 NK 细胞增殖,发挥调动机体免疫系统清除体内异物 (如肿瘤) 的作用。与 IL-2 相比,IL-15 不会刺激 Treg 增殖和诱导 T 细胞凋亡。SHR-1501 目前国外有 ALT-803 等多个相同靶点产品处于临床试验阶段,国内未有相同靶点产品处于临床试验阶段。截至目前,SHR-1501 相关研发项目累计已投入研发费用约 4,383 万元。
▲以上数据来源于 Insight 申报进度数据库

 产业资讯
产业资讯
 细胞基因治疗前沿
细胞基因治疗前沿  2026-06-09
2026-06-09
 442
442

 产业资讯
产业资讯
 药渡Daily
药渡Daily  2026-06-09
2026-06-09
 399
399

 产业资讯
产业资讯
 小药说药
小药说药  2026-06-09
2026-06-09
 418
418
 热门资讯
热门资讯