 产业资讯
产业资讯
 Insight数据库
Insight数据库  2022-07-08
2022-07-08
 5466
5466
转眼,2022 年已过去一半,这半年国内新药开发进展迅速。
Insight 数据库 显示,2022 年上半年国内共有 31 款创新药进入 III 期临床阶段,离报上市仅差一步之遥。布局企业包括恒瑞、天晴、翰森制药等;涉及肿瘤、眼科、免疫、代谢疾病等领域。*1)本文提及的「创新药」包含改良新以及进口药;「III 期临床研究」包含 II/III 期临床研究。2)文中表格为人工整理,如有纰漏请指正。

来源:Insight 整理
聚焦肿瘤领域
15 款产品,10 个癌种
从治疗领域来看,2022 上半年进入 III 期临床阶段的产品多数聚焦在肿瘤领域,共有 15 款。涉及到的癌种有乳腺癌、非小细胞肺癌等热门大癌种,也有结直肠癌、前列腺癌等当前赛道竞争较缓和且极具市场潜力的癌种。
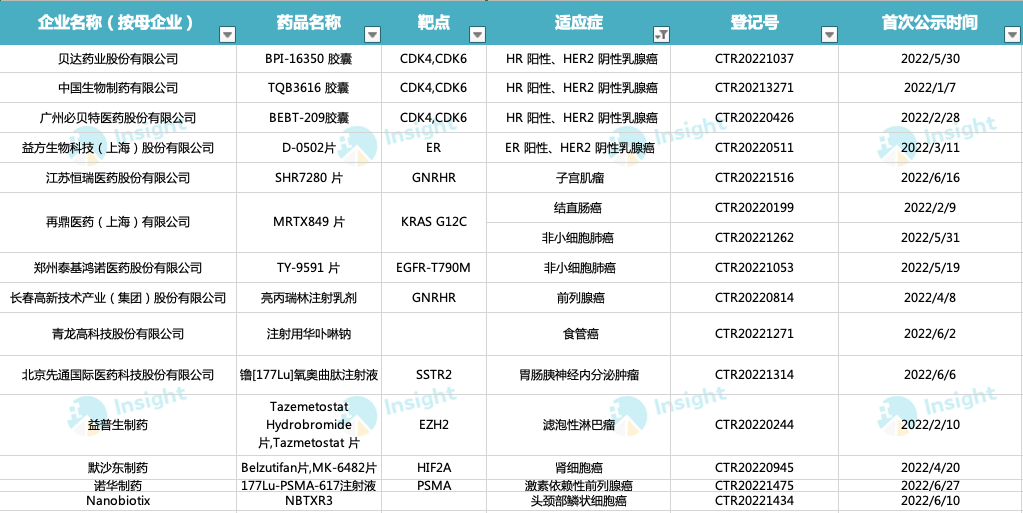
来源:Insight 整理
乳腺癌
针对乳腺癌,共有 3 款 CDK4/6抑制剂和一款口服 SERD 进入 III 期临床阶段。
乳腺癌新药列表
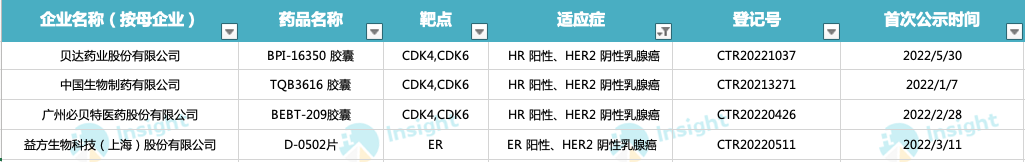
来源:Insight 整理
益方生物 D-0502 是一款口服选择性雌激素受体降解剂 (SERD),同时也是一个雌激素受体拮抗剂,可以有效用于治疗雌激素受体阳性的乳腺癌患者。
D-0502 于 2018 年首次在国内获批临床,2019 年 4 月首次公示临床试验(登记号:CTR20190092),当前正在开展一项对比 D-0502 与氟维司群在既往经治 ER 阳性、HER2 阴性局部晚期或转移性乳腺癌患者中的有效性和安全性的随机、平行对照、开放标签、多中心 Ⅲ 期临床研究。
D-0502 国内项目开发进度
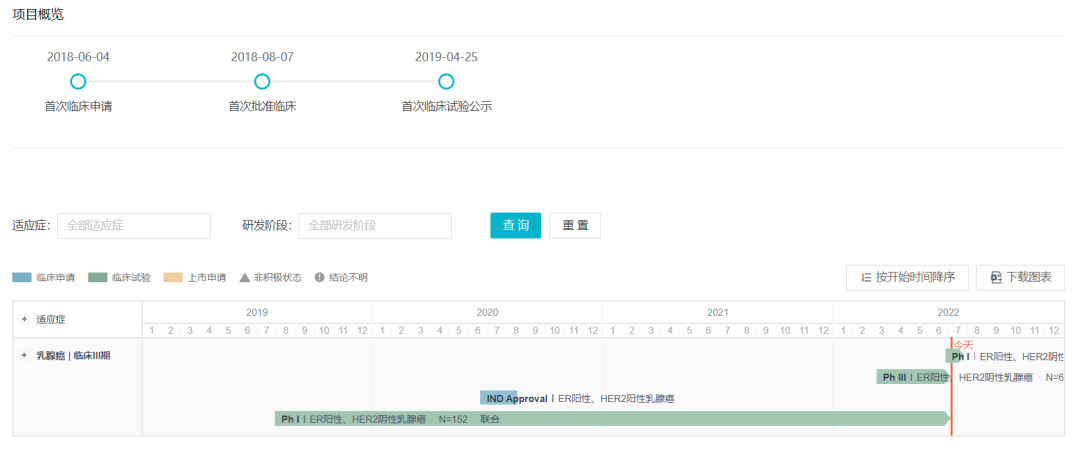
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
贝达药业的 BPI-16350、天晴的TQB3616 以及广州必贝特医药 BEBT-209 均为 CDK4/6 抑制剂,当前正在开展的 III 期临床研究均为联合氟维司群治疗 HR+/HER2- 乳腺癌患者。
CDK4/6 为乳腺癌领域的热门靶点,目前在多份乳腺癌指南中,CDK4/6 抑制剂联合内分泌治疗证据级别均从 Ⅱ 级提升为 Ⅰ 级。因此, CDK4/6 抑制剂也成为更多企业布局乳腺癌领域的热门靶点。
据Insight 数据库 显示,在乳腺癌领域当前全球共有 26 款 CDK4/6 抑制剂在研,其中,礼来阿贝西利、辉瑞哌柏西利、诺华利柏西利以及恒瑞达尔西利均已获批上市,另有 7 款进入 III 期临床阶段。而在国内共有 20 款在研,且处于临床 III 期阶段的有 6 款,未来会有多大市场机会?还未可知。
全球 III 期临床阶段 7 款 CDK4/6 抑制剂
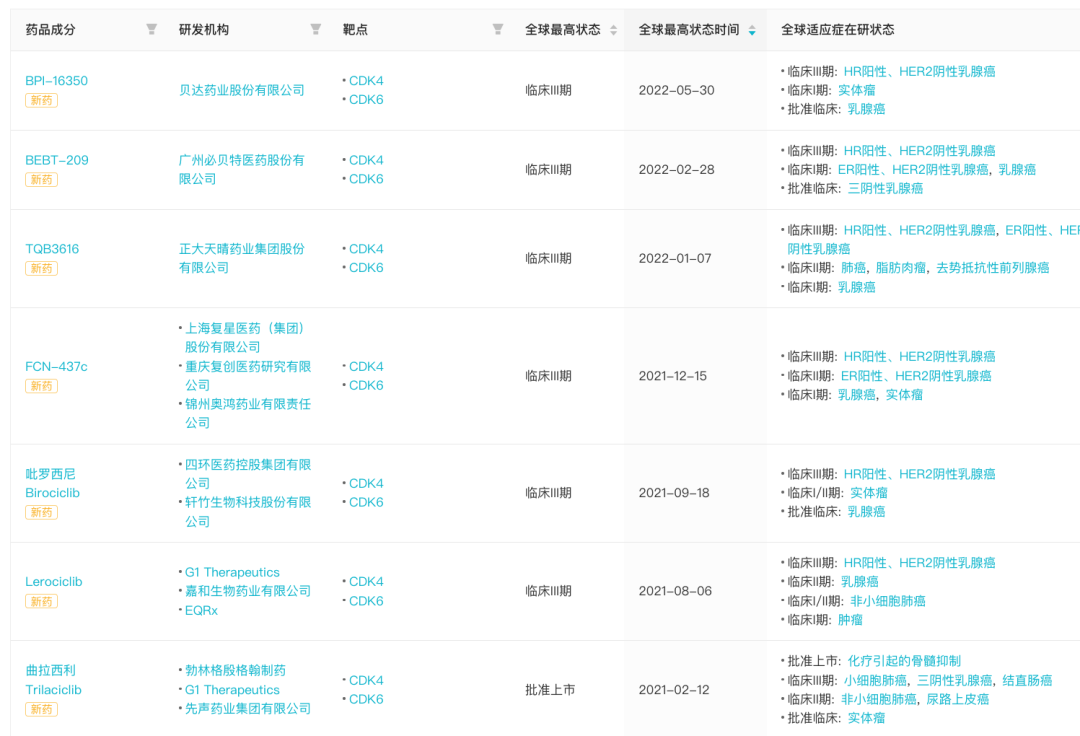
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
非小细胞肺癌
除乳腺癌适应症外,紧随其后的就是非小细胞肺癌,2022 上半年共有 2 款进入 III 期临床,三代 EGFR抑 制剂和 KRAS G12C 抑制剂各一款。
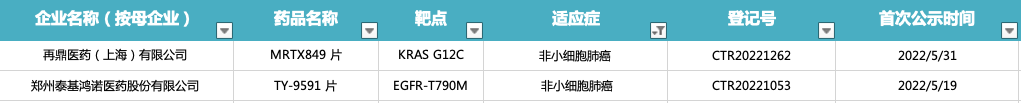
来源:Insight 整理
再鼎医药 MRTX849(Adagrasib)是一种研究性、高选择性的有效口服小分子 KRASG12C 抑制剂。
2021 年 6 月,再鼎医药宣布与 Mirati Therapeutics 达成合作,以 6500 万美元预付款 + 2.73 亿美元里程碑金额获得 Adagrasib 的大中华区开发和独家商业化权利。
Adagrasib 医药交易
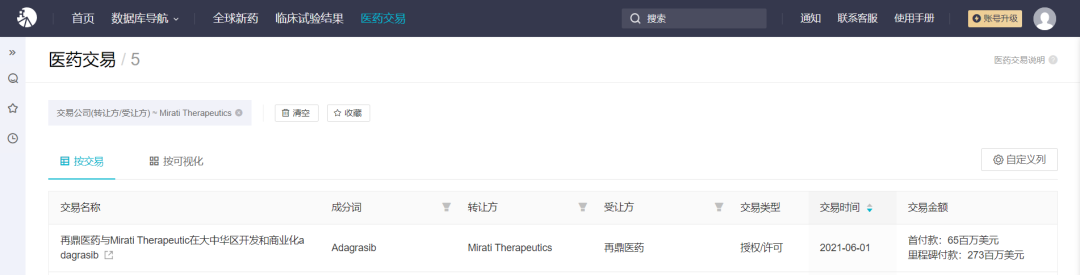
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
近期,Mirati 刚宣布了一项 Adagrasib 在 KRYSTAL-1 队列研究 2 期注册临床队列数据。共有 132 名 患者接受了治疗。在入组的患者中,98% 的患者在化疗后或联合化疗之前接受过 PD-1/L1 抑制剂治疗,中位随访时间为 12.9 个月。初步结果显示:Adagrasib 在 KRAS G12C突变的非小细胞肺癌患者的客观缓解率(ORR)为 44%,疾病控制率(DCR)为 81%,反应持续时间 (DOR) 的中位数为 12.5 个月。
Adagrasib 临床试验结果
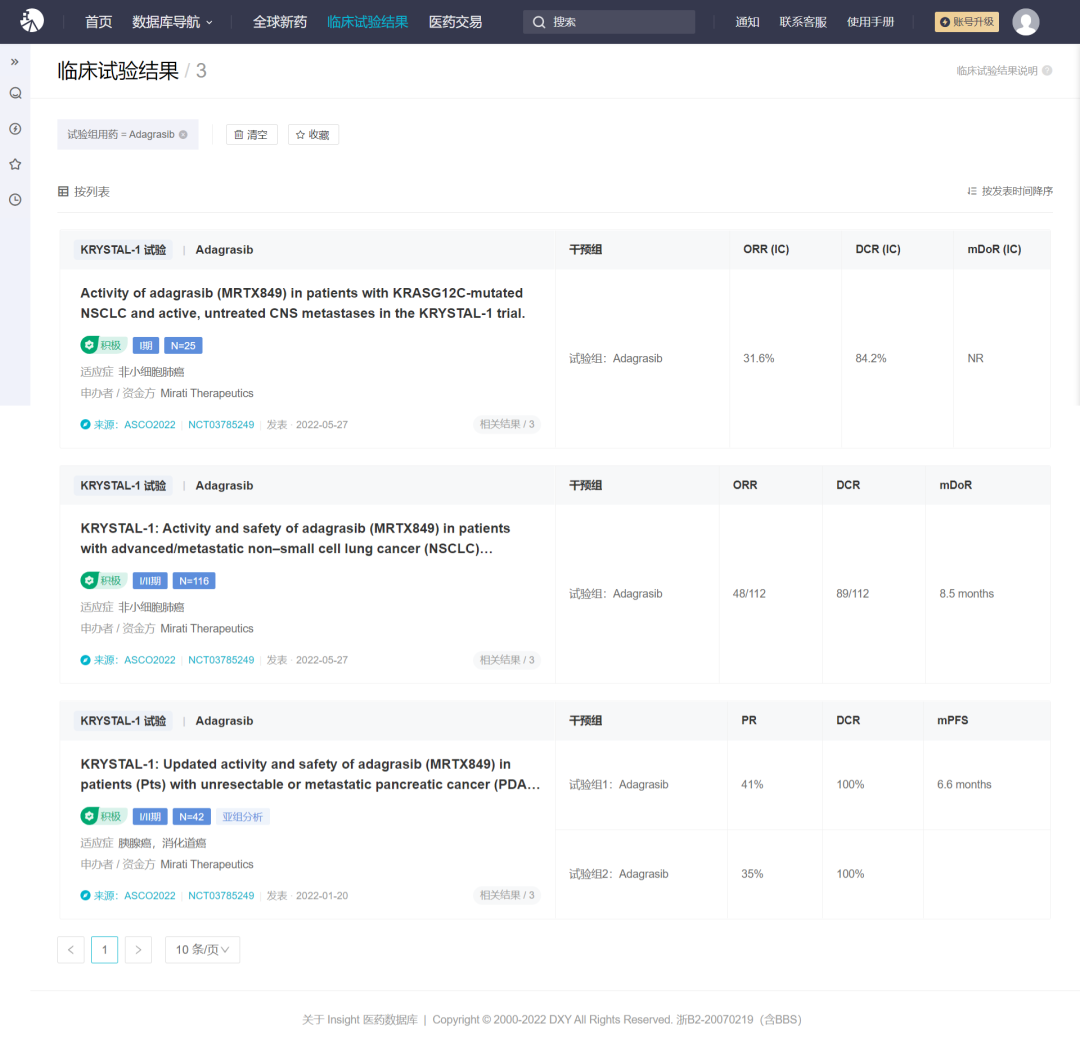
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
当前,除针对非小细胞肺癌外,Adagrasib 同时也在开展一项联合西妥昔单抗用于二线治疗携带 KRAS G12C 突变的晚期结直肠癌患者的 III期研究(登记号:CTR20220199)。
Adagrasib 全球研发进度
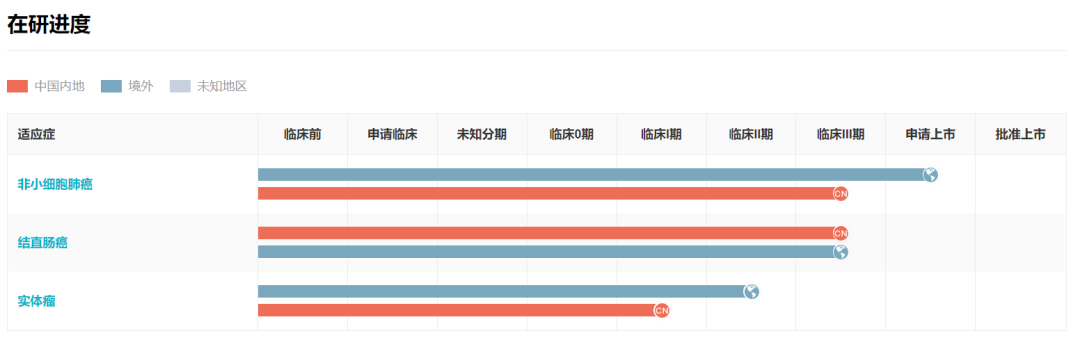
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
郑州泰基鸿诺医药的 TY-9591 是一款三代 EGFR 抑制剂,在今年 5 月刚刚公示启动了一项随机、双盲、多中心III期临床研究,旨在评估 TY-9591 片对比奥希替尼一线治疗 EGFR 敏感突变的局部晚期或转移性非小细胞肺癌患者的疗效和安全性(登记号:CTR20221053)。
TY-9591 项目概览
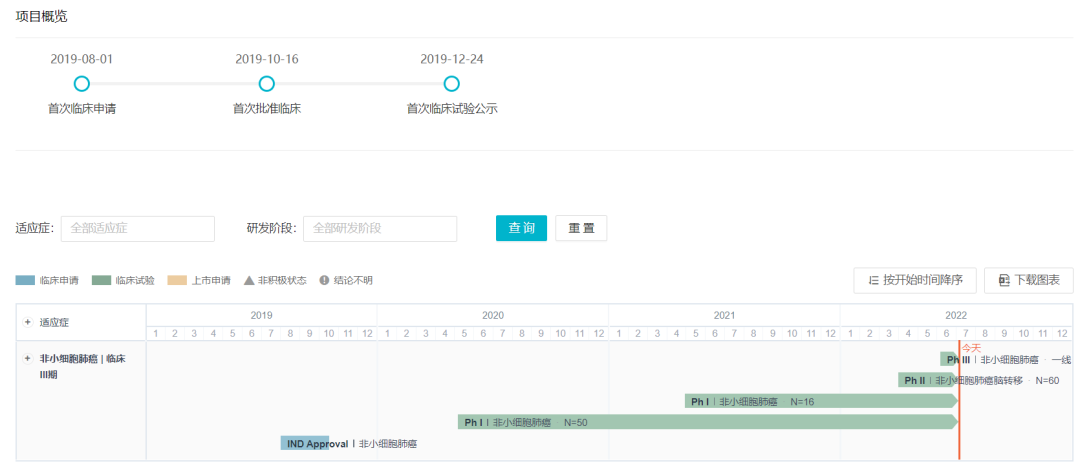
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
除上述的乳腺癌、非小细胞肺癌外,另有 9 款产品正在针对子宫肌瘤、前列腺癌、食管癌、肾细胞癌等多个瘤种开展 III 期临床试验。
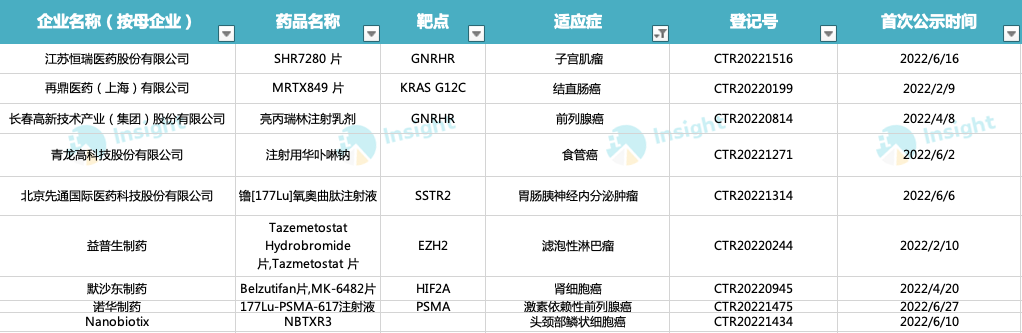
来源:Insight 整理
眼科疾病领域
眼科疾病领域也是近年企业争相挤入的一个赛道,2022 上半年国内 4 款产品进入 III 期临床阶段,分别为极目生物 ARVN003、参天制药株式会社硫酸阿托品滴眼液、大冢制药株式会社 OPC-1085EL 滴眼液以及箕星药业的酒石酸伐尼克兰鼻喷雾剂(OC01)。
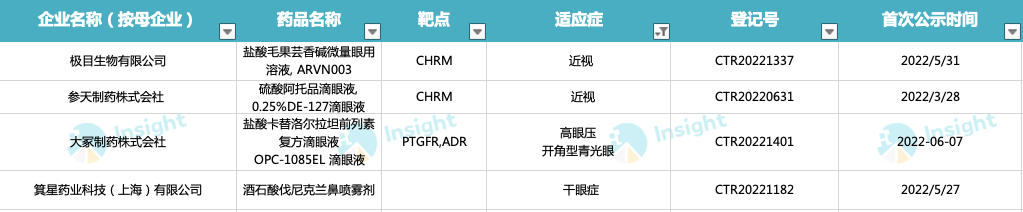
来源:Insight 整理
极目生物的 ARVN003(在美国名为 MicroLine)是一种针对老视的药物疗法。该产品的开发结合了采用 MAP™(Microdose Array Print)微矩阵药膜技术的 Optejet 微量给药系统,以及可以暂时性改善近视力的经典药物匹罗卡品(毛果芸香碱),可有效解决传统滴眼液给予相同药物时的耐受性和生物利用度等问题。
ARVN003 国内项目概览
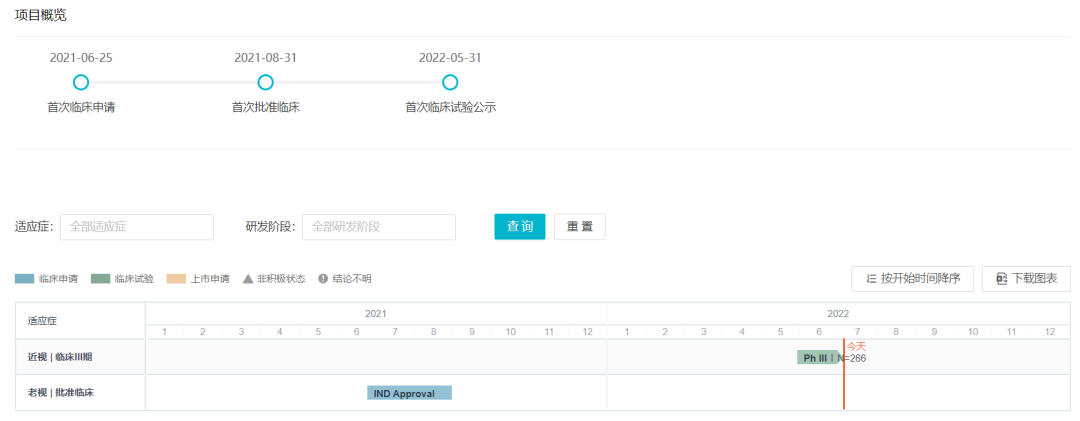
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
2021 年 8 月,ARVN003 治疗老视的 III 期 IND 申请获 CDE 批准,成为国内批准的第一项老视药物临床试验。这是一项老视患者使用微量给药器给予 ARVN00 以暂时性改善近视力的有效性和安全性的随机、多中心、双盲、安慰剂对照、III 期临床研究(登记号:CTR20221337),当前正在进行中。
CTR20221337 临床试验

来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
OC-01 (varenicline) 鼻喷雾剂是多剂量包装、不含防腐剂的高选择性胆碱能激动剂鼻喷雾剂,用以治疗干眼症和神经营养性角膜病变的症状和体征。
在临床前和临床研究中,OC-01 (varenicline) 以不含防腐剂的水性鼻喷雾剂形式给药,可激活鼻腔内三叉神经副交感神经通路从而激活自然泪膜分泌。
2021 年 8 月,Oyster Point Pharma 与箕星药业签署了一项许可和合作协议,根据交易条款,箕星获得了在大中华区开发和商业化 OC-01 与 OC-02 的独家许可。箕星将向 Oyster Point 预付 1750 万美元的现金和高达 0.75% 的箕星股份,其中一半受预先规定的归属条件限制。Oyster Point 也有资格获得高达 2.048 亿美元的里程碑付款,以及未来药物在大中华区净销售额提成。
OC-01 医药交易
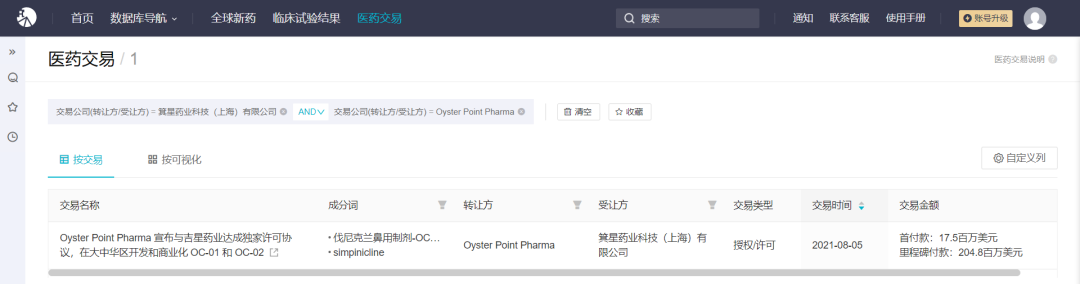
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
OC-01 最早于 2021 年10 月获 FDA 批准上市,用于治疗干眼症。此外,还在拓展其他适应症,当前正在美国开展一项针对神经营养性角膜炎的 II 期临床研究(登记号:NCT04957758)。在国内,正在开展针对干眼症的 III 期临床试验。
OC-01 全球在研进度甘特图
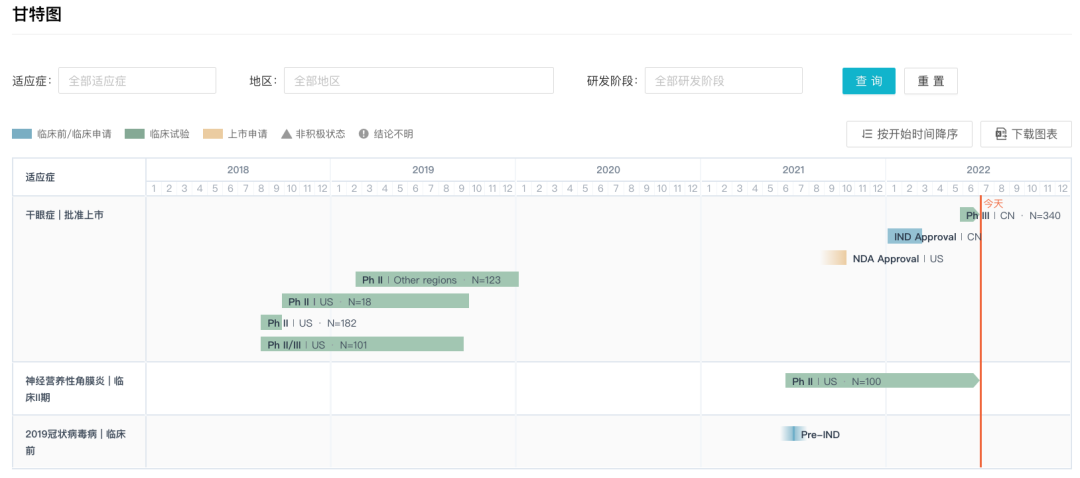
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
DE-127(通用名:硫酸阿托品)是一种抑制近视进展的毒蕈碱受体拮抗剂。参天制药已与新加坡国家级眼科和视觉研究所——新加坡眼科研究所 (SERI) 合作研发这一药物产品线,同时在日本和亚洲开展临床试验。
此前,参天曾发布公告称在亚洲展开的一项旨在评价 DE-127 (通用名: 硫酸阿托品) 用于治疗轻度和中度近视患者的安全性和有效性的 II 期临床实验 (即 APPLE 研究) 达到了主要终点。该研究的主要终点为给药 12 个月后受试者等效球镜度数的变化。整个实验过程中未观察到严重不良事件。
当前,正在国内开展一项在儿童近视受试者中评价 DE-127 滴眼液(不同浓度)的安全性和有效性的随机、双盲、安慰剂对照、平行组、多中心的 II/III 期确证性研究(登记号:CTR20220631)。目标入组人数为 396 人。
DE-127 国内项目概览
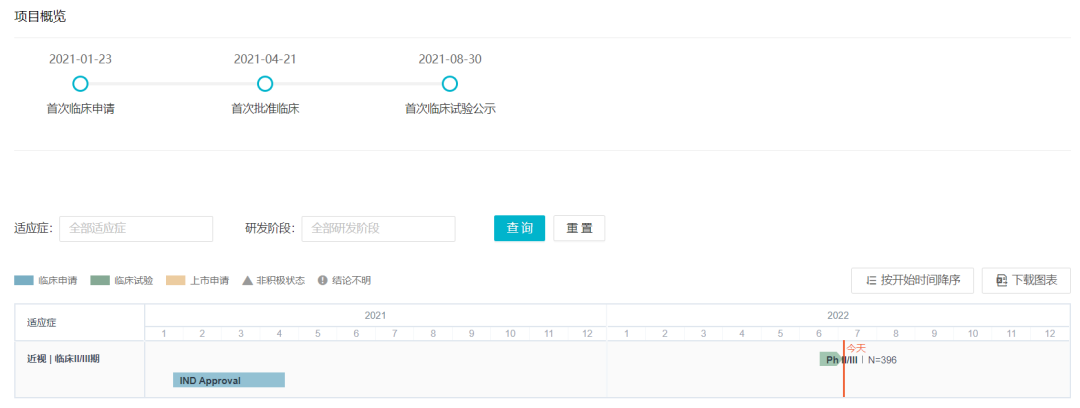
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
CTR20220631 临床试验
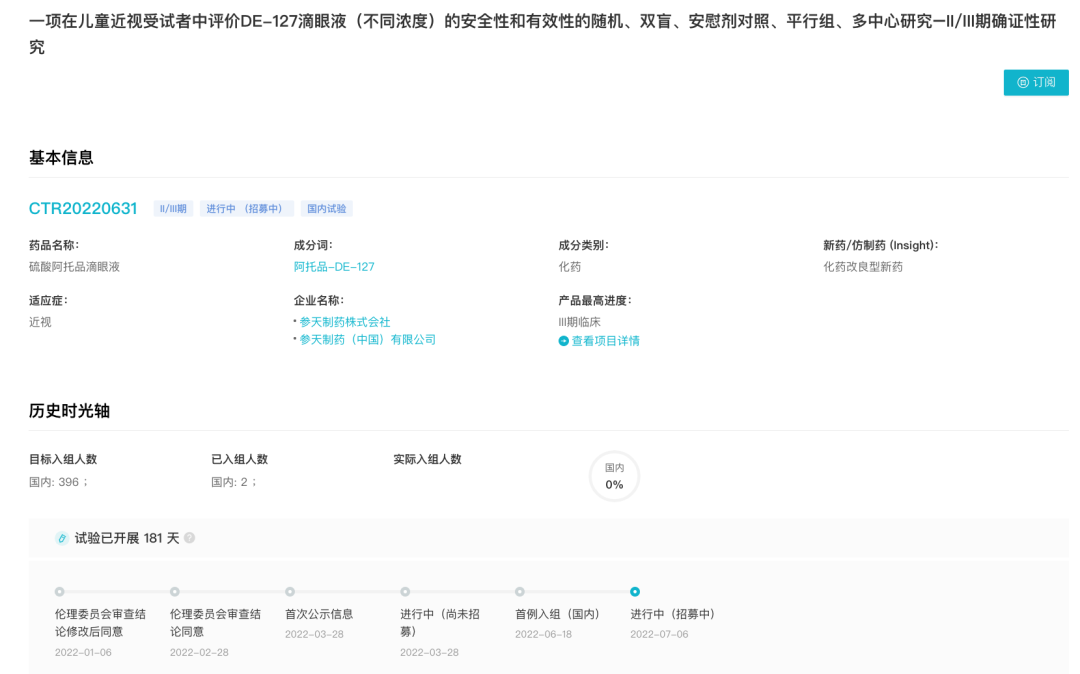
来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
大冢 Mikeluna(卡替洛尔/拉坦前列素)是一款复方滴眼液,由非选择性 β 阻滞剂盐酸卡替洛尔和前列腺素类似物拉坦前列素组成,2 者具有不同的降眼压机制。
盐酸卡替洛尔是一种非选择性 β-肾上腺受体阻滞剂,对 β1 和 β2 受体均有阻滞作用,对高眼压和正常眼压患者均有降眼压作用,其降压机制主要是减少房水生成,对房水经葡萄膜巩膜外流、房水流出易度及巩膜上静脉压无影响。
拉坦前列素则是一种前列素 F2a 的类似物,为选择性 FP 受体激动剂,其主要作用机制为增加房水的葡萄膜巩膜旁道流出,具有良好的降眼压效果。主要用于降低开角型青光眼和高眼压症患者升高的眼压。
通常,青光眼在最初治疗时采用单一制剂治疗,如果眼内压没有得到充分控制,则需要处方额外的药物进行治疗。然而,在应用一种滴眼液之后需要等待一段时间才能应用另一种滴眼液,往往导致治疗依从性下降,而这可能会降低治疗的疗效。将 2 种药物复配在一起,有望显著提高治疗的依从性。
此前 Mikeluna 已在日本获批上市,用于青光眼和高眼压症的治疗。在国内,目前同步开展针对青光眼和高眼压的 III 期临床研究(登记号:CTR2022140)。
CTR2022140 临床试验

来自:Insight 数据库 (http://db.dxy.cn/v5/home/)
除肿瘤、眼科以外,还有针对免疫、代谢等疾病领域的多款产品也于今年上半年进入 III 期临床阶段。

 产业资讯
产业资讯
 细胞基因治疗前沿
细胞基因治疗前沿  2026-06-09
2026-06-09
 442
442

 产业资讯
产业资讯
 药渡Daily
药渡Daily  2026-06-09
2026-06-09
 399
399

 产业资讯
产业资讯
 小药说药
小药说药  2026-06-09
2026-06-09
 418
418
 热门资讯
热门资讯