 产业资讯
产业资讯
 求实药社
求实药社  2023-02-03
2023-02-03
 12144
12144
持续多年的政策与资本支持叠加工程师红利,助推了中国创新药行业的高速发展,创新能力也在不断地提升,越来越多的创新药企业和创新药产品开始有能力走出国门,出海踏入国际市场。当行业还在热议科伦药业子公司科伦博泰与默沙东在2022年达成合同总额超过100亿美元重磅ADC产品合作时,2023年创新药出海的第一枪已经悄然打响。
新年伊始,药明生物于2023年1月5日宣布和葛兰素史克就多款创新TCE双抗/多抗达成许可协议,药明生物将获得4000万美元首付款和最高达14.6亿美元的里程碑付款,且有资格获得基于净销售额的分级销售提成。
创新药企业出海入局国际市场亲自做临床开发和商业化是最直接的形式,但是其门槛相对较高,风险也较大,将国产新药对外许可(License out)给海外药企借力拓展海外市场成为绝大部分国内药企当前的最优选择。近年来License out案例不论是数量还是金额都呈现了快速上升趋势,产品涉及的技术种类也逐年丰富,对外授权的标的也不再限于产品,更多的技术平台也开始获得海外药企的青睐。
本文主要对近年来国内创新药License out进展进行了梳理,并对部分案例进行了分析,以飨读者。
01 Why License out?
2010年经常被认为是中国创新药研发起步的元年,也正是这一年小编踏入大学校门。彼时,国内药企依然以仿制药为主,绝大多数的新兴Biotech们也才刚刚起步,产品定位主要还是中国市场。随着中国生物医药产业进入创新时代的土壤(比如资金、人才以及各类CRO/CDMO服务)逐渐成熟,各类创新产品和技术平台快速进入井喷期。
我们开始有拿得出手的产品,在新的技术赛道如双抗、ADC(Antibody-drug conjugate,抗体偶联药物)、PROTAC(Proteolysis targeting chimera,蛋白降解靶向嵌合体)、CGT(Cell and gene therapy,细胞与基因治疗)疗法等领域与海外药企不再是代际的差距,并逐步有了和海外Biotech甚至MNC(Multinational corporation,跨国公司)掰手腕的能力。
本土创新药企业的研发实力,已逐步得到海外市场认可,国产创新药正在昂首挺胸走向自己的航海时代。仅2022年,我们的多款产品和技术平台就获得了礼来、默沙东、强生、赛诺菲等跨国药企的认可。
“走自己的路,让别人无路可走”,用这句话来形容来近年来中国创新药的内卷也不为过。随着资金的快速涌入和人才红利的爆发,同质化竞争与日俱增,最典型的就是国产PD-1单抗,上市和在研产品过百项,产品售价也从几十万元每年很快下降到三万元左右每年,市场空间直接缩水近十倍。
当然红海泛舟的也不止PD-1,大多数创新药靶点未来都有可能重蹈覆辙,如EGFR、CD19、CD47、Claudin18.2、KRAS-G12C、KRAS-G12D等热门靶点也都有这一苗头显现。近两年CDE发布的《以临床价值为导向的抗肿瘤药物临床研发指导原则》与《新药获益-风险评估技术指导原则》等重磅指导原则,进一步加大同质化产品的临床开发和上市难度,给数量众多的me-too产品来了个釜底抽薪。
此外,受医保参保基数巨大、医保谈判、支付体系改革以及叠加疫情对医保费用的冲击等因素影响,创新药在国内市场无论是定价还是支付端买单能力和意愿都略显萎靡。在行业深刻变革与政策不断演化的大背景冲击下,中国创新药企业不得不被倒逼出海,创新药的IND(Investigational new drug,新药研究申请)申请也大都是中美双报的标配,无论是Biotech还是Big pharma都开始为出海做准备。
目前国产创新药企业出海主要有两种模式:一是自主出海,即中国药企自主在海外开展临床试验和自建销售团队,比如百济神州的BTK抑制剂泽布替尼,但是自主出海对资金和团队要求非常高,成功者屈指可数。二是借“船”出海,主要形式是License out,即药企将自己的产品或技术平台的部分或全部权益售让给海外药企,借助海外药企的经验或渠道实现新药产品和技术平台的出海。
当前我国大部分成熟药企尚不具备直接出海所需的海外临床和商业化能力,对于大多数的新兴Biotech公司,国内市场布局都经验尚浅甚至毫无头绪,海外市场的开发就更加遥不可及。考虑到海外开展临床翻倍的成本和完全不同的商业化环境,使得国内药企面对再大的海外市场蛋糕也只能望洋兴叹。
而选择License out交易模式,不仅在研发端可以通过与海外药企合作,借助对方的各类资源,实现优势互补、降低新药研发风险;销售端还可以借助国际药企的销售网络,实现快速进入国际市场、获得丰厚现金流。
在此背景下国内药企不得不舍近求远去选择门槛更低、风险更小且更为成熟的License out模式实现出海。License out的交易模式因其显著低于自主出海的门槛,能较快获得现金流并助力Biotech公司快速获得资本市场的认可等优势已经成为我国创新药出海最常用的模式。
02 License out简介
2.1License out定义
License out是指企业进行药物早期研发,然后将项目授权给其他药企做后期临床研发和上市销售,按照里程碑模式获得各阶段临床成果以及商业化后的一定比例销售分成。一般通过合作双方签署药品技术许可协议,产品许可方将知识产权、技术资料、研发数据等许可给被许可方,约定向许可方支付一定首付款,并约定后续的里程碑款项及未来的销售提成,从而被许可方获得在其所在地区或全球范围内的研发、生产和销售的商业化权利。近年来License out的标的也在逐步多元化,开始从早期的单一产品逐步拓展到系列产品组合以及技术平台等。
2.2License out定义
1)许可范围
License out主要交易条款之一是关于许可范围的约定,许可范围决定了一项产品或技术许可能涵盖的地域、行为以及用途等,将影响项目未来发展和其能够发挥的作用与价值。许可范围一般包括知识产权范围、地域范围、行为范围和用途范围等。作为交易文件核心条款之一,创新药企业在对外授权的交易谈判中,应根据具体情况选择最适合自身商业诉求和发展规划的许可范围。
2)支付对价
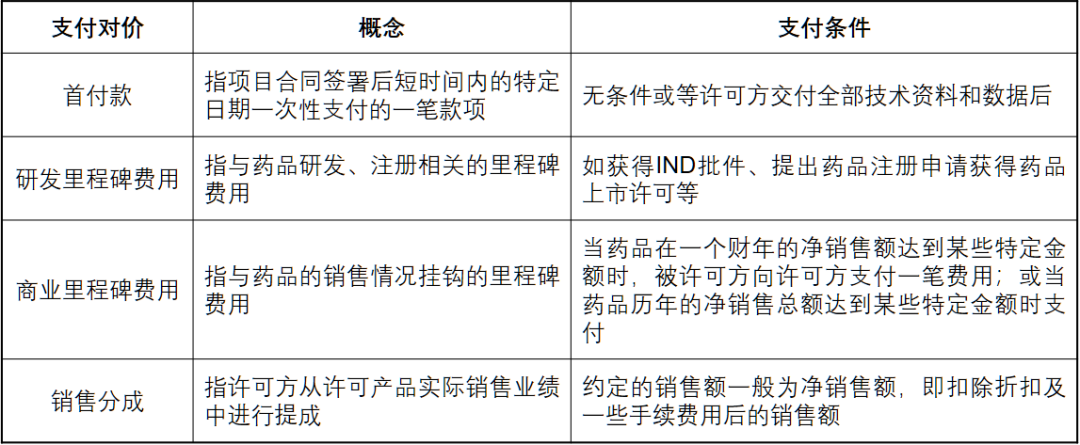
License out主要交易条款之二是支付对价,支付对价一般包括首付款(Upfront payment)、里程碑费用(Milestone payment)以及销售分成。其中里程碑费用又分为研发里程碑费用(Development milestone payment)和商业里程碑费用(Commercial milestone payment)。如果说,交易总额意味着产品未来潜在价值的大小,那么首付款,则更多意味着买家对该产品未来价值兑现概率的判断和信心。
表1 支付对价分类
03 我国创新药License out现状
近年来,我国创新药企业License out交易日趋活跃,无论从交易数量、金额还是项目种类方面都逐年增高,整体呈现出三大趋势:
(1)产品技术类型更加多样,除了小分子和单抗类项目,双抗/多抗、细胞疗法、ADC、疫苗等也相继出海进入国际市场;
(2)更多企业参与,从Biotech、Biopharma到Big pharma都有相关案例报道,通过对外授权实现短期内资金回笼,对Biotech的融资和已上市公司股价的上涨都有积极作用;
(3)被授权方更加多元化,过去国内创新药企业License out的对象多为大厂,比如礼来制药、强生、阿斯利康等,但这两年越来越多的海外Biotech也参与进来,部分交易的首付甚至都超过了被授权方的市值。
3.1整体概况
1)近年来License out交易情况梳理
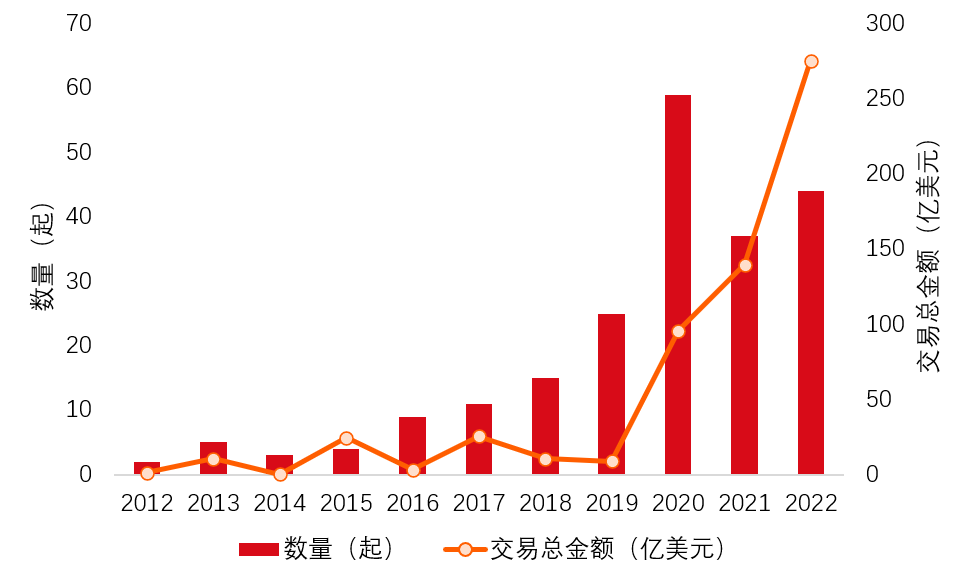
图1 我国创新药License out数量和交易总金额 数据来源:康橙投资、公开信息
2006年,微芯生物将自主研发的西达本胺发明专利授权给HUYABIO International(沪亚生物国际)进行大中华区以外的海外市场开发,成为我国首个实现License out原创新药。
此后,一直到2012年才开始有零星的License out案例报道,据不完全统计,2012年中国创新药License out事件仅发生2起,披露的交易金额仅1.4亿美元。从2018年开始,不论是交易数量还是交易金额都开始快速增加;在刚刚过去的2022年,中国创新药License out交易发生了44起,披露的交易金额达到275.50亿美元,相比2021年交易总额翻倍。
截止2022年底,中国创新药/新技术的对外授权总计已超过220起。近两年虽然交易数量略有下降,但是交易总额上依然实现了突破性增长。
2)产品与技术平台授权情况梳理
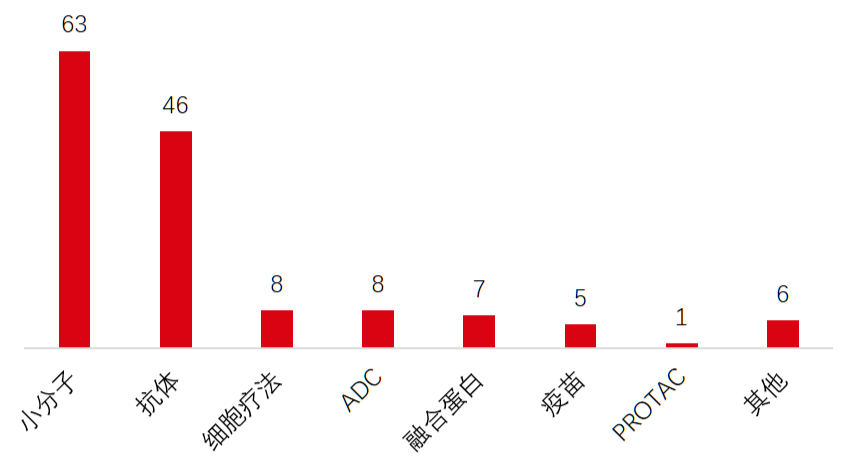
图2 我国License out创新药产品授权分类 数据来源:康橙投资、公开信息
本文将根据对外授权的标的不同,将License out分为创新药产品授权和技术平台授权两种。截止2022年底,我国共有145起创新药产品实现对外授权,其中小分子占比最高,共有63起,占总量的43%,但近年来占比呈现逐渐下降趋势;其次是抗体药物,共有46起,其中双抗产品占比快速上涨;细胞疗法和ADC授权项目占比增速也较快,仅2022年ADC相关授权就达到了7起,默沙东和科伦药业三次合作,均为ADC相关产品。
此外,2022年济民可信与Genentech(基因泰克)关于临床前口服雄激素受体PROTAC分子达成总金额高达6.5亿美元的授权合作,亿帆医药仅靠融合蛋白F-627(艾贝格司亭α注射液)授权给不同公司不同地区的权益完成了5次License out交易,都是非常值得关注的。
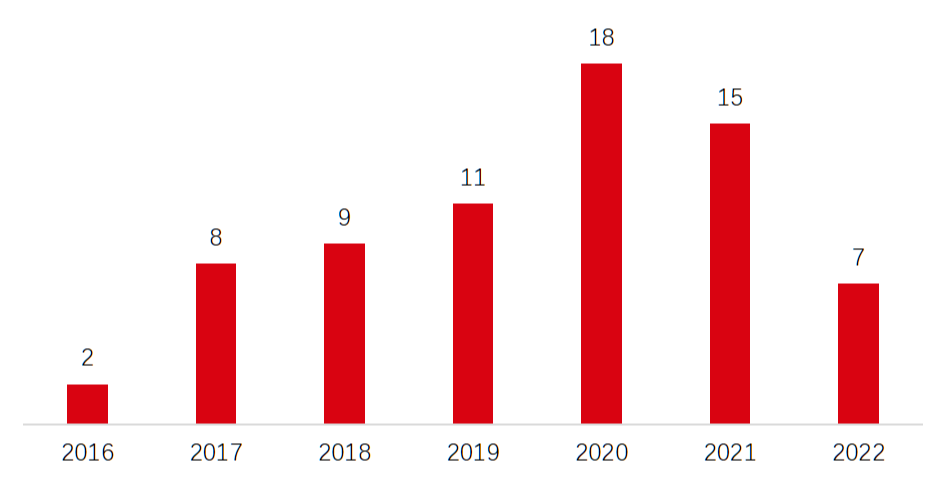
图3 我国License out技术平台授权数量 数据来源:康橙投资、公开信息
截止2022年底,我国已达成69起技术平台的对外授权,其中以DNA编码化合物库(DNA encoded library,DEL)技术授权最多,达到28次;其次是AI药物发现平台授权。技术平台类型也是朝着多元化快速发展,从早期的小分子药物筛选平台,逐步向单/双/多抗高通量筛选平台、AAV病毒载体设计、3D药物打印技术等新兴领域延伸。
3.22022年我国创新药License out盘点
如果说2020年是中国创新药License out元年,那么2022年则是国产创新药License out爆发之年。2022年我国药企达成44起License out跨境交易,而前十大License out交易总金额更是高达229.77亿美元,高于2021年全年交易总金额;其中多家药企达成2起以上License out跨境交易,多家跨国药企如默沙东、赛诺菲和默克等在中国完成不止1起项目的引进。
1)治疗领域
从治疗领域来看,2022年实现License out的产品主要集中在肿瘤方面,虽然近年来占比已经呈现下降趋势,但是2022年占比依然高达50%;其次是自身免疫类疾病和神经系统疾病,这两类适应症对应患者基数大,同时优质产品较少,存在巨大的未满足临床需求,也逐步成为新药开发的热点;代谢类疾病与感染等相对成熟的赛道,随着研发热度的下降,则相应产品数也较少。
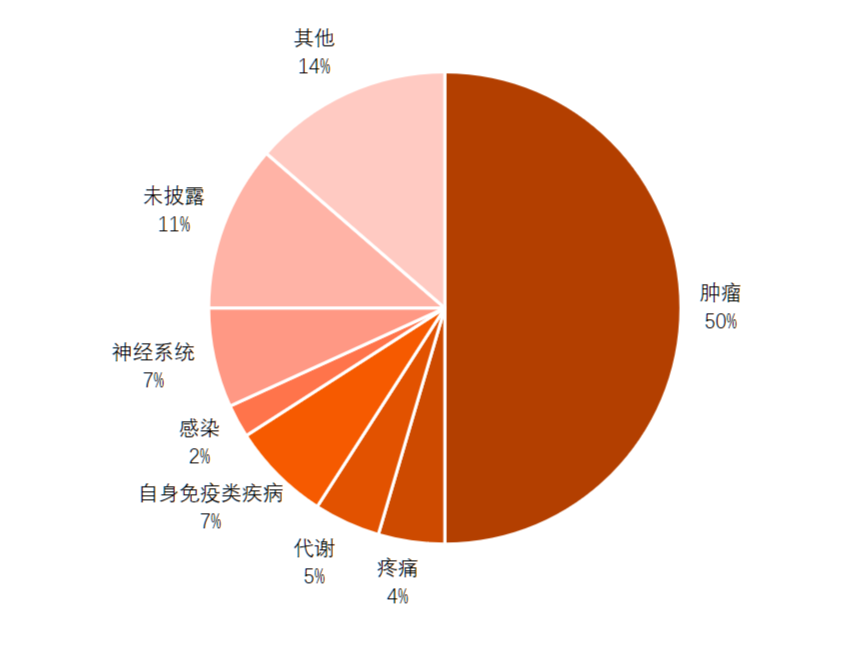
图4 2022年我国创新药License out治疗领域分布图 数据来源:康橙投资、公开信息
2)研发阶段
2022年License out交易中药品技术所在阶段非常多元化,包含临床前阶段、临床Ⅰ期阶段、临床Ⅱ期阶段、临床Ⅲ期阶段、NDA与上市后阶段。根据统计,2022年我国跨境License out交易中药品技术处于上市后阶段占27%,占比第一;其次为Ⅰ临床期阶段(24%)、临床前阶段(22%),从统计数来看近年我国创新药企业License out交易项目研发阶段在逐渐靠前。

图5 2022年我国创新药License out交易项目研发阶段分布图 数据来源:康橙投资、公开信息
3)2022年中国创新药License out交易TOP10
通常而言,交易总额包括首付款和里程碑款两部分。其中,里程碑款,需要后续达成各种临床成就后才能解锁。2022年中国创新药License out交易TOP10中,从交易总金额来看,共有6起License out交易金额突破10亿美元;单项最高交易金额近100亿美元,为科伦药业和默沙东关于合作开发七款临床前ADC候选药物项目的合作协议。
科伦药业和默沙东年内连续三次交易项目均是ADC药物,TOP10中ADC药物占比过半。康方生物与Summit Therapeutics关于PD-1/VEGF双抗合作的首付款即达到5亿美元,在国内License-out首付榜单中排第二,仅次于百济神州与诺华关于替雷利珠单抗合作的6.5亿美元,要知道Summit Therapeutics达成协议时账目资金才1.2亿美元,也算是“蛇吞象”交易在License-out领域的典例。
表2 2022年我国创新药License out交易TOP10
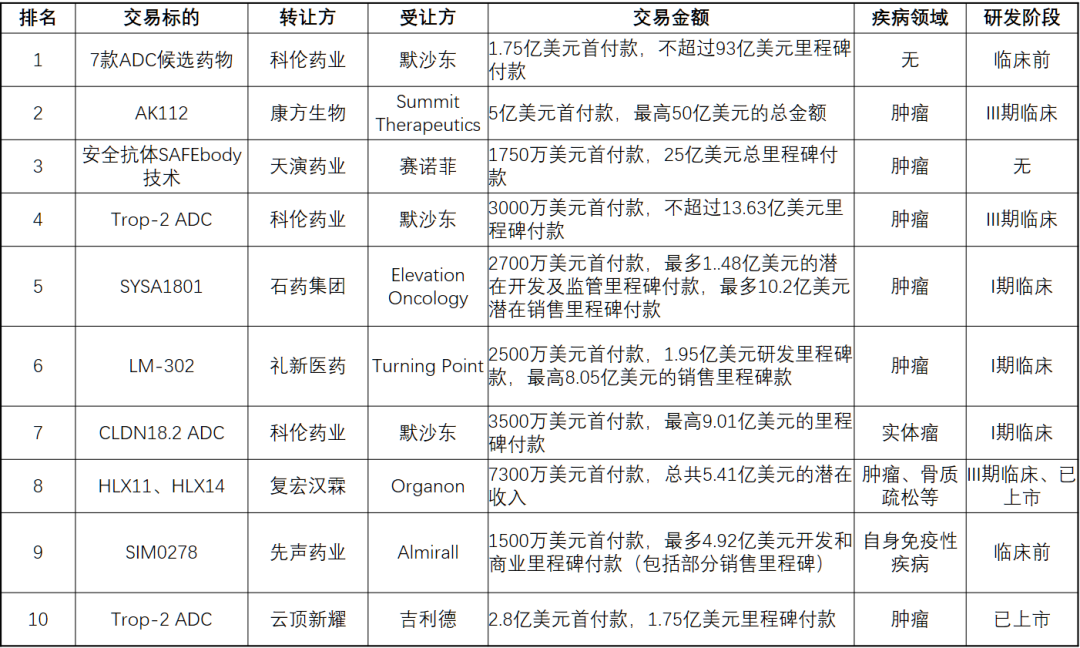
TOP10数据来源:康橙投资、公开信息
04 4.1默沙东和科伦药业关于ADC药物的合作
2022年12月22日,科伦药业发布公告称,与默沙东签署了合作协议,子公司科伦博泰将其管线中七种不同在研临床前ADC候选药物项目以全球独占许可或独占许可选择权形式授予默沙东在全球范围内或在中国大陆、香港和澳门以外地区进行研究、开发、生产制造与商业化。科伦博泰将收到一次性合计1.75亿美元不可退还的首付款,预计会收到默沙东里程碑付款合计不超过93亿美元。

图6 默沙东和科伦药业关于ADC药物的合作历程 图片来源:康橙投资
案例点评
该项交易是截至目前我国历年License out记录中单次合作总金额之最,而这已经是科伦药业在2022年年内第三次与默沙东进行ADC药物的合作,前两次的合作均为ADC产品,合作金额分别为13.63亿美元与9.36亿美元。
跨国药企与本土大药企深度绑定合作的案例不少,但是一年内连续三次签署重磅研发合作项目的属实不太多,12月29日科伦药业公布子公司科伦博泰完成新一轮融资,其中默沙东参与增资1亿美元,这进一步表明了默沙东对科伦ADC平台和研发能力的充分认可。
科伦药业多年来小分子药物和生物工程技术上的积累为科伦博泰在ADC药物研发和平台形成带来了得天独厚的优势,2012年启动转型以来科伦投入研发创新的资金也已累计超过90亿元,厚实的行业积淀辅以坚定的巨额研发投入,使得科伦在ADC领域快速建立了领先优势,还拥有自主研发的两套linker和两套毒素。
科伦从仿制药快速起步,以仿制药推动创新药,以创新药驱动未来增长,再借力MNC实现出海,十年卧薪尝胆,终实现华丽转身。此外,值得注意的是,这种掺杂着项目权益转移和股权交易的License out交易,大概率是未来全球范围内药企之间合纵连横的新式潮流。
4.2礼来和信达生物关于信迪利单抗的合作
2020年8月,礼来和信达生物就信迪利单抗的海外权益达成合作。礼来获得中国以外市场的权益,信达生物则能够获得2亿美元的首付款和8.25亿美元的开发和销售里程碑付款,另外还将收到两位数比例的净销售额提成。
2022年2月10日,FDA召开ODAC会议,审评信达生物与礼来制药的PD-1抗体信迪利单抗能否获批,最终投票结果为14:1,未获通过。2022年11月1日,礼来在其第三季度财报中表示,已经终止了涉及中国以外地区的Tyvyt(信迪利单抗)交易,并于10月将该药退回信达生物。

图7 礼来和信达生物关于信迪利单抗的合作历程 图片来源:康橙投资
案例点评
这项合作的首付款与里程碑款都不低,是国内创新药License out出海的代表作,在当时极度内卷的PD-1赛道也算是实现了成功突围,此后布局同一靶点的百济神州、恒瑞医药、君实生物也都尝试通过License out模式将PD-1产品推向大洋彼岸。
本次信达生物从礼来方面收回了PD-1的海外权益,虽然双方合作仍在继续不断地加深,但不难看出随着双方信迪利单抗产品与其他国产PD-1产品屡次闯关FDA接连受挫后,市场整体对国产PD-1产品的出海前景并非十分乐观。
无独有偶,2022年君实生物与阿斯利康也宣布终止PD-1单抗合作,双方“牵手”合作不到一年;EQRx也宣布决定不寻求FDA批准基石药业PD-L1抑制剂Sugemalimab(舒格利单抗)治疗转移性非小细胞肺癌的上市申请。
对于PD-1/PD-L1这样过度同质化的赛道,如果不能通过合理的临床设计促成FDA的批准上市,License out也可能只是暂时的逃避,后期的里程碑付款和销售提成也就成了空头支票。
一直以来美国市场都是中国创新药出海的首选,随着FDA审批逐步趋严,市场规模仅次于美国的欧洲,以及人口基数同样庞大的东南亚等,也能成为药企出海的新选择。
4.3强生和传奇生物关于西达基奥仑赛的合作
2017年12月,传奇生物与强生达成合作协议共同开发靶向BCMA的CAR-T疗法LCAR-B38M,中国权益两家按70:30共同承担成本和分享收益,海外权益则为50:50,强生支付3.5亿美元预付款。
2022年2月28日,FDA正式批准传奇生物/强生的BCMA CAR-T疗法Ciltacabtagene autoleucel(西达基奥仑赛,即早期的LCAR-B38M)上市,用于治疗复发性/难治性多发性骨髓瘤,商品名为Carvykti。截至目前,强生已经支付3亿美元里程碑金额,潜在里程碑金额仍有10亿美元左右。2022年该产品还陆续在欧盟、日本获批上市。

图8 传奇生物和强生关于西达基奥仑赛的合作历程 图片来源:康橙投资
案例点评
2017年传奇生物凭借LCAR-B38M在ASCO会议上惊艳的临床数据,很快收到了强生抛来的橄榄枝,并迅速达成了重磅合作,成为中国第一款完成License out的细胞疗法产品。如今也成为第一款临床阶段完成授权,并实现在海外上市的产品,仅获批上市不到半年,西达基奥仑赛销售额就达到4800万美金(约为3.3亿人民币,截至2022年6月30日)。
西达基奥仑赛在美国的成功获批和商业化,开启了国产细胞治疗产品出海欧美的先河,而传奇生物也成为众多细胞治疗上市公司中唯一一个股价持续维持高位的药企(2023年1月12日收盘总市值86.68亿美元)。
西达基奥仑赛美国获批上市时定价为46.5万美元,上市不到半年销售额即达到3.3亿人民币,相比国内药明巨诺的瑞基奥仑赛注射液129万/针,复星凯特的阿基仑赛注射液120万/针,在享受更高定价的同时,也收获了更为可观的收益。
— 小结和展望 —
2010年国内创新药刚起步,受限于企业经验和能力的有限和快速补充管线促进融资的需求,我们在市场上看到更多的都是从海外药企License in的产品,借助License in也诞生了再鼎医药、德琪医药、云顶新耀等多家港股和美股上市公司。但是,随着港股和美股医药板块的持续下挫,以及科创板对License in模式的质疑,近年来License in的声音也不像之前那么响亮。
此消彼长,经过多年的耐心耕耘与沉淀,国内药企的创新药出海不断迎来高潮,License out逐步成为医药板块交易的主旋律。或许不少人会认为创新药出海是国内药企面对市场内卷的不得已而为之,但我们不能否认的是,更主要的原因是我们有能力做出得到海外药企和市场认可的产品。
国产创新药出海,进军新大陆已然不仅仅是一个美好的愿景,中国药企们已经成功迈出了第一步,我们相信中国的创新药企业能搭乘自己的“桑尼号”在航海之路上找到自己的“One piece”。
License out模式逐步成熟,案例也逐年增加,呈现出一片欣欣向荣的景象,但是我们仍需保持冷静,继续打磨更好的产品。2022年,仅仅PD-1/PD-L1系列产品,就宣布了三项合作终止案例,License out交易TOP10中的云顶新耀将Trop-2 ADC产品Trodelvy授权给吉利德(而实质是退还给吉利德子公司Immunomedics),云顶新耀将获得2.8亿美元预付款和不超过1.75亿美元里程碑付款,虽然相比其License in的价格有所增值,但市场更多的解读还是为了现金流的被迫之举。
近两年在小编接触的众多创新药项目中,License out也经常成为企业推介的亮点之一,不少创新药企对License out的追求如饥似渴。License out对缓解紧张的现金流和后续的融资确实较为有益,但是交易中存在的一些现象也值得从业人员和投资者保持关注,如十亿美元级别的合作首付款仅为数百万美金,产品尚在早期研发阶段就在商业计划书中许诺目标实现数千万美金的首付款合作,将系列产品的首付和里程碑付款确认为主营业务收入并以此作为财务指标申请上市。
License out是国内药企出海的破局利器,但绝不是万能神药。不论是授权方,还是被授权方,亦或投资机构,都需要耕耘打磨,大胆假设,小心求证,才能在众多的珍宝中找到真正的库里南钻石。

 产业资讯
产业资讯
 药智网
药智网  2026-05-28
2026-05-28
 555
555

 产业资讯
产业资讯
 珍立拍
珍立拍  2026-05-28
2026-05-28
 608
608

 产业资讯
产业资讯
 药明康德
药明康德  2026-05-28
2026-05-28
 475
475
 热门资讯
热门资讯