 产业资讯
产业资讯
 药明康德
药明康德  2023-02-14
2023-02-14
 3814
3814
FDA肿瘤卓越中心发布年度报告
近日,美国FDA肿瘤卓越中心(Oncology Center of Excellence,OCE)发布2022年度报告。报告显示,美国FDA在2022年总计批准12款肿瘤学新药和54款与肿瘤学相关的医疗器械。具体信息请见下图。
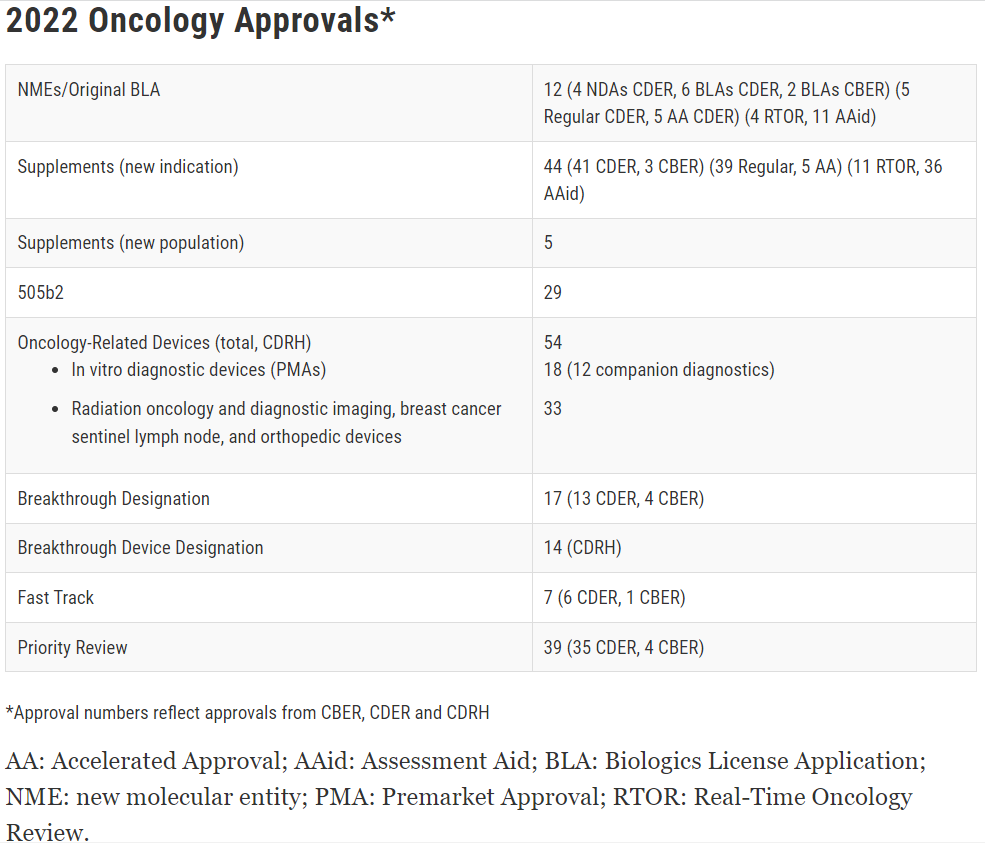
图片来源:参考资料[1]
报告指出,在2022年,OCE领导了不限癌种肿瘤学药物开发指南的制定,并且设立了专门职位来促进不限癌症开发项目的一致性和政策规划。在2022年,值得关注的不限癌种批准包括,dabrafenib/trametinib组合用于治疗BRAF阳性实体瘤,以及RET抑制剂selpercatinib用于治疗局部晚期或转移性RET融合阳性实体瘤。
此外,中心主任Richard Pazdur博士表示,在2022年OCE致力于推动肿瘤学药物开发过程中证据收集方式的现代化,让获得的临床试验数据能够满足当今患者和他们医生的需求。多项举措在2022年启动,其中包括:
Beyond Breakthrough项目:这一试点项目旨在针对获得突破性疗法认定,然而尚未获得批准的肿瘤学产品,聚焦于通过早期与开发商的互动,支持选择药物剂量的策略。
FrontRunner项目:目前的肿瘤学开发项目通常首先针对接受过多种疗法治疗的复发/难治性肿瘤开发创新疗法。FrontRunner项目的目标是将药物开发模式转向晚期/转移性肿瘤的更早临床阶段,目前这一项目正在与多个利益攸关方进行讨论,评估业界对这一策略的兴趣,并且发现这一策略可行并且合适的临床场景。
Pragmatica项目:这一项目的目标是探索针对已经获批的肿瘤学医疗产品,探索创新临床试验设计策略,评估将实用因素整合到多地区癌症临床试验中的机遇和挑战。
相关链接:
https://www.fda.gov/about-fda/oce-annual-reports/2022-oce-annual-report

 产业资讯
产业资讯
 药通社
药通社  2026-06-06
2026-06-06
 514
514

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2026-06-06
2026-06-06
 414
414

 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-06-06
2026-06-06
 433
433
 热门资讯
热门资讯