 产业资讯
产业资讯
 医药笔记
医药笔记  2023-02-24
2023-02-24
 2219
2219
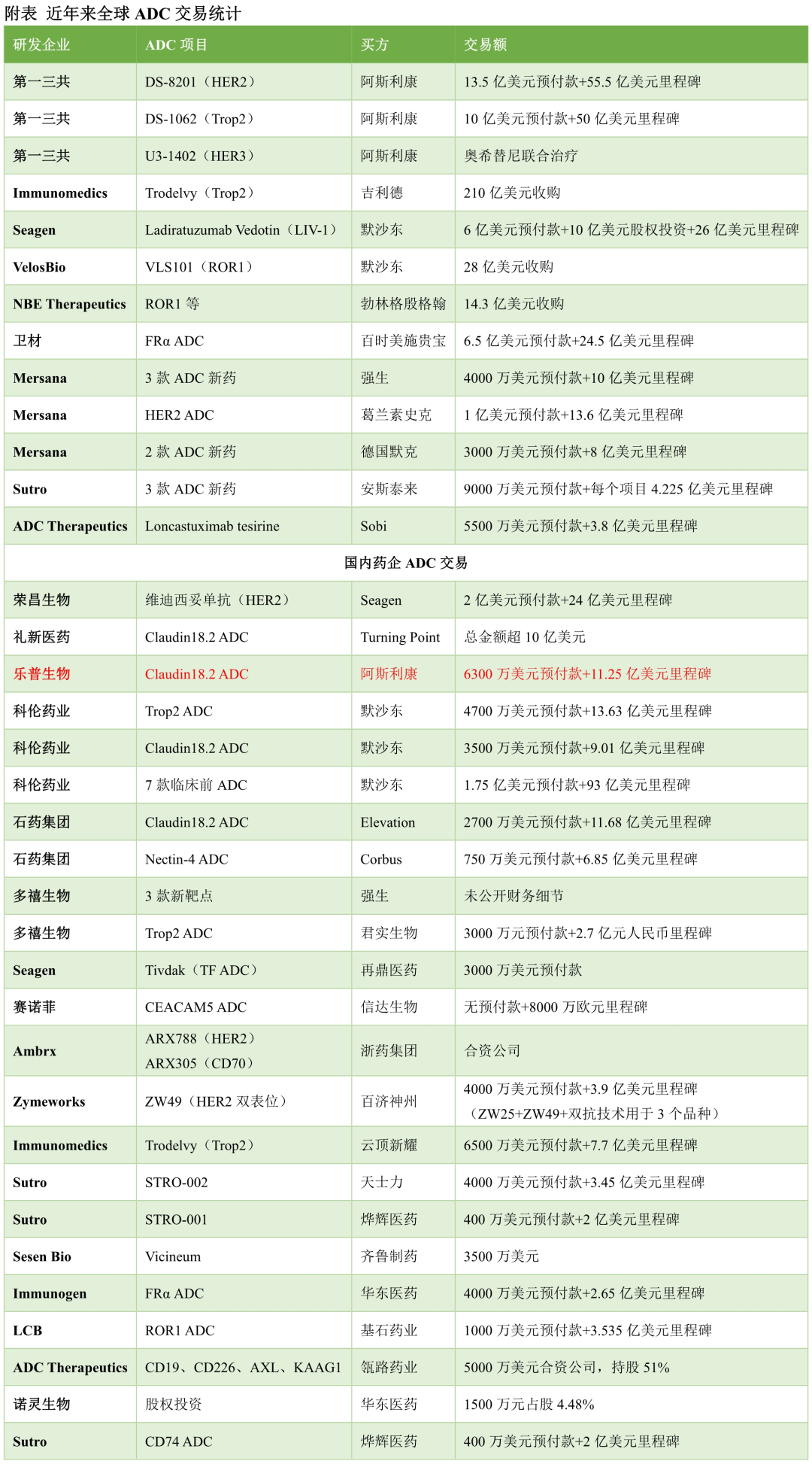
2023年2月23日,乐普生物宣布将Claudin18.2 ADC新药CMG901的全球权益授权给阿斯利康,后者支付6300万美元预付款、11.25亿美元里程碑金额以及一定比例的销售分成。


根据公开信息,CMG901乐普生物和康诺亚共同开发,由Claudin18.2人源化抗体,通过可裂解linker偶联MMAE毒素,乐普生物负责ADC技术,康诺亚负责抗体。

CMG901为全球第一款Claudin18.2 ADC新药,临床前展示出强大的抗肿瘤活性。
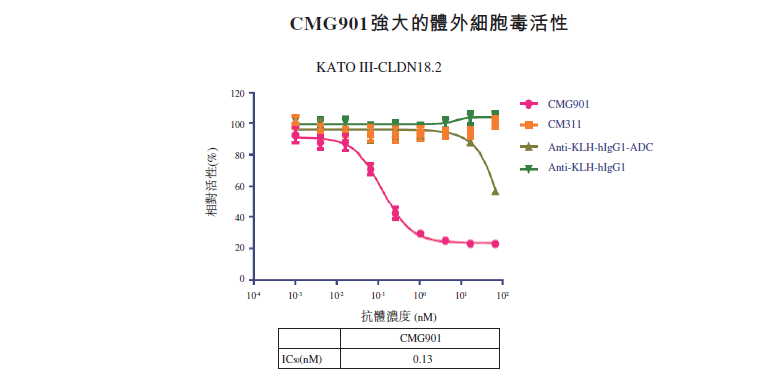
前不久,康诺亚生物刚刚在ASCO GI 2023会议上报告了CMG901的初步临床数据。CMG901 Ia期临床共入组27例患者(13例患有胃癌/胃食管结合部腺癌,14例患有胰腺癌)。研究结果显示,CMG901安全性和耐受性良好,3/27例(11.1%)患者发生药物3级相关不良事件,没有发生4级及以上药物相关不良事件。剂量递增成功至3.4 mg/kg,且尚未达到最大耐受剂量(MTD)。仅2.2 mg/kg组1例患者发生剂量限制性毒性。
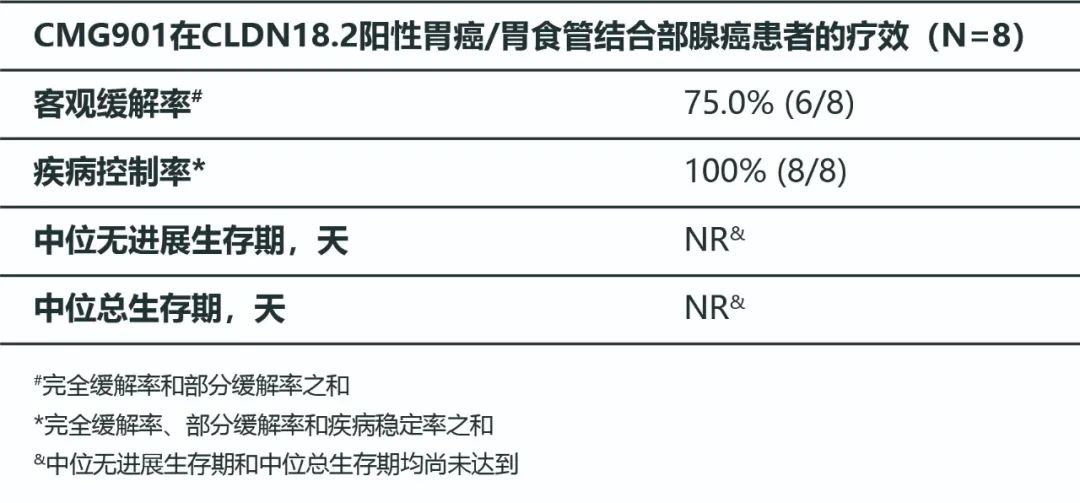
疗效方面,8例接受CMG901治疗的Claudin 18.2阳性胃癌或胃食管结合部腺癌患者中,客观缓解率为75%,疾病控制率为100%。其中,2.6、3.0和3.4mg/kg队列患者的客观缓解率均为100%。中位无进展生存时间(mPFS)和中位总生存时间(mOS)均尚未达到。
阿斯利康在ADC领域布局已久,尤其是与第一三共就3款ADC新药达成了超百亿美元合作,DS-8201更是以一己之力带动ADC进入第二波发展热潮。值得注意的是,DS-8201的胃癌适应症已经获批,此次引进乐普生物的Claudin18.2 ADC,表明其对CMG901的高度认可。
总结
乐普生物建立了具有竞争力的ADC技术平台和产品管线,在国内处于领先地位,目前有5款ADC新药进入临床阶段,靶点分别是EGFR、HER2、CD20、TF和Claudin18.2。此次合作,标志着乐普生物ADC技术和管线得到跨国药企的充分认可,6300万美元预付款金额也创造了早期临床阶段ADC药物出海授权合作的纪录。

 产业资讯
产业资讯
 中国科学院上海药物研究所
中国科学院上海药物研究所  2025-07-12
2025-07-12
 37
37

 产业资讯
产业资讯
 智药局
智药局  2025-07-12
2025-07-12
 38
38

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2025-07-12
2025-07-12
 37
37