 产业资讯
产业资讯
 佰傲谷BioValley
佰傲谷BioValley  2023-03-02
2023-03-02
 4783
4783
截至至今,在PARP抑制剂领域,阿斯利康与默沙东共同研发的Olaparib(商品名Lynparza)仍然是全球市场上最受欢迎的药品。2022年,阿斯利康Olaparib总收入29.93亿美元,是其肿瘤业务中的第二大单品,同比增长9%;默沙东Olaparib总收入11.16亿美元,同比增长13%。Olaparib去年拿下41.09亿美元的好成绩,占据了PARP抑制剂市场份额的60%以上,且在前列腺与胰腺癌适应症上独占鳌头。可以说Olaparib似乎已是一枝独秀,但留给阿斯利康与默沙东快乐的日子可能还未许久,尤其是在前列腺癌上,未来的挑战者已来势汹汹。辉瑞的弯道超车之路近日,美国临床肿瘤学会泌尿生殖系统癌症研讨会(ASCO GU)公布了三项 III 期研究数据,预示了PARP抑制剂联合抗雄激素药物在前列腺领域的激烈竞争。辉瑞的Talazoparib(Talzenna)和强生/GSK的 Niraparib(Zejula)正面入局,试图击败大幅领先,早早获批的前列腺癌适应症的阿斯利康Olaparib。
ASCO GU 在2023年2 月 16 日公布的这三项 III 期研究具体为:
●PROpel 研究:阿斯利康的Lynparza® (Olaparib)联合强生的Zytiga (abiraterone acetate)和prednisone或prednisolone;
●TALAPRO-2 研究:辉瑞的Talzenna (Talazoparib)与自家的Xtandi (Enzalutamide)联合疗法;
●MAGNITUDE研究:强生/GSK的Zejula (Niraparib)/ Zytiga (abiraterone acetate)。
值得一提的是,来自NCI的Neeraj Agarwa宣布辉瑞TALAPRO-2试验的结果时表示,辉瑞的PARP联合疗法将支持其在所有前列腺癌患者的一线治疗,且无论患者的BRCA等基因突变状态如何。
而此前阿斯利康Olaparib获批的适应症就被限制在sBRCA突变的前列腺癌。
不要小瞧这个是否BRCA的限制。在BRCA基因突变的肿瘤细胞中已经存在同源重组修复缺陷(HRD),此时再应用PARP抑制剂,就能同时抑制单链断裂的损伤修复,使细胞DNA无法通过这两个通路进行修复,进而促进肿瘤细胞的凋亡,发挥更强的抗肿瘤作用。
简而言之,如果HRD阴性,通常会降低PARP抑制剂有效性。这也在此前的卵巢癌适应症中就给了各大药企蒙头一棍!
最开始GSK/强生的Zejula与Clovis的Rubraca基于其PFS数据,都获得了所有卵巢癌患者的适应症。但在后续的试验数据中,BRCA基因未突变的患者服用Zejula后的表现的比对照组更差。于是去年11月,FAD将GSK的Zejula的二线维持标签限制为仅适用于BRCA突变患者。随后FDA又要求Clovis公司做出类似的限制,接连回撤Rubraca的适应症,这一举直接导致了以Rubraca谋生的Clovis公司走向破产。
回头来看,辉瑞的数据能否反应其完全符合所有前列腺癌患者的一线治疗,似乎还有待商榷。
TALAPRO-2的数据显示当Talzenna + Xtandi疗法面对HRD阴性的患者时,PFS获益明显下降。除此之外,在对比Xtandi单独疗法与Talzenna + Xtandi联合疗法时,疾病进展风险降低27% (p<0.001),这种影响极有可能是由HRD阳性患者所驱动的(风险比0.46),尤其在那些HRD阴性的患者(风险比0.66)中更加明显。
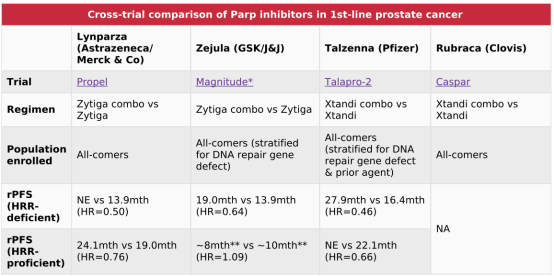
四款PARP抑制剂对比
这一情况在阿斯利康以及GSK的PARP抑制剂临床试验中也有展现。与HRD阴性患者对比,在HRD阳性患者中使用PARP抑制剂,没有显著的益处。
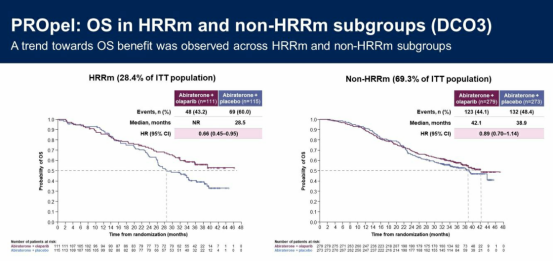
市场拓展 vs 监管收紧
前列腺癌作为男性的第二大癌种,其潜在的市场价值是毋庸置疑的。当阿斯利康(AstraZeneca)于2021年9月公布PROpel的顶线数据时,分析师就曾预测,美国每年有3至5万名有资格接受一线治疗的患者,仅在美国市场该适应症上就可以带来30亿至50亿美元的销售额。
如今阿斯利康的Olaparib作为仅有的获批HRD阳性前列腺癌适应症的PARP抑制剂,能够拿下六成以上市场不禁让各大药企眼红。如果能够解除HRD的限制,那么无论是前人或后来者都将极大的拓展市场价值。
不过对于FDA等监管机构而言,去年卵巢癌适应症上的各大回撤势必会使如今在前列腺癌上的审批更加严格。阿斯利康与默沙东去年12月便试图将Olaparib扩展到所有前列腺癌人群,不过FDA仍然将其行动日期推迟了三个月。不冲突的是,适应症的扩大这也是辉瑞其他等药企不遗余力争取前进的方向,未来FDA能否让各大药企如愿以偿,还需时间来揭晓。
参考资料:
1.https://xueqiu.com/5964803315/243012042
2.https://mp.weixin.qq.com/s/Sq82YRDpvtoleGVtHpI4gg

 产业资讯
产业资讯
 药通社
药通社  2026-06-06
2026-06-06
 525
525

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2026-06-06
2026-06-06
 425
425

 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-06-06
2026-06-06
 443
443
 热门资讯
热门资讯