 产业资讯
产业资讯
 药咖荟
药咖荟  2023-03-10
2023-03-10
 4616
4616
目前,全球共有2.63-4.46亿罕见病患者,已知的罕见病近7000种。面对罕见病庞大的患者群体,以及诊断难、治疗难、费用高的诊疗困境,数以万计的个人与团队奔跑在为希望发声的路上,以期病有所医、医有所药及药有所保。
2月26日,中国生物医药产业链创新与转化联盟孤儿药分会、中国孤儿药创新联盟、豌豆Sir、药咖荟共同发起的“中国孤儿药创新沙龙”国际罕见病日特别活动《患者推动孤儿药可及性的中国实践》线上直播圆满落幕。中国生物医药产业链创新与转化联盟孤儿药分会主委郑维义博士、遗传学与罕见病科普公益平台“豌豆Sir” 创始人陈懿玮博士,以及7位中国罕见病患者组织的负责人,共同分享了各自组织在推动孤儿药可及性方面的实践与洞见。
专业人才深度协助
搭建患者组织、政府部门、医疗机构
与新药研发企业的沟通桥梁
郑维义 博士
中国孤儿药创新联盟 发起人
苏州诺景生命科技有限公司 董事长
南京师范大学罕见病基因治疗联合研究中心 主任
中国生物医药产业链创新与转化联盟孤儿药分会 主任委员
国家重大人才工程项目 A类专家
郑维义博士在报告《孤儿药的诞生:从研发到上市》中,分享了目前国内的孤儿药研发集中在:发病率较高的罕见病(血友病,地贫,SMA和眼科等)、罕见肿瘤治疗药物(有扩展适应症的能力,享受美国孤儿药支持政策)、氘代罕见病新药,以及仿制药孤儿药适应症。如何更好地给予小众罕见病患者关注是当前孤儿药研发的难点。
郑维义博士指出,2022年国家药监局发布“以患者为中心”的药物研发相关的四个指导原则(征求意见稿),明确了“以患者为中心”的药物研发是指以患者需求为出发点、视患者为主动参与者、以临床价值为最终目的的核心指导思想。指导原则的发布,使中国孤儿药研发的临床试验直接获益,患者招募周期从之前平均30个月缩短到7个月左右,不仅提高了II期和III期临床试验药物获批的可能性,也有效解决了孤儿药研发过程中患者招募慢的问题。

陈懿玮 博士
遗传学与罕见病科普公益平台“豌豆Sir” 创始人
中欧智慧医疗研究院 特邀研究员
中国生物医药产业链创新与转化联盟孤儿药分会 秘书长
医疗技术的发展、法规的协调、企业的参与和社会资源投入都是应对罕见病诊疗的关键力量,而豌豆Sir平台则搭建了多方沟通的专业桥梁。深耕遗传学与罕见病科普领域的第七年,豌豆Sir已为近70个罕见病患者社群提供科学传播的服务与支持,惠及超过50万患者个体,成长成为中国罕见病领域最有影响力的科学传播平台之一。
作为豌豆Sir的创始人,陈懿玮博士明显地感觉到这七年间大众对于罕见病关注度的极速上升,与此同时,传递罕见病患者的声音显得愈发重要。近期,由豌豆Sir发起的公益项目——“让罕见病科普更暖心”,被腾讯公益平台选为2023年国际罕见病日【罕见人生,“药”有所依】特别活动的3个重点支持项目之一,并已募集社会各界的爱心小红花超过20万朵。相信在爱心力量的汇入下,将更有效地推动罕见病的宣传倡导、营造善意良好的社会大环境。

患者组织跨界融合
推动罕见病宣传教育、科研临床、
药物开发、政策倡导等多环节发展
黄倩 女士
重庆市九龙坡区蚕宝儿社会工作服务中心 理事长
中国LNS诊疗与科研联盟 联合发起人
中国残疾人康复协会罕见病康复专业委员会 委员
Lesch-Nyhan综合征 患儿家长
在《患者组织驱动的LNS自然史研究》中,黄倩女士分享了蚕宝儿LNS罕见病关爱之家在科学研究、临床协作、国际合作、学术交流等方面的努力。目前,LNS的发病率仅为38万分之一,尚无明确的致病机制,科研极其有限。而自然病史的研究,有助于帮助患者及患者家庭更好地认识疾病发展、制定照护方法,帮助医生提升诊断、治疗及多学科管理,帮助政府制定更科学合理的公共卫生保障策略。
2019年,陈懿玮博士与黄倩女士联合发起了中国LNS诊疗与科研联盟。在关爱之家与联盟诸多学者专家的共同推动下,首个《中国LNS诊断共识(2020版)》面世、全球范围内样本量最大&调研内容最丰富的《中国LNS患者生存状态调研报告》发布、全球最大的LNS文献库建立、LNS患者病程管理数字化工具项目启动、专项LNS科研基金建立……
目前,蚕宝儿LNS罕见病关爱之家还在进行中国Lesch-Nyhan综合征基因型与表型研究以及中国Lesch-Nyhan综合征患者群体遗传咨询相关的工作。正如黄倩女士所言,“自然病史研究实现科研与患者的双向奔赴”,希望“能为蚕宝儿们争取一个有希望的未来”。

王芳 女士
深圳市泡泡家园神经纤维瘤病关爱中心 主任
神经纤维瘤病1型 患者
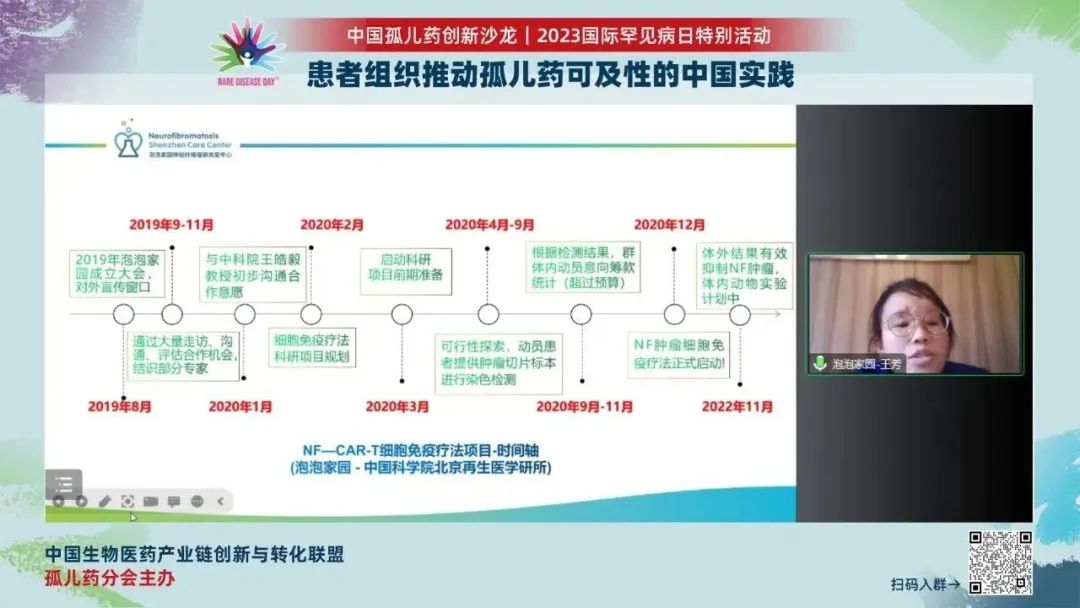
在报告《患者组织推动的早期药物发现》中,王芳女士为我们带来了神经纤维瘤病(NF)由初步想法、项目可行性探索、科研筹资,到项目启动以及阶段性研究成果的分享。
目前,除手术干预外,神经性纤维瘤患者们面临着无药可治的窘境。在针对罕见遗传病的基因编辑、基因疗法逐渐火热的大背景下,“泡泡家园”开始思考“开发针对NF疾病的细胞免疫治疗疗法”。
中科院动物所王皓毅教授实验室专注研究针对恶性肿瘤的免疫疗法,正好关注到NF。与教授多次面对面沟通后,“泡泡家园”进行了科研项目的总体规划,包括实验的目的、方法以及周期等信息。并动员患者提供肿瘤切片标本进行染色检测,评估初步结果,进一步确定项目可行性。
在科研筹资方面,“泡泡家园”的经验也非常值得罕见病患者组织借鉴。2020年9月,在项目评估通过后,“泡泡家园”通过QQ群、微信群等渠道动员NF病友群体,并在短短2个月的时间内累计获得筹款112万元。同年12月,“泡泡家园”正式与中国科学院北京再生医学研所签订NF——CAR-T免疫疗法研究合作协议。
2023年,“泡泡家园”计划筹建NF科委会。王芳女士希望通过科研人员、临床医生等专业力量的加入,能够更加科学有效地推动NF——CAR-T免疫疗法的研究发展,以及NF相关的科研项目。
王菲菲 女士
北京市美儿脊髓性肌萎缩症关爱中心 项目主管
初级社会工作师
随着国内SMA患者规范化诊疗进入全新时期并逐渐完善,美儿SMA关爱中心更清晰地认识到:作为罕见病患者,SMA患者需要全生命周期的照顾、关爱和管理。仅仅依靠药物治疗是远远不够的。
王菲菲女士介绍,美儿SMA关爱中心目前已建立国内最大的SMA患者数据登记库,并配合专家团队开展真实世界患者生活状态研究,包括自然病史、生存状况、生活质量、疾病负担、卫生经济等多方面。除此之外,中心为药物临床试验在中国的落地和开展提供支持,协助试验中心联络、医生沟通等;配合医生筛选适合临床试验的患者家庭,与患者家庭沟通配合医生顺利完成临床试验。
美儿SMA关爱中心协助政协委员、人大代表了解患者情况,学习了解各地现有政策,开展相关主题讲座,并积极关注医保落地,通过服务支持、公众宣传等形式,充分地帮助患者及其家庭。

谭雪松 先生
深圳市安安雷特罕见病研究所 创始人
拥有25年跨领域工作经验的科技管理工作者
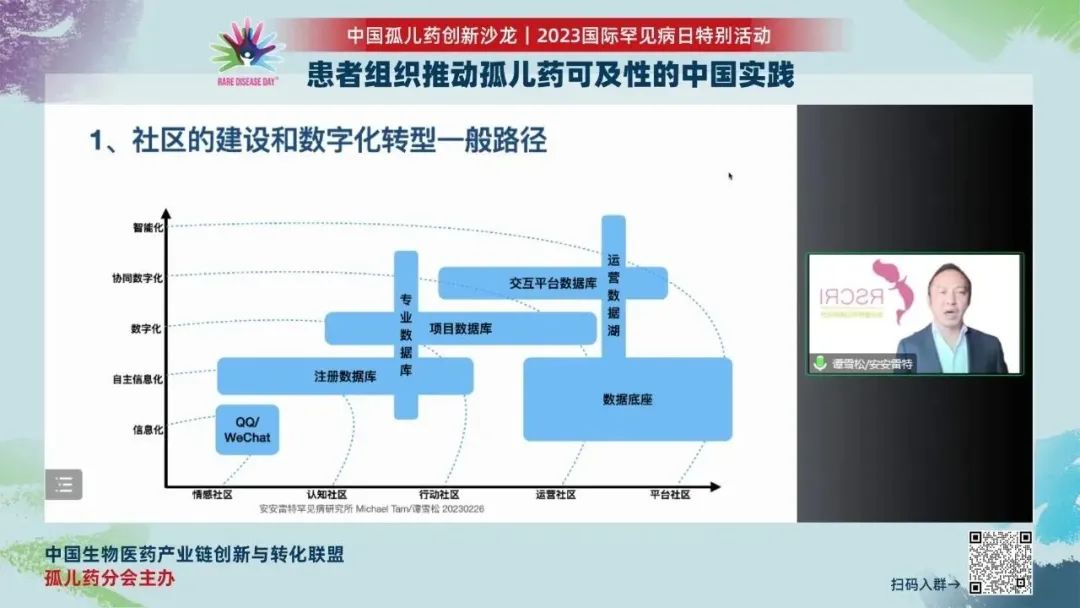
在报告《罕见病患者社区数字化转型进程的实践和思考》中,谭雪松先生介绍,罕见病患者社区在发展过程中会经历情感社区、认知社区、行动社区、运营社区到平台社区的建设转变。与此同时,信息的维度也会发生信息化、自主信息化、数字化、协同数字化、智能化的改变趋势。
谭雪松先生强调,面对商业合作时①有规则,这对患者组织能力的要求也随之增加。他分享了自己总结的患者组织可以尝试开展的5个“1”,以加速患者组织能力的提升:1次成功的主题众筹项目执行,1个共性问题/需求的解决 (诊断,筛查等),1个科研项目立项、上链,1次国际会议露出、带科研项目,1次国内外专家互访会议、更多的科研项目立项和上链,1个药物临床试验开展。②有甄别。利用大数据的基础功能可以持续做有甄别的合作。
数字化、智能化趋势下,患者组织与利益相关方(药企、临床医生、研究者等)的数据关注点并不相同,所以合作的产生需要更多的沟通与共识,从而形成健康的生态协作与数据交互。期待更多基于数据治理的新科技、新路径以及新成果。
研究者发起的临床研究(IIT)
为罕见病患者提供治疗的机会
但风险并存
根据国外的研究报告显示,罕见病药品从开展研发与试验到获批上市,平均周期是6-10年,对罹患进行性疾病的罕见病患者而言,这无疑是消耗生命在等待药品上市。而随着国内罕见病药物研发热度增加,也有很多罕见病患者关注到研究者发起的临床研究(IIT),那临床试验、特别是IIT,是否可以看作是患者接受治疗的捷径?各位参会嘉宾各抒己见。

刘轩飞 先生
亮点连接罕见病关爱之家 创始人
“罕见病万里行”公益活动 发起人
罕见病患者组织网 创始人
肾上腺脑白质营养不良 患者
刘轩飞先生认为,IIT作为一种治疗希望,更需要有力量能够保障研究顺利的进行。比如:第一,前期费用可控且患者可承受。患者可以根据试验的步骤付费,而非一次性支付;第二,以患者为中心,对于临床后治疗药物的剂量等患者保留知情权。
姚颜锁 先生
北京至爱杜氏肌营养不良关爱中心 执行主任
Duchenne肌营养不良 患儿家长
姚颜锁先生则对IIT持谨慎态度。他认为,目前针对DMD的治疗,可使用的药物相对较多。希望国内药企可以发挥中国的患者优势,对国外上市的药物、疗法进行改良。从安全性的角度出发,如果药物已经在在国外接受过验证,那对于患者的风险会更小。
陈建敏 博士
皮质醇增多症联盟 负责人
“希有乐团”成员
库欣综合征 患者
陈建敏博士关心库欣综合征治疗药物的“老药新用”。期待有合适的药物能够降低皮质醇,在安全性与有效性共存的情况下用于皮质醇增多症。希望患者组织可以联合专业研究者,针对某一类药物进行单项试验以加速药物上市的过程。
郑维义 博士
中国孤儿药创新联盟 发起人
苏州诺景生命科技有限公司 董事长
南京师范大学罕见病基因治疗联合研究中心 主任
中国生物医药产业链创新与转化联盟孤儿药分会 主任委员
国家重大人才工程项目 A类专家
郑维义博士非常理解罕见病患者及患者家属迫切性的需求,但IIT研究是非常严肃的事情。国内目前并没有相关的指导原则,行业内亟需出台规范性的文件,以约束IIT科学、规范、健康的可持续发展,从而使患者获益。需要特别指出的是,任何临床试验包括IIT是不应该向受试者收费的。
陈懿玮 博士
遗传学与罕见病科普公益平台“豌豆Sir” 创始人
中欧智慧医疗研究院 特邀研究员
中国生物医药产业链创新与转化联盟孤儿药分会 秘书长
陈懿玮博士则希望更好地保护罕见病患者的权益。无论是药物临床试验还是IIT,药物与疗法的有效性与安全性都是未知数,都是风险与获益并存。而临床试验所面对的诸多监管条例与规范,许多都是漫长的药物研发历史中血的教训。对于罕见病患者而言,IIT提供的在研药物使用机会≠治疗必然有效果和试验的过程没有风险。

 产业资讯
产业资讯
 清科研究
清科研究  2025-08-02
2025-08-02
 30
30

 产业资讯
产业资讯
 空之客
空之客  2025-08-02
2025-08-02
 33
33

 产业资讯
产业资讯
 医药魔方
医药魔方  2025-08-02
2025-08-02
 33
33