 产业资讯
产业资讯
 IQVIA艾昆纬
IQVIA艾昆纬  2023-07-26
2023-07-26
 2730
2730
标准治疗的演变
在美国,肺癌是主要的死亡原因,每年有大约218,500人确诊和142,000例死亡。非小细胞肺癌(NSCLC)占肺癌病例的80%以上,包括鳞癌非鳞癌(腺癌和大细胞癌)和鳞癌(表皮样癌)两种类型。NSCLC的药物疗法分为靶向疗法和免疫疗法。靶向疗法已被推荐给了多数存在驱动基因突变的转移性NSCLC患者;靶向疗法在一线治疗中的缓解率更高、耐受性好,并且这类人群对免疫疗法的应答率可能性较低。
从传统意义上讲,对于缺少“驱动基因突变”的NSCLC患者来说,含铂化疗是一线标准治疗。但是缺乏选择性、耐药性、全身毒性,以及患者生存质量降低,限制了这种疗法的临床潜力。晚期NSCLC治疗方案于2015年开始快速发展,在这一年,PD-1免疫检查点抑制剂纳武利尤单抗(nivolumab)和帕博利珠单抗(pembrolizumab)获批,准许在含铂化疗出现进展后,用于二线治疗。在CheckMate 017试验中,与多西他赛(docetaxel)化疗相比,纳武利尤单抗使鳞状细胞癌患者的1年生存率将近翻倍(42% vs. 24%),显著地改善了总生存期。在针对非鳞NSCLC人群的CheckMate 057试验中,纳武利尤单抗再次展现出优越性,在两种重要的组织学亚型癌症治疗中,均取得了令人瞩目的效益。在二线PD-L1阳性人群中(PD-L1表达程度≥1%),与多西他赛相比,帕博利珠单抗在KEYNOTE-010试验中显著地延长了生存期,并因此获批。以PD-L1为靶点的阿替利珠单抗(atezolizumab),随后根据OAK试验的结果,于2016年获批,加入到二线NSCLC的竞争中。
这些免疫疗法试验的成功,使得免疫疗法快速地扩张到一线场景中。KEYNOTE 024是一项标志性研究,该研究比较了帕博利珠单抗单一疗法与含铂化疗在“患有一线转移性NSCLC、PD-L1表达程度≥50%、没有表皮生长因子受体突变或间变性淋巴瘤激酶重排的患者”治疗效果。在PD-L1表达程度较高(≥50%)的患者身上,免疫疗法显著地改善了无进展生存期和总生存期,推动了免疫疗法进入一线领域,并为开展PD-L1检测提供了例证。
NCCN指南(2023年第3版)建议,帕博利珠单抗单一疗法、或者帕博利珠单抗与化疗、阿替利珠单抗或西米普利单抗(cemiplimab)联合使用,作为用于治疗PD-L1表达程度较高(≥50%)的患者的首选疗法,无论其组织学类型如何。用于此场景的其他免疫疗法包括“纳武利尤单抗(nivolumab)+伊匹木单抗(ipilimumab)”以及“度伐利尤单抗(durvalumab)+替西木单抗(tremelimumab)”。在PD-L1表达程度较高的患者身上,单一免疫疗法对比免疫化疗联合疗法,孰优孰劣仍有争议。目前,治疗方案根据临床判断斟酌决定,因为两种模式均被认为是标准治疗;不过,一些研究提示,联用含铂化疗并未显著地有利于总生存期,并有可能增加毒性,这为采用单一免疫疗法提供了理论依据。
在PD-L1表达程度较低者(1-49%)身上,KEYNOTE 189和KEYNOTE 407试验确认,帕博利珠单抗与化疗联用是用于治疗非鳞癌和鳞癌两种组织学类型癌症的一线主要疗法,与单纯化疗相比,联合疗法的总生存期更优。不过,在PD-L1表达程度较低(1-49%)的患者身上,除非存在联合化疗的禁忌症,否则,帕博利珠单抗单一疗法不是优选的疗法,因为在III期KEYNOTE 042试验中,帕博利珠单抗单一疗法与化疗相比,该亚组人群的总生存期没有统计学意义上显著的改善。NCCN指南(2023年第3版)认为,尽管也可以使用其他免疫疗法,帕博利珠单抗与化疗联用属于“1类推荐”,无论其组织学类型如何或者PD-L1状态如何。
在过去十年时间里,NSCLC可选疗法的范围有了实质性的扩大,治疗策略也转向基于免疫检查点抑制剂的联合疗法。
新兴疗法和未来方向
免疫疗法的成功继续延伸,多种新兴制剂正在研发中,它们可能会完善前线非小细胞肺癌(NSCLC)的标准治疗。一些有前景的新型制剂包括:基于TIGIT的疗法、 抗体偶联药物(ADC)、CTLA-4抑制剂、LAG-3抑制剂等。
TIGIT
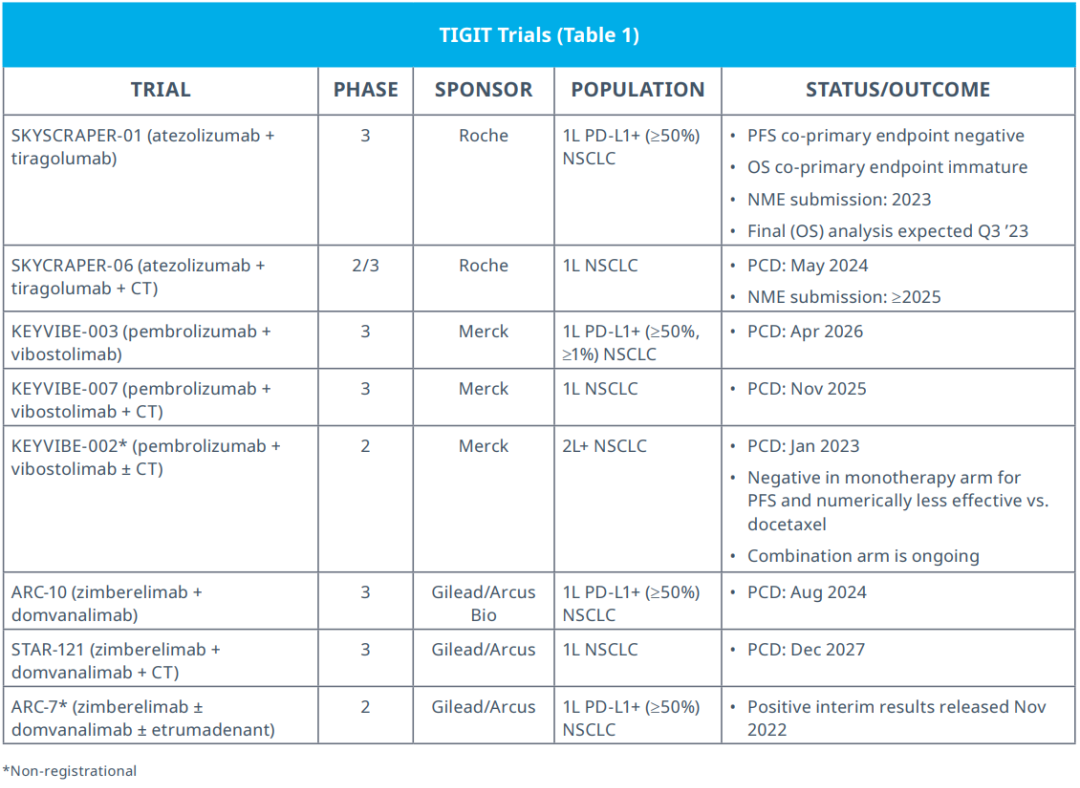
T细胞免疫球蛋白和免疫受体酪氨酸抑制性基序结构域(TIGIT)是在淋巴细胞中表达的抑制性受体,包括细胞毒性T细胞、辅助性T细胞、调节性T细胞和NK细胞。临床前研究表明,PD-(L)1和TIGIT双重阻断可能会在多种癌症的治疗中引发肿瘤排斥反应,特别是对免疫检查点抑制剂有抗药性的肿瘤。多家公司正在多项晚期试验中、在“经过PD-L1选择”(高表达)和“未经PD-L1选择”两种场景中研究这种NSCLC治疗策略(表1)。
ADC
抗体偶联药物(ADC)也正在作为用于非小细胞肺癌(NSCLC)的一线治疗进行研究(表2)。
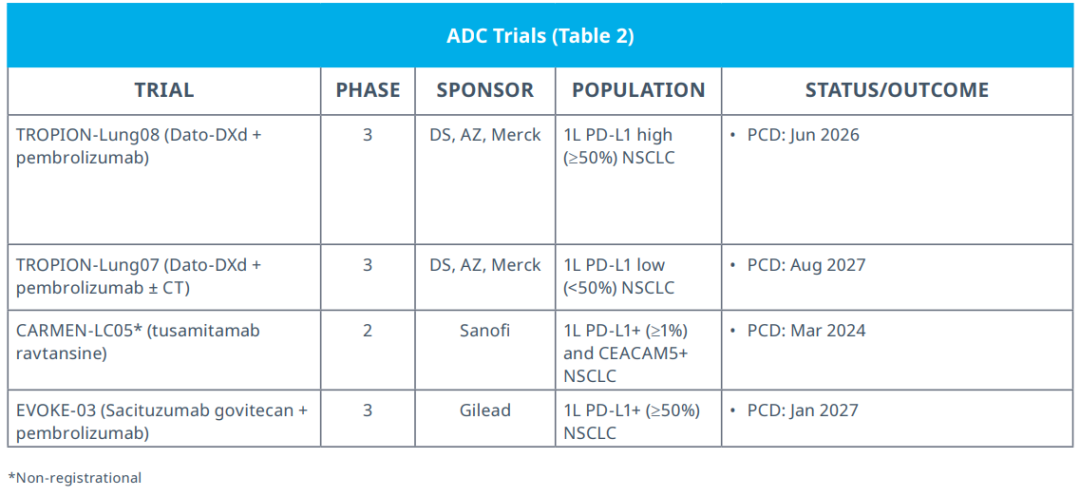
第一三共的“德达博妥单抗-德鲁替康(Dato-DXd)”(DS-1062)正在进行III期TROPION-Lung08试验研究,与帕博利珠单抗联用,治疗一线PD-L1阳性(≥50%)NSCLC。与此类似,III期TROPION-Lung07试验研究了“德达博妥单抗-德鲁替康”,与帕博利珠单抗联用、与或不与化疗联用,治疗一线(PD-L1 < 50%)NSCLC。赛诺菲正在II期CARMEN-LC05试验中研究“特赛妥单抗-雷星”(tusamitamab ravtansine,SAR408701,一种CEACAM5和DM4抗体偶联药物),与帕博利珠单抗联用、与或不与化疗联用,治疗“经过生物标志物选择”(PD-L1≥1%和CEACAM5阳性)的一线NSCLC。吉利德也正在进行III期EVOKE-03试验;该试验研究了“沙西妥珠单抗-戈维替康”(sacituzumab govitecan)与帕博利珠单抗联用,治疗一线PD-L1阳性(≥50%)NSCLC。
CTLA-4
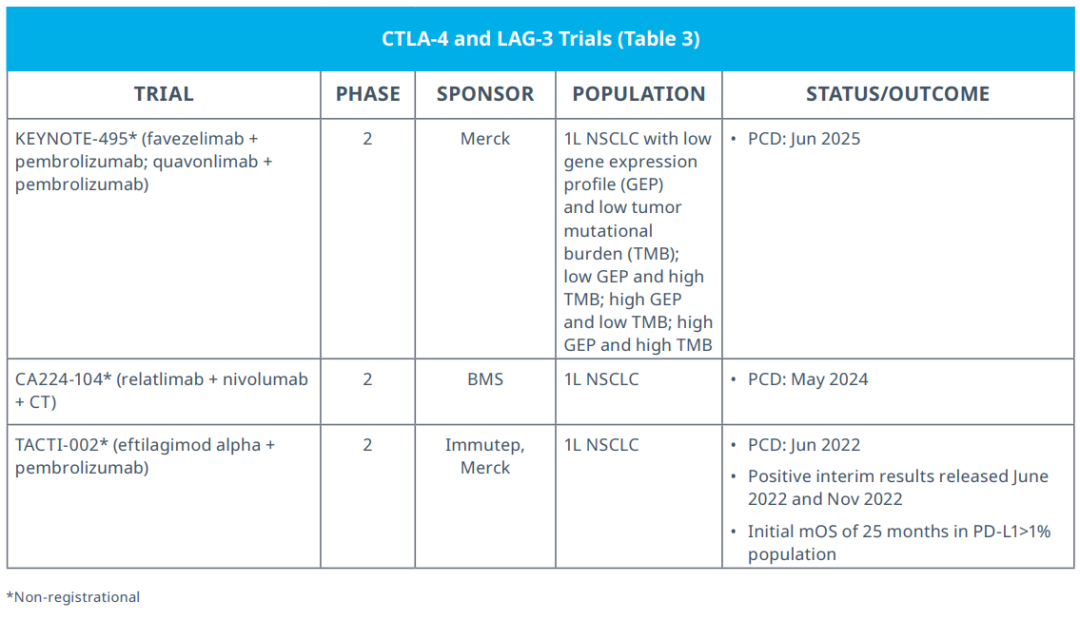
除了伊匹木单抗和替西木单抗以外,正在进行中的试验继续评估了新型CTLA-4抑制剂与PD-(L)1抑制剂联合疗法。II期KEYNOTE-495试验正在研究“由生物标志物导向的”(基因表达态势和肿瘤突变负荷)基于帕博利珠单抗的联合疗法,用于治疗一线NSCLC;库瓦芬利单抗(quavonlimab)与帕博利珠单抗联用是试验方案之一(表3)。在一项初步I期研究中,库瓦芬利单抗与帕博利珠单抗联用的客观反应率为35.1%,中位无进展生存期为6.1个月,中位总生存期为16.5个月,表明其疗效近似于CheckMate 012和CheckMate 227试验中纳武利尤单抗与伊匹木单抗联用的疗效。
LAG-3
LAG-3是另一项受到关注的用于共刺激检查点靶向生物标志物。在NSCLC治疗中,LAG-3会引起预后不良,因为LAG-3呈阳性或者LAG-3与PD-L1同时呈阳性会造成“提早术后复发”。如果LAG-3表达程度较高,还有可能提高肿瘤浸润淋巴细胞的PD-L1表达程度,这进一步佐证了联合治疗策略的合理性。
抗LAG-3抗体玛维泽利单抗(favezelimab)是KEYNOTE 495试验中与帕博利珠单抗联用的制剂之一。BMS的一项II期试验正在研究瑞拉利单抗(Relatlimab),与纳武利尤单抗和化疗联用,对比单纯采用“纳武利尤单抗+化疗”,治晚期或复发一线。尽管多数新型LAG-3靶向药物为单克隆抗体,但Immutep的依替拉莫阿尔法(eftilagimod alpha)却是一种可溶的LAG-3融合蛋白,它能结合到II类主要组织相容性复合体上,并能介导抗原呈递细胞和CD8 T细胞活化。II期TACTI-002试验评估了在一组“PD-L1未筛选”的患者中,依替拉莫阿尔法与帕博利珠单抗联用,治疗一线NSCLC;在2022年美国临床肿瘤学会年会上,提交了此试验的数据。据报道,客观缓解率为37.3%,疾病控制率为73.3%,中位无进展生存期为6.9个月:在所有PD-L1亚组中均观察到缓解。在2022年癌症免疫治疗学会年会上,根据新提交的结果,客观缓解率升高到40.4%,中位持续缓解时间的中期结果为21.6个月;除了这些数据以外,Immutep近期还宣布,PD-L1表达程度>1%的患者的中位总生存期初步结果为25个月。FDA表示支持其开展注册性试验,评估依替拉莫阿尔法与抗PD-1疗法的联用情况;Immutep已制定了计划,正在推进TACTI-004注册性试验,该试验重点研究PD-L1 > 1%的人群。
其他策略
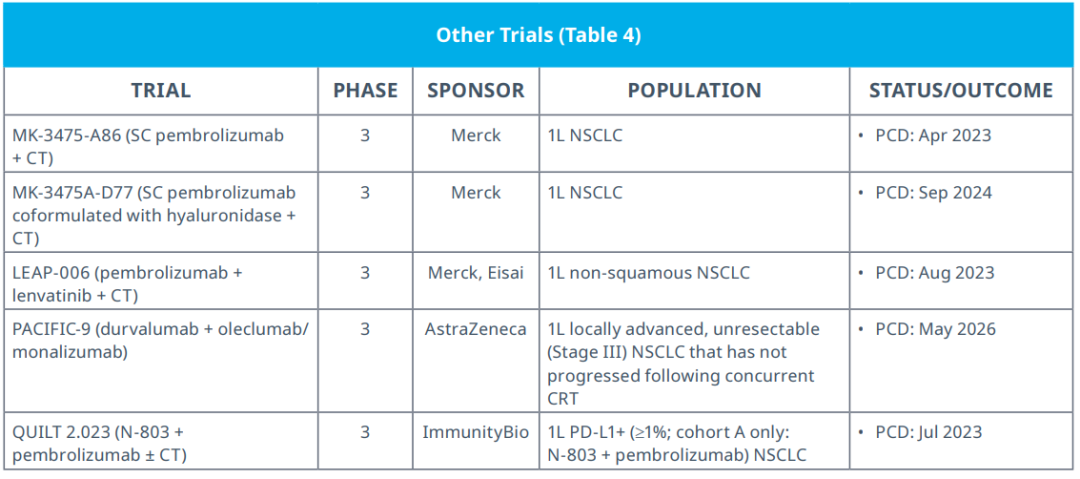
帕博利珠单抗和其他检查点抑制剂目前都通过静脉注射给药;然而,皮下制剂可以减少用在医疗健康系统上面的花销,提升药物可及性,为患者和医务人员双方提供更大的便利。从商业策略的角度来看,Keytruda的美国专利权将于2028年到期,这进一步增加了默沙东开发皮下制剂的动力,以延长专利期。III期MK-3475-A86试验正在评估帕博利珠单抗皮下给药与化疗联用,对比静脉给药与化疗联用,治疗鳞状和非鳞状一线NSCLC。同时,默沙东正在研发帕博利珠单抗与透明质酸酶的皮下复方制剂,该制剂正在近期启动的III期MK-3475A-D77试验中接受测试。
多靶点酪氨酸激酶抑制剂联合治疗策略也正在探索之中,此类抑制剂具有抑制血管内皮生长因子等生血管激酶的活性,与免疫治疗药物联用。通过血管内皮生长因子信号传递,可以调节肿瘤微环境,并调节PD-1等抑制性检查点分子的表达,这为仑伐替尼(lenvatinib)与帕博利珠单抗的联合疗法提供了依据。III期LEAP-006试验正在评估帕博利珠单抗和仑伐替尼与化疗联用,治疗一线非鳞状NSCLC。13位患者的初步试验结果显示,客观缓解率为69.2%,疾病控制率为92.3%,但54%的患者出现了3级以上的不良事件,这表明毒性担忧可能会限制这种“免疫疗法+酪氨酸激酶抑制剂”策略的使用。其他对抗免疫抑制性环境的策略包括以CD73和NKG2A为靶点;同时,PACIFIC-9试验正在评估,在同步化疗/放疗之后,度伐利尤单抗与奥来鲁单抗(Oleclumab)或莫那利珠单抗(monalizumab)联用,治疗局部晚期NSCLC。
ImmunityBio的N-803是一种新型IL-15超拮抗剂复合物,由一种IL-15突变体(IL-15N72D)和一种IL-15受体(α/IgG1 Fc融合蛋白)融合而成。N-803可以皮下注射,能促进自然杀伤细胞和CD8+ T细胞的活化,而非调节性T细胞的活化。N-803与免疫检查点抑制剂联用具有协同增效潜力,因为N-803能引发免疫应答,而免疫检查点抑制剂能阻止免疫抑制。此外,研究显示,N-803能在体内增强免疫细胞上的PD-L1表达。III期QUILT 2.023试验正在研究N-803与帕博利珠单抗联用、与或不与化疗联用,治疗一线III/IV期NSCLC。
结论
新型免疫疗法、生物标志物和联合治疗策略可能会改善非小细胞肺癌患者的预后;随着新型疗法的出现,治疗竞争格局会继续演变;然而有上述文中提到的进展,但是仍有大量需求未得到满足。未来的研究可能会重点关注新型作用机制、限制毒性、以及发挥个体化治疗的潜力。尽管NSCLC市场空间拥挤,但药企仍在继续大力投资,使其资产差异化,最终改善患者预后。

 产业资讯
产业资讯
 UmabsDB
UmabsDB  2025-06-23
2025-06-23
 47
47

 产业资讯
产业资讯
 支点财经
支点财经  2025-06-23
2025-06-23
 48
48

 产业资讯
产业资讯
 药视声
药视声  2025-06-23
2025-06-23
 49
49