 产业资讯
产业资讯
 E药经理人
E药经理人  2023-08-04
2023-08-04
 2991
2991
今年,无论是头部创新药企,还是小而美的Biotech,都在尽力对外释放积极信号。
摆在台面上的是,他们不约而同地宣告上半年“首次盈利”了,原来似乎遥不可及的目标如今一个接一个地达成。然而体量太大的头部公司,要想实现盈利更难,他们能做到的是给大家强劲增长的预期,最好能在规模增长的同时缩窄亏损。
藏在水面下的又是什么?在半年报发布之际,E药经理人根据收入规模、细分赛道、技术方向等维度筛选了6家港股创新药企的财报,通过分析他们上半年在商业化、BD合作、研发方向的策略和表现,来反映整个创新药企的现状。
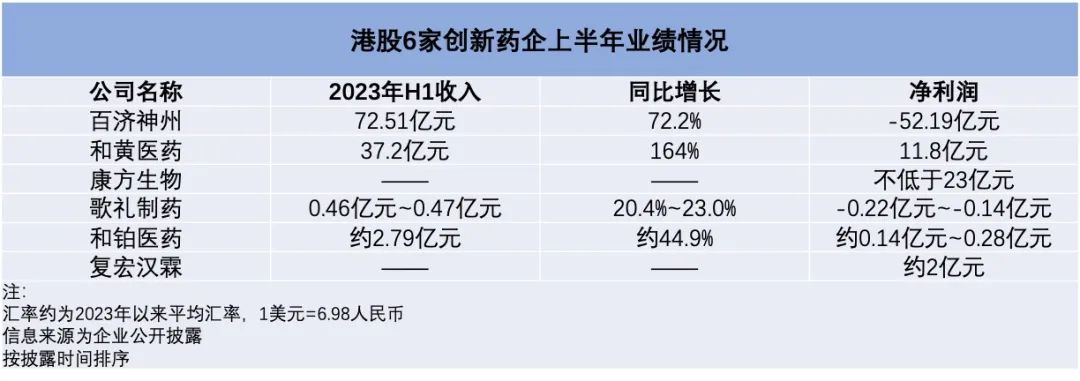
这6家公司,从规模上既覆盖了头部Biopharma,如百济神州等,也包含了小而美的Biotech,如和铂医药等;从赛道上囊括了小分子、大分子、双抗的龙头,如和黄医药、康方生物等;从适应证领域上,除肿瘤外,还有抗感染领域的歌礼制药;从模式上,除创新药企外,还包含了兼顾生物类似药的复宏汉霖。
商业化:“首次盈利”的信号
一直以来,行业对于未有盈利上市的Biotech都有一个终极拷问——“何时能实现盈利”?寒冬下,更甚。因为Biotech的上市,改变了行业对上市公司的估值逻辑,“很难看懂”成为一道渴望被打破的隐形门槛。
当复宏汉霖宣告首次盈利时,人们发现他是港股第一家依靠产品销售实现盈利的创新药企。答案破解,行业中似乎有了可以参照的对象。可大家没有想到的是,接下来,和铂医药、和黄医药、康方生物纷纷加入盈利大军。尽管后来者们,都是靠产品/技术授权盈利,但这同样可期,因为长期以来美国Biotech都以此为经营模式,并形成了良好的行业生态。
复盘来看,4家Biotech实现正面盈利的共性原因离不开“开源节流”之道。以复宏汉霖为例,上半年预计实现利润约人民币2亿元,原因有二,一端是核心产品销售收入持续增长,另一端是精细化管理下的成本控制。
核心产品的商业化成功与其策略和执行紧密相关。复宏汉霖在商业化上采用了“自主+合作”的模式——实体瘤产品由自己的商业化团队推广,把不同的产品交给不同的合作公司,以发挥产品商业化上的潜在协同。成立以来,复宏汉霖共上市了5款产品,汉曲优(曲妥珠单抗)、汉斯状(斯鲁利单抗)、汉贝泰(贝伐珠单抗)自主商业化,血液瘤产品汉利康(利妥昔单抗)交给了江苏复星,汉达远(阿达木单抗)则由复星医药旗下万邦医药进行销售。
执行同样在线。据该公司首席商务官余诚此前透露,在汉曲优的商业化过程中,复宏汉霖只花了大约5个月,就把全国的医保编码、各省的医保进行了落地。
类似的模式可见于康方生物。康方生物共上市了两款产品,其中PD-1派安普利单抗交给了中国生物制药,而双特异性抗体(双抗)新药开坦尼(PD-1/CTLA-4双抗,卡度尼利)自主商业化。前者因为绑定了正大天晴的销售网络,该产品被分析师认为是最具市场潜力的PD-1产品,事实上,在PD-1激烈的市场竞争中,该产品上市第一年(2022年)销售就达到了5.58亿元。今年上半年,康方生物也透露该产品获得了持续的增长。
康方生物自主商业化的卡度尼利也不逊色,仅凭借晚期宫颈癌一个适应证,上市6个月便大卖5.46亿元。今年上半年,康方生物在预告中透露,凭借突出的临床价值,卡度尼利覆盖的患者数量持续增加,销售收入不断提高。
当然康方生物本次盈利主要受益于与美国Summit Therapeutics的授权合作,这一许可费收入金额约为29亿元,而康方上半年预计实现利润约23亿元,产品销售收入大体可推测会是一个亮眼的数字。
在痛失销售占比约八成的核心商业化产品后,歌礼制药深陷亏损扩大泥潭。然而失之东隅收之桑榆。今年上半年,歌礼抓住新冠疫情最后的“尾巴”,在新冠口服药利托那韦上发力,此前通过给辉瑞中国、先声药业及一家未披露的中国制药公司商业化供应利托那韦片,其在去年实现了约483万元的收入。今年歌礼预计,这一供应将对2023年总收入作出重大贡献。不过,对歌礼来说,产品的缺失仍未改变其商业化现状。
尽管百济神州没有实现盈利,但他强劲的增长给行业灌注了信心,甚至给出一种高瓴资本又投出个药界“京东”的既视感。上半年,得益于核心产品的销售增长,百济神州产品收入实现66.96亿元,同比增长82.2%,已接近去年全年八成。同时,上半年亏损收窄。
在一众创新药企仍困于其创新药商业化的难关时,百济神州通过变革率先走出了一条独立增长的曲线。不论是国内的商业化还是海外的商业化,百济神州似乎都掌握了要义般,使得其核心产品步入了稳健的高增长轨道。上半年,泽布替尼(百悦泽)实现全球销售额36.12亿元,其中在美销售额超过25亿元,较上年同期增长超过一倍。如以此增速发展,泽布替尼将成为国内首个10亿美元“重磅炸弹”。
替雷利珠单抗(百泽安)更是在“PD-1四小龙”中一枝独秀。今年上半年,该产品在国内市场销量再提速,同比增长42.5%,达到了18.36亿元。销售一路增长背后,是百济神州强大的临床和市场准入。截至上半年,替雷利珠单抗获NMPA批准11项适应证,其中9项已获批适应证已被纳入国家医保目录,是目前国内获批适应证和纳入医保适应证数量最多的PD-1产品。同时,根源还在于产品的临床疗效。值得关注的是,国内包括康方生物、齐鲁制药在内的多家药企已经将替雷利珠单抗作为头对头三期临床的参照药物。
百济神州的商业化也获得了传统制药公司的认可。7月4日,百济神州与绿叶制药宣布,就后者的注射用戈舍瑞林微球(中文商标:百拓维)达成商业化合作,百济神州将获得该产品在中国大陆地区研究、开发及商业化的独家权利,而绿叶作为该产品上市许可持有人(MAH),基于百济预估的需求供应和生产该产品。该产品为全球首个且唯一获批上市的戈舍瑞林长效微球制剂,用于需要雄激素去势治疗的前列腺癌患者。
BD的学问:康方、和铂借此盈利
在今年的一场行业会议上,一位国内创新药企负责人透露公司将在2025年依靠商业化产品实现盈利。他随后解释道,盈利一方面来自于国内产品商业化,一方面来自海外销售分成。
不可否认,BD收入成为当下国内创新药公司的重要营收来源。目前披露业绩的几家港股创新药上市公司中,BD收入就占据了他们上半年营收的一大部分。比如发布正面盈利预告的和铂医药和康方生物,前者预计上半年溢利介乎200万美元至400万美元,后者预计实现利润不低于人民币23亿元。
其中,HBM7008及HBM9161两款创新药产品的授权合作是和铂医药收入增加的主要原因之一;康方生物的盈利原因之一则是PD-1/ VEGF双抗依沃西授权给Summit后在今年一季度获得了5亿美元的首付款。
另外,和黄医药的H1财报中也披露,总收入增长164%至5.32亿美元,其中2.59亿美元来自于与武田制药合作的首付款。
光从业绩数据上来看,其实创新药企在一段时间内获得一笔授权合作收入,然后在披露业绩之时因此达到盈利的事件在国内市场来讲并不稀奇。荣昌生物也在2021年因将ADC药物维迪西妥单抗授权给Seagen获得2亿美元首付款并在当年实现了盈利。
但不可忽视的是,国内创新药公司License-out的产品被“退货”,合作“分手”在今年以来频频发生,引发了业内对于BD合作可持续性的讨论。5月,EQRx退回基石药业PD-L1单抗;7月,艾伯维返还SHP2抑制剂权益给加科思;同月,百济神州也发布公告称与诺华终止TIGIT靶点合作。
因此,BD合作如何持续,或者像上述创新药企负责人所设想的为公司业绩带来补充成为他们需要探索的课题。其实观察今年上半年因BD交易获得收入或者实现盈利的几家公司,他们的合作方案或许是答案之一。
例如康方生物就给依沃西找到了合适BD合作伙伴,既保留了对产品的开发“话语权”,又可以实现依沃西在海外市场的价值最大化。
康方生物在去年12月与Summit达成依沃西在美国、加拿大、欧洲和日本的开发和商业化授权合作,包括5亿美元的首付款和最高50亿美元的里程碑付款,未来还将收到销售净额的低双位数比例提成作为特许权使用费。
值得注意的是,依沃西当时是全球进展最快的PD-1/VEGF双抗,康方生物正在进行依沃西单药对比K药单药一线治疗PD-L1表达阳性的非小细胞肺癌的三期临床研究,以及依沃西联合化疗对比化疗在EGFR-TKI耐药的EGFR突变的晚期非鳞状NSCLC的三期临床研究,并取得了一定的积极数据。而合作方Summit作为海外的生物技术公司,通过合作依沃西将成为其核心产品之一,今年6月,Summit就注册了一项联合化疗一线治疗转移性鳞状非小细胞肺癌的三期研究。
和黄医药也是如此,为在国内已上市产品呋喹替尼找到了武田作为BD合作方,授权后者在除中国内地、香港和澳门以外的全球范围内的开发、商业化和生产。在今年5月,呋喹替尼用于治疗经治转移性结直肠癌成人患者的新药上市申请获得了FDA的受理,拟定处方药用户付费法案(PDUFA)目标审评日期为2023年11月30日。
此外,和黄医药还与礼来在国内市场合作销售呋喹替尼,并将赛沃替尼的商业化权益授权给了AZ,上半年两款产品分别卖出了5630万美元和2200万美元。
其实总结来看,BD合作的条款设置、BD产品的阶段选择、BD合作方的选择等都是学问,创新药企谨慎选择才能实现产品价值的最大化。
研发:没有静悄悄
毫无疑问,只有不断创新,不断有新产品问世,才能加强一家药企未来的确定性。
展开这几家药企的半年报,结合官网披露信息,各大药企都在能力范围内不遗余力展开研发,聚焦重点研发管线。一个规律是,大家几乎均先围绕着既定优势产品扩大适应证范围,从而巩固所在疾病领域的优势地位,并试图更差异化;同时再将羽翼不断扩大,触角踏入一些新领域进行布局。
如百济神州一向在血液肿瘤领域的布局中具有突出优势,泽布替尼正是其最具代表性的自研产品之一。百济神州自然不会放过这块“肥肉”,仍在持续开发潜在“同类最佳”sonrotoclax(BCL2抑制剂)和BTK CDAC作为泽布替尼的补充,以进一步扩展至更多的恶性血液疾病领域,从而欲实现“高筑墙”。
这番押注,百济神州或也经过了深思熟虑,欲凭借多款同类最佳潜力药物,成为全球血液学市场强有力的竞争者,从而实现全球放量。目前,百济神州在研管线涵盖23个开发项目和超过60个临床前项目,广泛覆盖血液瘤、实体瘤领域各高发瘤种。此外,该公司还计划在未来18个月,推动超过15款新分子进入临床阶段。
在前不久举行的投资者研发活动日上,百济神州还透露了其它研发产品,如另一款产品BTK CDAC也显示出治疗潜力,I期试验中200mg单药治疗复发难治CLL患者可达89%缓解率。除了血液瘤、实体瘤两大优势领域,可以很明显看到,百济神州也在拓宽自身边界,布局前沿疗法。
康方生物同样如此,选择持续在优势领域双抗展开布局,推进以其为基石的联合疗法研究。不过走到现今,康方已更有实力去关注更早期的靶点发现了。当前,凭借独有的以端对端全方位药物开发平台(ACE Platform)和双特异性抗体开发技术(Tetrabody)为核心的一体化研发创新体系,康方生物已经拥有30个以上用于治疗肿瘤、自身免疫、炎症、代谢疾病等重大疾病的创新候选药物。
每一款产品都要历经多年积累铺垫,临床研发进度则直接决定着药企的未来生存空间,“研发最创新的产品”或更能带来临床和商业价值的共存。后续管线蓄力带来了“逆天改命”的机会也未可知。
2022年颇受挑战的和铂医药和歌礼经过了一段时间的沉淀后,也开始拥有新的“盘算”。在2022年连砍进度靠前的主要管线后,虽然凭借部分业务授权及业务扩展重新站起来了,但而今和铂医药研发管线相对比较早期,如全球首创靶向B7H7/HHLA2抗体HBM1020 I期临床试验在美国完成首例患者给药。
歌礼制药同样经过了研发管线的转向。而今寄予厚望的产品则是是从康宁杰瑞引进的PD-L1抑制剂恩沃利单抗。除了乙肝市场外,歌礼制药还有多款NASH(非酒精性脂肪性肝炎)适应证的自研产品正在积极推进中,如Sagimet Biosciences合作的ASC40用于治疗NASH和胶质母细胞瘤。
同样如此,歌礼除了丙肝药,进展最快的管线仍然在Ⅱ期,会否失去先发优势这一众药企的“通忧”。但从自主研发的角度来看,歌礼THR-β(甲状腺激素受体β)激动剂ASC41治疗NASH已进入II期临床阶段,是国内进展最快的THR-β激动剂;FXR(非甾类法尼醇X受体)激动剂ASC42已在中美两国开展NASH适应证临床试验,有成为同类最佳的潜力。
实际上,同样在实体瘤和血液瘤治疗领域广泛布局的和黄医药已于2022年底在管线产品优先顺序上经过了一轮调整,这个战略已初见成效。目前已有13款产品进入临床阶段,其中3款抗肿瘤创新药已经在国内上市,分别是呋喹替尼(爱优特)、索凡替尼(苏泰达)和赛沃替尼(沃瑞沙);血液瘤及自免疾病药物安迪利塞和索乐匹尼布分别有BIC和FIC潜力,正在开展注册临床,有望在2023年提交上市申请。
虽风险常在,目前仍难以判断未来研发全命运,尚需时间验证,但众药企纷纷各自发力研发,撒网捕鱼便是机会所在之处。
 产业资讯
产业资讯
 智药局
智药局  2025-12-15
2025-12-15
 24
24

 产业资讯
产业资讯
 Medaverse
Medaverse  2025-12-15
2025-12-15
 26
26

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2025-12-15
2025-12-15
 24
24