 产业资讯
产业资讯
 医药时间
医药时间  2023-08-22
2023-08-22
 2609
2609
2023年医保目录调整有了新进展。
近日,国家医保局发布《关于公示2023年国家基本医疗保险、工伤保险和生育保险药品目录调整通过初步形式审查的药品及相关信息的公告》。
国家医保局组织力量对2023年医保药品目录调整的药品申报资料进行了初步形式审查。2023年7月1日9时至2023年7月14日17时,企业申报信息629份,涉及药品(通用名,下同)570个。经审核,390个药品通过初步形式审查(226 个为医保目录外产品)。与2022年相比,申报药品数量有一定增加。公告称,通过形式审查不等于纳入国家医保药品目录,后续还需要按程序开展专家评审、谈判竞价等环节。
值得注意的是,今年公告公布的药品名单包括此前备受关注的百万一针的“抗癌神药”CAR-T疗法阿基仑赛注射液和瑞基奥仑赛注射液,以及GLP-1类“减肥神药”司美格鲁肽注射液和利拉鲁肽。其中,司美格鲁肽目前在国内仅获批用于糖尿病治疗。
两款CAR-T产品再进初审名单
因为“百万一针”“抗癌神药”的光环,自2021年6月首款CAR-T疗法阿基仑赛注射液在国内获批,此类产品是否能通过医保谈判降价并进入医保目录,就备受关注。
阿基仑赛注射液,是复星凯特公司从美国Kite Pharma引进Yescarta技术,并获授权在中国进行本地化生产的靶向CD19 CAR-T细胞治疗药品。用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者。今年6月新增用于治疗一线免疫化疗无效或在一线免疫化疗后12个月内复发的成人大B细胞淋巴瘤(r/r LBCL)的适应症。
根据复星医药2022年财报,截至2023年1月末,阿基仑赛注射液已治疗近300位复发或难治性大B细胞淋巴瘤患者。按照其120万元/针的定价来估算,该疗法自上市至今的1年半时间内产生的销售收入约为3.6亿元。
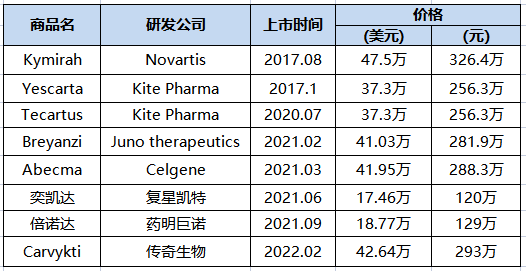
瑞基奥仑赛注射液方面,该产品于2021年9月获批用于治疗经过二线或以上系统性治疗后成人患者的 r/r 大 B 细胞淋巴瘤 (LBCL)定价129万元/针。2022年10 月,该产品用于治疗复发或难治性滤泡淋巴瘤(r/r FL)患者的适应症获得批准,成为中国首个获得FL适应症的细胞免疫治疗产品。
此外,药明巨诺还在拓展瑞基奥仑赛注射液用于其他适应症的治疗:pALL(小儿急性淋巴细胞白血病)、二线LBCL(大 B 细胞淋巴瘤)、一线LBCL IIT临床试验、三线治疗MCL(套细胞淋巴瘤)、系统性红斑狼疮等。
根据药明巨诺2022年财报,其全年1.46亿元营收中绝大部分来自其CAR-T产品瑞基奥仑赛注射液,该药2022年一共开具165张处方,完成141例患者的回输。
阿基仑赛注射液和瑞基奥仑赛注射液曾分别于2021年和2022年进入初审名单,但最终未纳入医保。业内普遍认为,该类产品价格过高不满足谈判的条件。今年2款CAR-T疗法再次进入初审名单,结果拭目以待。
此外,国内第三款获批的CAR-T疗法——今年6月获批上市的信达生物与驯鹿生物的伊基奥仑赛注射液,并未出现在此次的初审名单中。
6月30日晚间 ,国家药监局(NMPA)官网公示,这款靶向BCMA的CAR-T产品伊基奥仑赛注射液已获批上市, 用于治疗复发或难治性多发性骨髓瘤 (MM) 成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。
按照医保目录调整规则,2018年1月1日至2023年6月30日(含)期间获批的药品均可以申报。上述伊基奥仑赛注射液属于踩线获批,理论上拥有了申报资格。有业内人士指出,要么企业主动放弃了申报机会,要么是获批太赶,企业来不及准备申报素材。
两款“减肥神药”进初审名单
2023年以来,CLP-1类药物因为减重效果大火,甚至被部分人奉为“减肥神药”,此次初审名单中就有 2 款“减肥神药”——司美格鲁肽和利拉鲁肽。
司美格鲁肽是跨国药企诺和诺德旗下重磅产品,早在2014年就在美国获批减重适应证,但在我国,该药在2021年4月仅获批用于2型糖尿病的治疗。6月3日,国家药监局药审中心(CDE)官网显示,司美格鲁肽注射液的新适应证上市申请获得受理。业内普遍认为,此次适应证上市申请大概率与减重有关。
诺和诺德2023年H1财报显示,其皮下注射制剂Ozempic(用于降糖)实现营收达到417.41亿丹麦克朗,同比增长58%;口服片剂Rybelsus(用于降糖)销售额达83.44亿丹麦克朗,同比增长97%,减重产品Wegovy销售额则达120.81亿丹麦克朗,同比增长367%。综合以上产品营收,今年上半年司美格鲁肽的系列产品为诺和诺德合计贡献了621.66亿丹麦克郎的营收。业内推测,以现有的增长攀升趋势,司美格鲁肽有望2023年全年销售突破200亿美元。
利拉鲁肽方面,其原研也是诺和诺德,其糖尿病适应证于2011年在中国获批,但减肥适应证尚未获批。诺和诺德的利拉鲁肽于2017年首次被纳入医保,之后成功续约国家医保目录2019年版、2020年版、2021年版、2022年版。
另一款利拉鲁肽来自华东医药,商品名:利鲁平,是区别于原研药的生物类似药。今年3月,该药获批上市用于治疗成人2型糖尿病,其也成为首款获批上市的国产利拉鲁肽注射液。今年7月4日,利鲁平的肥胖或超重适应症的上市许可申请获得批准。据悉,目前利鲁平已正式实现商业化上市销售,并在全国各省积极开展挂网和进院的工作。
事实上,国内还有一款用于减重的GLP-1针剂产品。今年7月27日,仁会生物的贝那鲁肽注射液的减重适应症获批,成为国内首款获批减重适应症的原创新药。不过该药的获批时间较晚,不满足今年的申报条件,因此未出现在此次的初审名单中。值得一提的是,贝那鲁肽的半衰期仅为11分钟,每日需要给药三次,而利拉鲁肽一天一次,司美格鲁肽一周一次。使用频率或影响患者的依从性,也会在一定程度上影响最终产品的市场认可度。
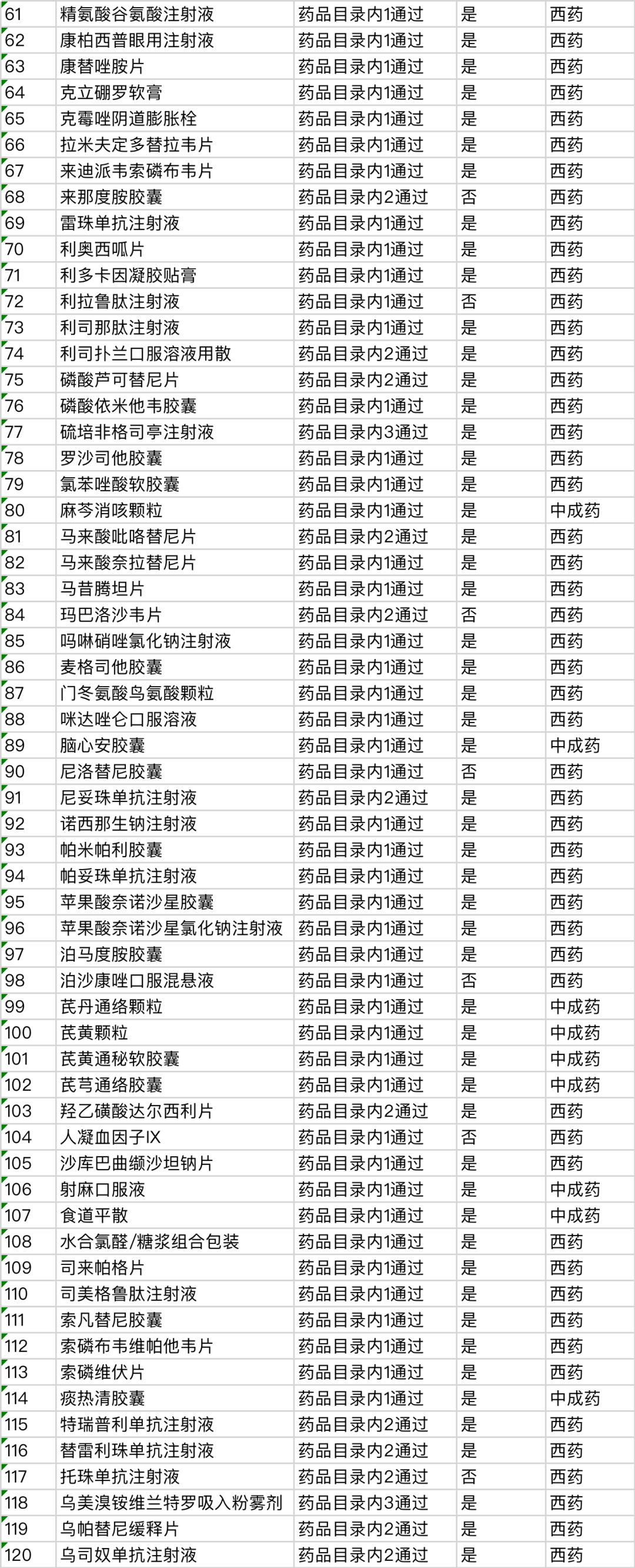
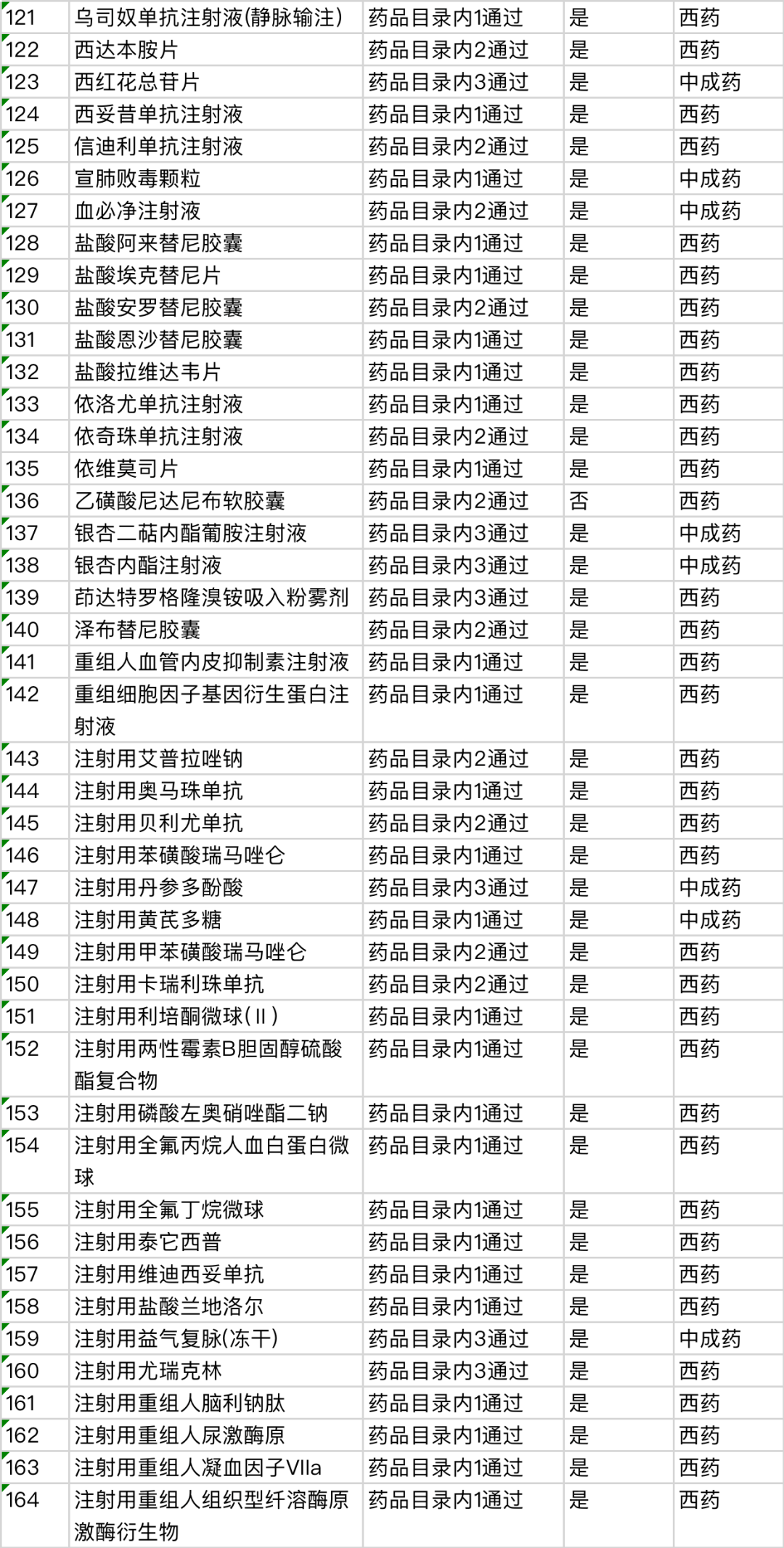
附:《2023年国家基本医疗保险、工伤保险和生育保险药品目录调整通过初步形式审查的申报药品名单》
一、目录外西药和中成药
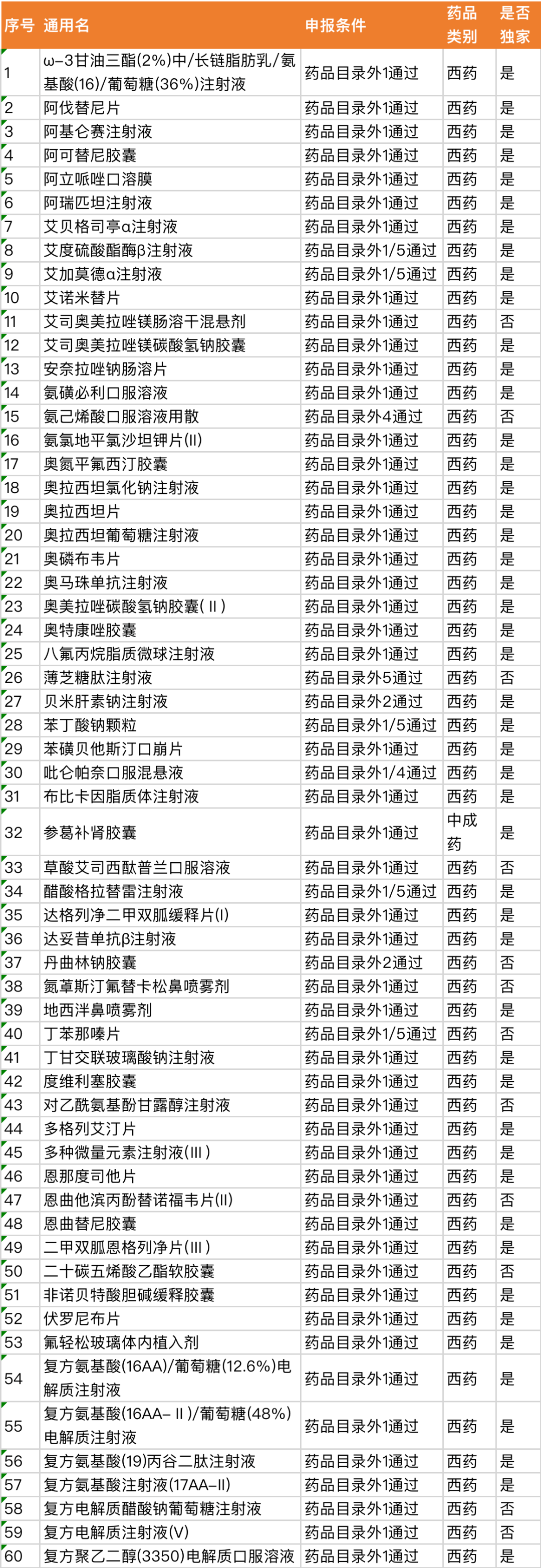

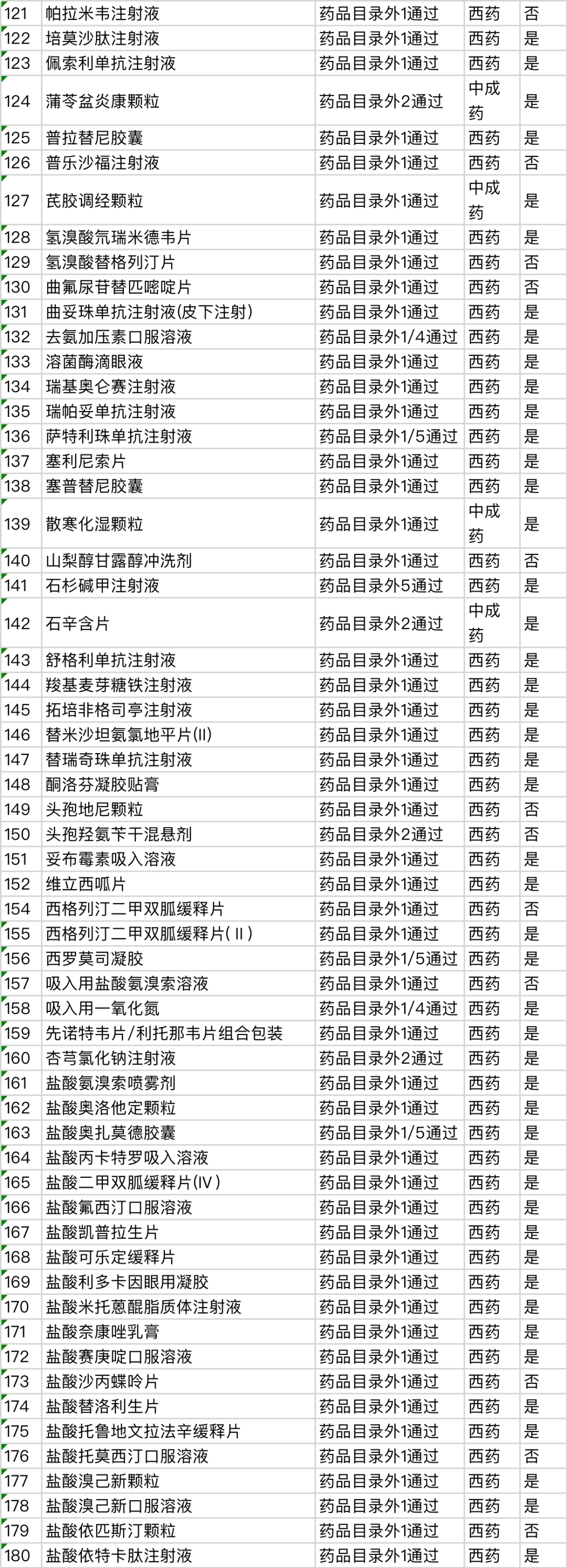

二、目录内西药和中成药


 产业资讯
产业资讯
 新湾novaBAY
新湾novaBAY  2025-06-30
2025-06-30
 130
130

 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2025-06-30
2025-06-30
 128
128
 产业资讯
产业资讯
 Medaverse
Medaverse  2025-06-30
2025-06-30
 90
90