 产业资讯
产业资讯
 医麦客
医麦客  2023-10-27
2023-10-27
 5028
5028
2023年10月26日/医麦客新闻 eMedClub News/--CGT领域虽然倍受追捧,但尚还处于早期发展阶段,药物生产成本更高,需要更灵活的产能,这就为CDMO行业带来了新的机遇和挑战。CRB报告显示,77%的CGT企业与CDMO公司有合作,仅有23%的企业完全自主制造。

▲ 全球基因治疗CDMO市场规模预测,图源:松禾资本
全球基因治疗CDMO行业处于快速发展阶段,据L.E.K统计,有超过20家制药企业及CDMO公司将在2020-2023年间建成工厂投产使用以满足CGT市场的高速发展。这些现象也从侧面验证了市场对CGT CDMO 的巨大需求。从地区来看,目前欧美CGT CDMO占据全球主要市场,头部三家企业占据了约70%的市场份额。但由于人力成本、环保压力、产能配置等原因,全球产能持续向中国等兼顾质量与效益的地区转移。同时,随着国内审评形式越来越与国际接轨、国内新药越来越多进行海内外同步申报、海外新药项目在研发早期阶段进入国内的数量增多,CDMO国际化服务需求日益增长。随着越来越多的基因治疗候选药物步入关键性临床阶段,终端市场的不断扩容,优秀的CGT CDMO 企业有望成为推动药物研发与商业化的重要驱动力,为行业实现降本增效提供可靠保障。
CDMO,缺口就是风口
虽然CGT CDMO一片欣欣向荣的景象,但也不能忽略医药“寒冬”的大背景,CGT最大的痛点便是成本控制,这既是促进CGT CDMO行业发展的根本驱动力,也是CDMO企业需要首先克服的技术与工艺难题。产能便是行业公认的对生产成本影响最为明显的因素之一。然而CGT药物研发难度高,生产工艺复杂,生产成本高,都给产能建设增添了不少难度。
事实上,全球CGT CDMO产能问题一直都在持续,甚至海外MNC也在面临产能的困扰。今年3月,强生决定暂停推进CAR-T西达基奥仑赛在英国的报批程序,正是因为暂时无法生产出足够供给支持英国患者所需的产品。为解决CAR-T产能问题,强生/传奇生物不仅自建产能扩张,还与诺华就西达基奥仑赛技术转让、生产及临床供应服务签订了有效期三年的协议。
算算AAV,产能“缺”多少
根据测算,全球CGT市场38%产能小于100L,其中病毒载体的生产能力需要增加5-500倍才能满足最终的商业需求。目前行业平均等待时间为16个月,甚至长达两年。盘点已上市的AAV疗法,我们不难发现,在不同的注射方式中AAV的临床用量差异较大。根据临床用量来计算生产需求,对于眼科等局部病毒递送的适应症而言,只需生产1016-1017vg病毒即可满足10,000名患者接受基因治疗疗法;但是,对于大量的需要全身递送载体的基因治疗适应症,如血友病,则需要生产1019-1020的病毒才能够满足10,000名患者接受基因治疗疗法,这对于目前的AAV基因治疗产能而言是一个巨大的挑战。与其寄希望于研发出临床用量更低的药物,不如相信CGT CDMO一定会抓住产能缺口,针对AAV生产能力的提升。
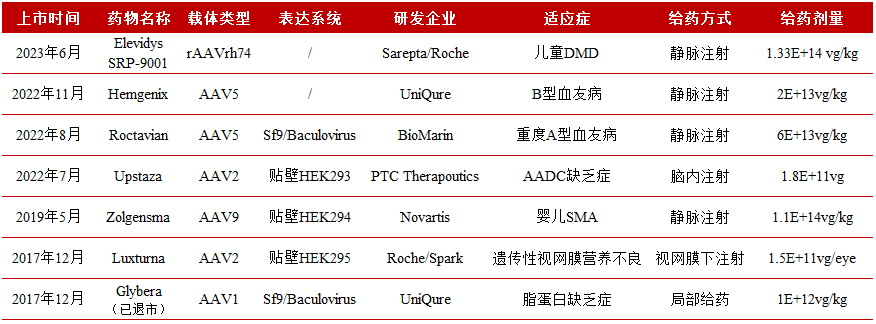
▲ 已上市的AAV疗法,图源:医麦客整理
根据CELL & GENE THERAPY INSIGHTS最近的一份综述分析,假设10,000名治疗杜氏肌营养不良症(DMD)患者接受AAV基因治疗疗法,按照目前的生产产率计算,该患者群体所需要的AAV总量大概需要80个3,000L一次性生物反应器,以每年20批次的效率来产出,大致相当于目前全球总产能的三倍!这也凸显了目前基因治疗载体产能的严重不足。
如何实现产能“弯道超车”
CGT病毒载体短缺可以通过扩大生产规模、提升技术缩短制备周期,但病毒载体的质量、批次间的差异往往不可控,因此产能扩张仍然是CGT CDMO解决产能问题的主要方式。目前,CGT市场仍然缺少成熟的CDMO供应企业,全球病毒载体CDMO都在近几年投入重金扩大产能。据悉,由于需要个性化定制,CGT产能建设耗资巨大且难度较高,从建设到投入使用往往需要近2年,这些因素也导致目前国内CGT CDMO仍存在产能缺口。因此,探求除了扩大生产规模以外的增产方式也是实现“弯道超车”的必然之举。采取更容易进行规模化生产的生产工艺便是这样一种另辟蹊径的解决方案。
AAV载体生产的主要技术体系有HEK293三质粒共转染系统和昆虫细胞杆状病毒包装系统(Bac/Sf9)(以下简称“IC-BEVS系统”)。目前已上市的AAV产品中也几乎都采用了这两种方法,其中HEK293三质粒共转染系统由于其起步快、周期短、感染效率高、操作简便、安全性较高等优点,成为实验室及制药工业领域最常用的AAV生产方法之一。但由于其较为依赖GMP级质粒生产,贴壁培养的可放大性有限,产量较低,生产成本居高不下,甚至间接导致了“史上最贵疗法”的诞生,可见其在规模化生产方面并不具优势。而IC-BEVS系统则天然存在悬浮培养的优势,且容易在无血清培养基中存活,可在一些大型发酵罐中进行培养用于生物药物的快速生产,或许就是实现提升产能、降本增效的“超车”秘籍之一。
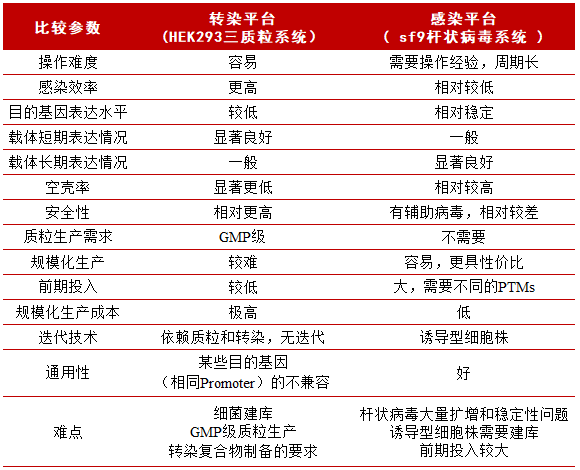
▲ 转染生产工艺对比图,图片来源:医麦客整理
没有什么方法是完美的,由于增加了病毒制备过程,IC-BEVS系统制备周期长,杆状病毒的不稳定性会影响工艺放大,并有VP1/2/3比例引起的感染力问题。最关键的是潜在的昆虫弹状病毒问题。2014年,FDA报告了每个Sf细胞系,包括两个商业来源Sf21和Sf9细胞,被污染了一种新的病毒,这种病毒现在被称为新弹状病毒(Sf-RV)。监管机构为了保证生物制品的安全性,希望所有生物制品都经过病毒检测,一旦发现了任何外源病毒污染,都要采取一切办法将它去除,以降低病毒污染的风险,在国内也不乏看到因基于弹状病毒污染sf细胞被驳回的案例。因此,从细胞源头解决病毒污染问题,使用无弹状病毒污染的Sf9细胞株成为当下的首选。希济生物拥有自主开发的无弹状病毒昆虫细胞株,无弹状病毒Sf9细胞传代稳定,从P20传代至P44,细胞生产能力、活细胞浓度和细胞活率均与有弹状病毒Sf细胞表现一致。
既要又要还要,软硬兼施能做到
病毒载体工艺及大规模GMP生产的难度极高、工艺复杂、产能短缺和制备周期较长,是CGT药物开发的主要瓶颈之一。病毒载体,质粒DNA和其他原材料(血清,转染试剂等)的产能有限,一次性设备组件的交付时间长,经验丰富和熟练的专业人员有限,这些都阻碍了AAV基因治疗产品的开发进度。换言之,能够平衡“合规”、“效率”、“成本”三者之间的关系,同时拥有AAV基因治疗开发、生产和测试专业知识的集大成者少之又少。希济生物目前已经构建了完整的CMC能力,在AAV规模化生产方面形成了高效高质的服务体系,还在今年7月正式落成了规模领先的CGT厂房,可谓兼具硬、软实力。希济生物已经形成了自主知识产权的技术和工艺平台、攻克关键技术的研发能力、CGT药物从0到1的成功经验、供应链管理和成本控制和完整GMP项管和质量体系五大核心竞争力,在规模放大的技术和设施全方位处于国内行业领先地位。
在产能优势上,希济生物引进成熟的IC-BEVS病毒平台,拥有3条生产线,可实现3L-200L灵活放大的悬浮慢病毒生产,年产能达90批次,目前已经成功完成5批200升规模生产,Sf9悬浮细胞生产纯化后单次产量可达2E+16vg/批以上,处于行业领先地位。同时,希济生物的质粒平台上拥有2条生产线,可实现10L-200L快速高密度发酵工艺,产量最高达克级/L;细胞平台拥有超200平米的GMP级细胞产业化平台,采用领先行业的全封闭无血清工艺,可以满足从科研到临床试验、商业化不同阶段的需求。加之8000平米CGT厂房投入使用,坐拥15条GMP级生产线、800平米研发实验室、P2实验室以及生物样本管理系统,已然拥有目前行业领先的CGT GMP设施,有效优化当下CGT领域普遍存在的产能不足问题,帮助创新药企解决后顾之忧。
在质量保证优势上,希济生物打通了AAV上下游生产开发能力,从高性价比、高标准的质粒的平台,到杆状病毒与细胞库的建立与表征,再从开发、放大、生产多种AAV工艺与平台的搭建,到完备的分析平台与质量控制,无论是GMP设备还是工艺技术都兼容满足多品种、多包材、多种测试的要求,在满足cGMP/GMP的法规要求的基础上建立了“希济标准”,为实现研发到GMP生产的无缝对接提供了全方位的保障。同时,希济生物已完成了质量体系2.0的升级,建成了完整的药品生产质量管理体系,涵盖了药品研发、注册临床到商业化生产的全生命周期,并且针对药品不同生命周期阶段,贯穿项目管理,建立分级质量管理策略,做到科学管理、有效管理,防止质量管理的过度或不足。

▲ 图片来源:希济生物
在技术优势上,希济生物拥有国内首创的悬浮无血清慢病毒制备技术是当下行业领先的慢病毒工艺,相较于贴壁工艺而言,在规模放大及成本上具有显著优势。此外,希济生物具有一系列自主创新平台,打造了成熟的AAV载体平台工艺及质量体系,能够根据客户需求提供工艺开发、工艺优化、工艺升级等服务,并已拥有成功交付的实战经验。下游纯化工艺可以采用纯柱纯化或柱纯化加超离的工艺,超离后空壳率可控制在5%以下。
在效率优势上,依托强大的产能优势与技术优势,希济生物最快可半年完成质粒&慢病毒从菌种库建立到病毒IND三批次生产的交付,交付时间较业内平均时间缩短20-30%,助力CGT药物研发降本增效。
在经验优势上,希济生物脱胎于艺妙神州,其团队拥有近10年的CGT产品研发生产积累和从0到1的成功经验,已经成功助力获批了6个临床批件,包括一个实体肿瘤CAR-T批件。在成立短短一年半时间里,希济生物已签署及确认合作在签合同超过20项,合作客户超7家,订单总金额已超1.5亿人民币。
CMC能力是将科学发现转化为产品的基础,也是抓住产能缺口的关键,更是AAV产品实现降本增效的必由之路。希济生物不仅有完善的CMC能力,还能够实现快速迭代,有保持可持续CMC能力的实力,兼顾兼容性和灵活性。与大多从单一优势技术切入的企业不同,希济生物正在打造具有“新”“全”“精”特色的一站式CGT CDMO服务及解决方案,旨在解决日益增长的AAV以及整个CGT药物临床开发需求和缺乏高标准、不依赖海外技术的矛盾,为客户提供从科研到商业化不同级别的质粒、病毒、细胞、胞外囊泡等研发、注册及生产服务,助力企业研发出价格更低、疗效和安全性更优的差异化AAV创新药物,进而助推AAV,乃至整个CGT领域发展。

 产业资讯
产业资讯
 识林
识林  2026-05-23
2026-05-23
 505
505

 产业资讯
产业资讯
 米内网
米内网  2026-05-23
2026-05-23
 415
415

 产业资讯
产业资讯
 药通社
药通社  2026-05-23
2026-05-23
 428
428
 热门资讯
热门资讯