 产业资讯
产业资讯
 求实药社
求实药社  2023-12-20
2023-12-20
 10112
10112
红斑狼疮曾被称为世界三大疑难病,也被很多人称为“不死的癌症”。
系统性红斑狼疮(Systemic lupus erythematosus,SLE)是红斑狼疮最严重的一种形式,是系统性自身免疫疾病,可导致肾脏、心血管、肺、消化系统、血液系统、血管、眼部等多器官损伤。最明显的症状就是面颊出现“蝶形红斑”。多发于15~45岁的生育年龄女性,男女比例约为1:9。我国流行病学调查报告显示,SLE患病率为70/10万人,中国约有患者100万人,全球约有患者500万人。
SLE的治疗可谓有着巨大临床需求,但由于其发病机制复杂,新药研发之路异常困难,国际上多项研发项目均以失败告终。
SLE全球管线现状
2023年12月13日,全球共布局353条在研管线用于治疗系统性红斑狼疮适应症,其中国内有160条在研管线。值得注意的是,目前,以上国内外SLE适应症的在研管线有近1/3已经处于终止状态,包括辉瑞、安进、吉利德、罗氏、AZ、渤健、施贵宝、赛诺菲、礼来、GSK等药企巨头的在研项目。
本文收集了国内针对SLE适应症处于上市/研发后期,或有代表性的近50款药物信息,如果有数据更新不及时的情况,敬请谅解。
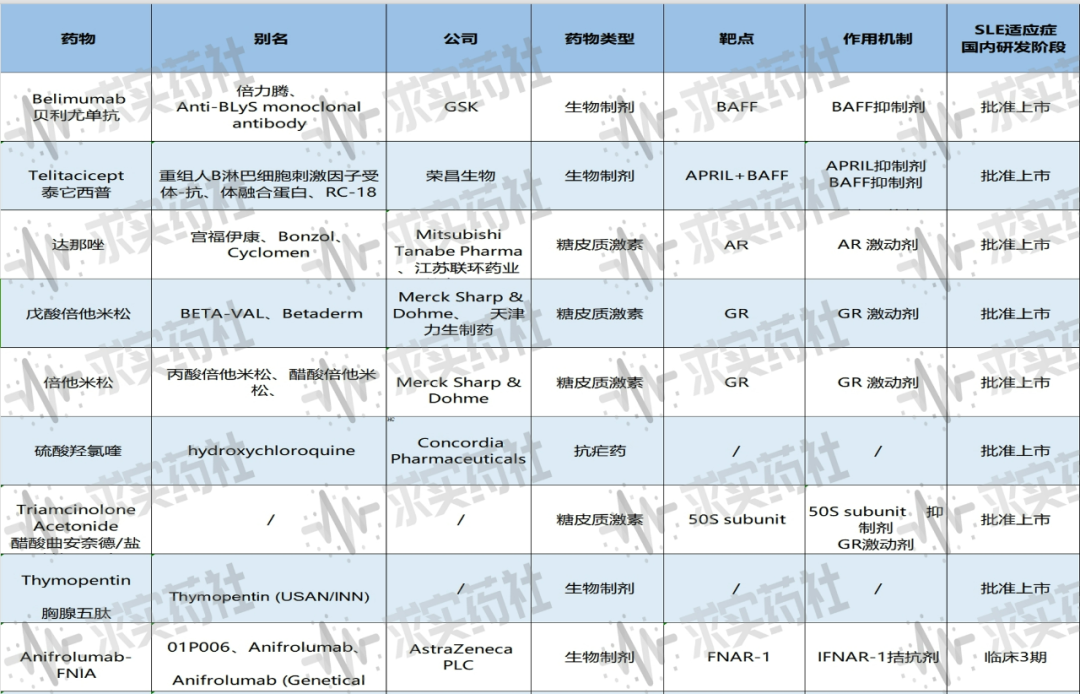




图片来源:新药数据库、药融云、官网等;求实药社整理
表格数据可见,研发项目中用于治疗SLE的药物主要有糖皮质激素、免疫抑制剂、抗疟药及生物制剂等。下面,将按照SLE的不同疗法对表格中部分药物进行分类解读。
生物制剂
生物制剂是SLE领域的新兴疗法,在过去60余年,仅有贝利尤单抗获得FDA和NMPA批准用于治疗SLE,泰它西普获NMPA批准上市。
GSK的贝利尤单抗作为首个获得FDA和NMPA批准用于治疗系统性狼疮和成人活动性狼疮性肾炎的药物,历来为人瞩目。贝利尤单抗是一款靶向B淋巴细胞刺激因子(BLyS)的人源化IgG2λ单克隆抗体,2011年、2019年分别获得美国FDA、国家药监局批准,也是中国首个获批用于治疗系统性红斑狼疮的生物药。自其上市以来,在全国医院已累计销售711610,销售总额约5.3亿元。
荣昌生物的泰它西普是中国首个获批用于治疗SLE的“双靶”生物制剂(融合蛋白),2021年3月获得国家药品监督管理局附条件上市批准,并被纳入2022版国家医保目录。2023年11月,荣昌生物“泰它西普”正式获得国家药品监督管理局同意,由附条件批准转为完全批准。泰它西普目前仅在中国销售,2021年销售额约为4730万元。
利妥昔单抗是一种靶向性针对B细胞表面CD20抗原的单克隆抗体,通过与B细胞表面CD20抗原特异性结合,杀伤B细胞。利妥昔单抗的适应症是治疗慢性淋巴细胞白血病 (CLL)、某些类型的非霍奇金淋巴瘤(NHL)等疾病。但因为国内外指南的推荐,利妥昔单抗被超适应症用于重度SLE和狼疮肾炎。
阿斯利康的Anifrolumab(阿尼鲁单抗),它是一种直接针对I型干扰素(IFN)α受体1(IFNAR1)的亚基1的IgG1k 单克隆抗体。Anifrolumab于2021年7月在美国上市,获批适应症为成人中重度SLE。目前Anifrolumab在中国开展SLE临床3期试验。
Biogen(渤健生物)的BIIB059是一种靶向血液树突状细胞抗原2(BDCA2)的全人源化IgG1单克隆抗体,是全球唯一进入临床阶段的BDCA2单抗,目前系统性红斑狼疮(SLE)适应症已推进至临床3期,皮肤红斑狼疮(CLE)适应症处于3期临床。
罗氏的奥妥珠单抗是一种人源化第二代抗CD20单克隆抗体,目前关于奥妥珠单抗的两个3期临床试验REGENCY(NCT 04221477)和OBILUP(NCT 04702256)正在进行中。
UCB和渤健生物联合开发的Dapirolizumab pegol,展示出良好的耐受性和对于SLE疾病活动的改善作用,目前正在进行扩大样本量的临床3期研究。
艾伯维开发的乌帕替尼是一款高选择性的JAK-1抑制剂,FDA批准其用于治疗溃疡性结肠炎、中轴型脊椎关节炎、类风湿性关节炎、银屑病关节炎和特应性皮炎,目前尚未有JAK抑制剂获批用于SLE。该款药物目前处于临床3期。
华东医药则通过其全资子公司中美华东与美国一家临床阶段的生物制药公司Provention Bio达成独家临床开发及商业化协议,获得Provention Bio在研产品——双特异性抗体PRV-3279两个临床适应症(用于治疗系统性红斑狼疮处于美国临床1期,用于预防或降低基因治疗的免疫原性处于美国临床前研究)在大中华区的独家临床开发及商业化权益。目前该款药物在国内处于临床2期阶段。
康诺亚的CM313注射液是中国首款获国家药监局临床试验申请批准的国产抗CD38抗体,SLE适应症的研发目前2期临床阶段。
恒瑞医药1类新药SHR0302缓释片于12月14日获国家药监局临床试验申请批准,拟开发治疗系统性红斑狼疮。
嘉兴特科罗生物针对系统性红斑狼疮的研发管线中的一款口服药物TDM-003已经在CMC阶段。
南京艾美斐生物7月18日宣布,其自主研发、拥有全球知识产权的1类小分子新药IPG11406治疗系统性红斑狼疮(SLE)的临床试验申请已经获得国家药品监督管理局药品审评中心(CDE)批准,将积极开展针对狼疮性肾炎的临床研究。
爱科诺生物自主研发的拥有全球权益的创新口服小分子高选择性TYK2/JAK1抑制剂AC-201获国家药品监督管理局(NMPA)批准,即将在中国正式启动临床试验。AC-201于今年5月份获澳大利亚HREC批准开展临床试验,目前澳洲I期临床试验正进行中。
免疫抑制剂
免疫抑制剂与激素联合使用有利于控制SLE活动度,减少复发,以及减少长期激素用量和副作用。免疫抑制剂也同样存在感染、骨髓抑制、肝肾毒性、生殖毒性等多种不良反应,其应用受到很大限制。
艾伯维今年5月表示,在一项系统性红斑狼疮(SLE)的2期试验中,其免疫学明星产品乌帕替尼单独使用或联合使用均达到了主要终点和关键次要终点。目前,该款药物的SLE适应症在国内处于临床3期。
Deucravacitinib(氘可来昔替尼)是一款被多国批准用于成人斑块型银屑病的口服、选择性、异构酪氨酸激酶2抑制剂。过去的多项临床研究表明,在系统性红斑狼疮(SLE)患者中,Deucravacitinib(氘可来昔替尼)在多个治疗终点上呈现出显著疗效,其中包括系统性红斑狼疮反应指数4(SRI-4)在32周时的表现以及低疾病活性状态(LLDAS)在48.1周的展示。LLDAS与SLE相关器官损伤和死亡率的降低有着显著的联系。目前,该款药物的SLE适应症在国内处于临床3期。
巴瑞替尼是礼来和Incyte公司联合研发的口服JAK抑制剂。巴瑞替尼在SLE的Ⅱ期临床研究中也取得了较好疗效。小规模观察性研究发现托法替布对SLE 患者的皮疹和关节炎具有一定疗效。脾脏酪氨酸激酶抑制剂等能显著减轻狼疮小鼠皮肤和肾脏病变。目前,该款药物的SLE适应症在国内的临床3期显示处于终止状态。
泰瑞米特钠由苏州长征-欣凯制药(江苏吴中医药控股子公司)和欣凯医药共同研发,用于治疗系统性红斑狼疮和风湿性关节炎的药物。该化合物2013年1月向国家食品药品监督管理总局提交临床试验申请( 泰瑞米特钠片、泰瑞米特钠,化药1.1类),于2014年10月获得化药1.1类临床批件。目前,该款药物的SLE适应症在国内处于临床2期。
奥布替尼是诺诚健华研发的1类新药,是具高度选择性的新型BTK抑制剂,旨在用于治疗血液肿瘤及自身免疫性疾病。奥布替尼在中国治疗系统性红斑狼疮(SLE)II期研究都已获得概念验证(PoC)。
糖皮质激素
目前,糖皮质激素是治疗SLE的最常用药物,在诱导缓解期能快速控制疾病活动;在病情缓解后,能帮助保持缓解状态,保护重要脏器功能。在我国,激素的使用存在剂量大、时间长的特点。激素剂量越大,疗效越显著,但副作用也随之增加。据统计,激素相关不良反应发生率>30%。
针对SLE适应症已上市的达那唑、戊酸倍他米松、倍他米松、醋酸曲安奈德/盐酸林可霉素都属于糖皮质激素类药物。
抗疟药
羟氯喹是治疗SLE的基础用药,可通过抑制自身抗原的加工和呈递、减少炎性细胞因子表达、抑制溶酶体功能等多种途径发挥抗炎与免疫调节作用,进而延缓SLE病情进展。羟氯喹的重要副作用—眼毒性表现为角膜沉积、眼调节反射障碍和视网膜病变,是限制其临床使用的重要原因。
硫酸羟氯喹片属于新型喹诺酮类药物,通过调节机体免疫功能改善系统性红斑狼疮患者的临床症状,可减少激素用量,修复皮肤损伤。Concordia Pharmaceuticals的硫酸羟氯喹已批准上市。
双氢青蒿素(DQHS)新增SLE适应症的临床申请由中国中医科学院中药研究所于2016年1月正式提出,2016年3月已经获得了药监局临床批准,目前由昆药集团开展临床二期试验。根据文献对DQHS治疗SLE作用机制的报道,其能明显改善BXSB小鼠LN的病理状态。另外,DQHS通过抑制B淋巴细胞增殖,促进CD4T细胞和CD8T细胞的增殖,尤其是CD8T细胞增殖明显,减少B细胞分泌自身抗体,从而达到治疗红斑狼疮的作用。目前,该款药物的SLE适应症在国内处于临床2期。
结语
近年来SLE的诊断和治疗方面取得了较多新进展,从最初对SLE治疗的束手无策,到后来的糖皮质激素和免疫抑制剂应用,再到现在的生物制剂和精准医学,医学正一步步朝着提高SLE患者疗效和预后的目标迈进。但SLE是一种非常复杂的疾病,存在很大的临床异质性,而且SLE发生发展的分子机制还不十分清楚,攻克这一医学难题还有一段很长的路要走。

 产业资讯
产业资讯
 一度医药
一度医药  2026-06-03
2026-06-03
 340
340

 产业资讯
产业资讯
 健闻咨询
健闻咨询  2026-06-03
2026-06-03
 436
436
 产业资讯
产业资讯
 医药魔方Invest
医药魔方Invest  2026-06-03
2026-06-03
 439
439
 热门资讯
热门资讯