 研发追踪
研发追踪
 细胞基因治疗前沿
细胞基因治疗前沿  2024-05-27
2024-05-27
 2428
2428
5月20日,T细胞免疫治疗领域领导者Atara Biotherapeutics宣布,已向美国FDA提交了tabelecleucel(tab-cel)的生物制品许可申请(BLA),作为爱泼斯坦-巴尔病毒(EBV)阳性的移植后淋巴增殖性疾病(PTLD)单药疗法,用于至少接受过一次治疗的成人以及两岁以上儿科患者。
Atara 总裁兼首席执行官 Pascal Touchon 说道:“tab-cel 的 BLA 提交,对于同种异体 T 细胞治疗领域来说是一个重要时刻。如果tab-cel获批,将成为全球首款同种异体T细胞免疫疗法,以及治疗EBV阳性PTLD的首款疗法。”

PTLD是一种罕见且可致命的急性血液癌症,常见于实体器官移植(SOT)或同种异体造血细胞移植(HCT)后,发病率约1%-30%,目前,该疾病尚无获批疗法。
Tab-cel是一种同种异体的EBV特异性T细胞免疫疗法,旨在靶向并消除EBV感染的细胞。此次BLA得到了超430名患者的数据支持。研究显示:tab-cel客观缓解率达到达到48.8%(p<0.0001)。
目前,Tab-cel 已获得美国 FDA 授予治疗利妥昔单抗难治性 EBV 阳性PTLD的突破性疗法以及孤儿药认定。
Tab-cel 已进入包括冰岛、挪威和列支敦士登,以及27个欧盟成员国市场。2022年12月,欧盟委员会批准tab-cel上市(商品名“Ebvallo”)。2023年5月、2024年5月,英国和瑞士分别批准tab-cel上市。
同种异体,又被称为“现货”(off-the-shelf)和通用型,是从健康的捐赠者那里收集T细胞或干细胞来源的T细胞,经过工程化设计表达CAR,以识别和摧毁癌细胞,并限制病人自身免疫反应。相比自体T细胞疗法,现货型Ebvallo有望解决成本过高的问题,并规避制备能耗、时长、高度“定制化”与无法形成规模化效应带来的可及性限制因素。
放眼国内,布局同种异体细胞疗法的公司有传奇生物、亘喜生物、科济生物、茂行生物、晨泰医药、济因生物等。
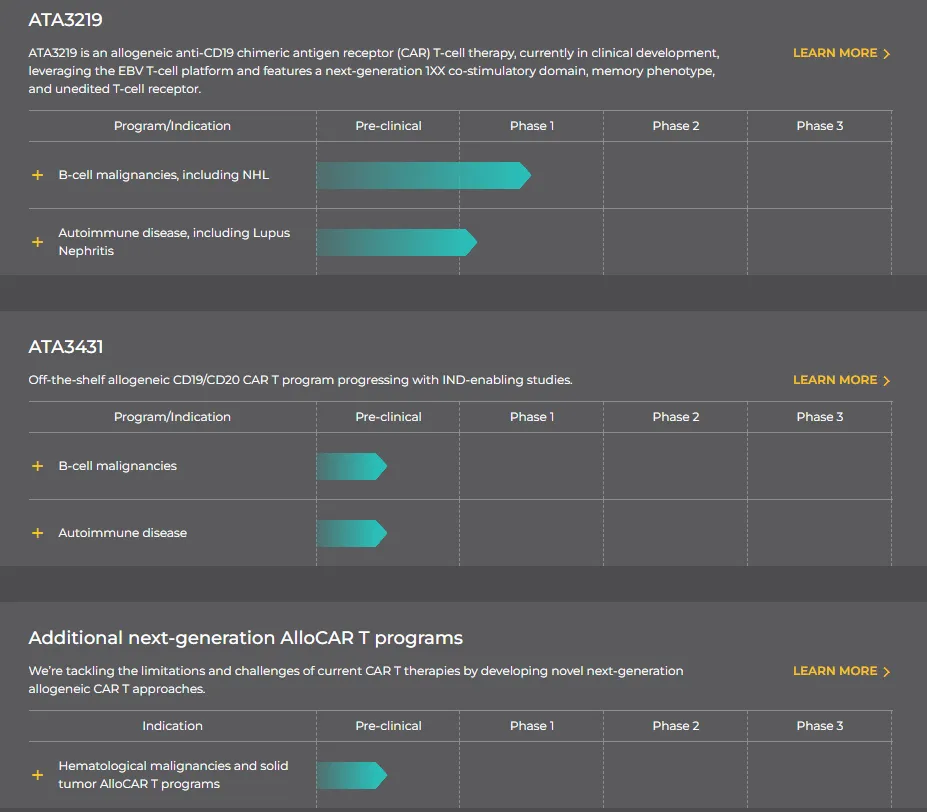
关于Atara BiotherapeuticsAtara Biotherapeutics于2012年8月成立,是一家领先的现成同种异体T细胞免疫治疗公司,为癌症、自身免疫性疾病和病毒性疾病患者开发新型治疗方法。Atara最先进的T细胞免疫疗法是tabelecleucel。而Tab-cel还开发了用于B细胞淋巴瘤的同种异体CAR-T疗法ATA3219、ATA3431以及用于多发性硬化症的现货型T细胞疗法ATA188。其中,ATA3219于今年3月份获得FDA批准用于治疗狼疮性肾炎的IND申请,成为全球首个自免适应症获批临床的通用型CAR-T疗法。这是ATA3219继非霍奇金淋巴瘤(NHL)后获得的第二个IND批件。
研发管线

参考资料:
https://investors.atarabio.com/news-events/press-releases/detail/348/atara-biotherapeutics-submits-tabelecleucel-tab-cel

 研发追踪
研发追踪
 医麦创新药
医麦创新药  2025-06-30
2025-06-30
 6
6

 研发追踪
研发追踪
 凯莱英药闻
凯莱英药闻  2025-06-30
2025-06-30
 7
7

 研发追踪
研发追踪
 医药观澜
医药观澜  2025-06-30
2025-06-30
 8
8