 产业资讯
产业资讯
 抗体圈
抗体圈  2024-06-04
2024-06-04
 915
915
5月30日,吉利德公布了Trop2 ADC 戈沙妥珠单抗(Trodelvy)治疗局部晚期或转移性尿路上皮癌(mUC)的3期TROPiCS-04确证研究的初步结果,研究没有达到总生存期(OS)主要终点。
1月22日,吉利德宣布Trodelvy对比多西他赛治疗经治转移性或晚期非小细胞肺癌(NSCLC)患者的III期EVOKE-01研究未达到总生存期(OS)的主要终点。
5月27日,阿斯利康和第一三共也披露了DS-1062在全人群的晚期非鳞状非小细胞肺癌中III期数据不及预期。
不可忽视的安全性问题
ADC的设计理念是通过将细胞毒性药物精确地传递到目标细胞,以解决传统化疗药物疗效受限和副作用较大的问题。然而,理想与现实之间往往存在差距。即便是效果显著的药物,也难以达到完美无缺。在ADC药物展现出显著疗效的同时,其潜在的毒性问题同样不容忽视。
2023年7月,阿斯利康与第一三共联合开发的TROP2靶向抗体药物复合体DS-1062,在晚期非小细胞肺癌(NSCLC)患者的III期临床试验中达到了无进展生存期(PFS)的主要研究终点。尽管这一结果被视为“正面”,市场的反应却出人意料地消极。第一三共的股价遭遇了自2008年以来最大的单日下跌,跌幅达到了15%;而阿斯利康的股价也下跌了8%,导致公司市值减少了约195亿美元。一个关键的担忧是药物的安全性问题。间质性肺炎的风险再次被提及,同时在DS-1062的临床试验中还记录了一些5级严重不良事件,这意味着有患者因药物的副作用而不幸去世。
吉利德公司在2020年推出了其备受瞩目的药物Trodelvy,该药物在上市之初便以210亿美元的巨额投资获得了市场的关注。该药物在去年的销售额突破了10亿美元大关,显示出其强劲的市场潜力。然而,一些行业分析师警告说,如果戈沙妥珠单抗未能获得尿路上皮癌适应症的正式批准,其销售收入可能会下降高达33%。在最不利的情况下,该药物甚至可能面临被迫退出市场的风险。
并且在临床试验ASCENT中的表现并未达到预期。该研究显示,患者在接受治疗时遭遇了较高的3级及以上不良事件,其发生率为45%。其中,疲劳、恶心、腹泻以及中性粒细胞减少等不良反应尤为突出,分别占据了52%、62%、65%和64%的比例。特别值得注意的是,中性粒细胞减少和腹泻这两种副作用的严重性,已经引起了美国食品药品监督管理局(FDA)的关注,并被特别标注为黑框警告。
甚至一些ADC因安全性问题导致项目终止。
Vadastuximab talirine是由Seagen开发的靶向CD33的ADC药物,2017年6月Seagen宣布停止项目开发,主要原因是:在III期试验中出现多例患者死亡。
Magenta开发了MGTA-117,由靶向CD117的单抗与Amanitin(鹅膏蕈碱)偶联而成。2023年1月25日,根据Magenta Therapeutics公布的研究数据,队列3的一例患者在接受0.08mg/kg剂量的MGTA-117给药后出现了呼吸衰竭及心脏骤停所致的死亡(5级严重不良事件)。Magenta表明该患者的死亡可能与MGTA-117治疗相关并随即暂停了该研究,最终MGTA-117项目还是宣告失败。
黑暗之后总会迎来曙光
科伦博泰/默沙东的SKB-264是目前国内进展较快的Trop-2靶点ADC药物。相较于其他Trop-2 ADC药物,其颇具破局之处在于安全性。
科伦博泰在2024年美国癌症研究协会(AACR)年会上公布的数据,其研发的二线非小细胞肺癌(NSCLC)治疗药物SKB-264在EGFR基因突变的患者中表现出了显著的治疗效果。在一项非头对头的比较研究中,SKB-264在21名受试者中实现了60%的客观缓解率(ORR),并且无进展生存期(PFS)达到了11.5个月,这一效果在同类药品中显得尤为突出。
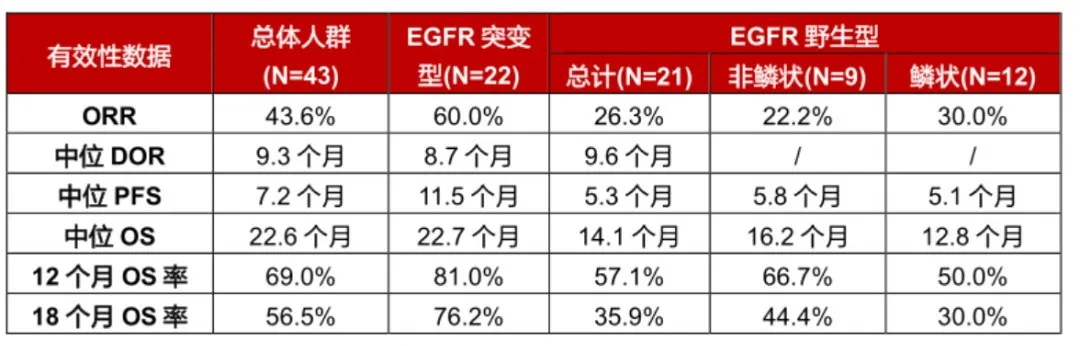
SKB264 治疗 NSCLC 的临床数据(来源:瞪羚社)
在安全性方面,SKB-264目前为止并未在临床中发现有间质性肺炎相关的副作用,主要三级以上副作用来自于血液毒性,包括中性粒细胞减少、贫血和白细胞减少等。
5月24日,科伦博泰宣布将在2024年美国临床肿瘤学会(ASCO)年会上公布两项临床研究结果。研究人员将以口头报告的形式公布2期临床OptiTROP-Lung01的结果。截至2024年1月2日,1A队列和1B队列分别入组40名及63名患者。

2期临床OptiTROP-Lung01(来源:ASCO官网)
在队列1A和1B中,观察到的治疗相关不良事件(TRAE)中,最常见的严重程度达到3级或以上的包括中性粒细胞减少、白细胞计数下降、贫血、皮疹以及药物疹。特别地,在1B队列中,有一位患者因发生超敏反应而不得不中断了芦康沙妥珠单抗的治疗,没有记录到任何因治疗相关不良事件导致的死亡案例。
诗健生物在ASCO上公布了TROP2 ADC产品ESG401在一线三阴乳腺癌患者中的最新临床结果。本次报告总结了Ib期试验中一线mTNBC队列的阶段性结果。

ESG401 Ib期试验(来源:ASCO官网)
在14例疗效可评估的受试者中,ORR为78.6%,其中1例(7.1%)患者达到完全缓解(CR),DCR为100%,CBR为85.7%。8例患者(57.1%)的PR已确认。至截止日期,仍有14例(63.6%)患者正在接受治疗,最长的治疗持续时间为8.0个月。
安全性与之前的报告保持一致,没有发现新的或非预期的安全信号。最常见的TRAEs为白细胞减少(65.2%)、中性粒细胞减少(69.6%)、贫血(43.5%)、乏力(21.7%)、恶心(43.5%)和呕吐(34.8%)。最常见的≥3级TRAE为中性粒细胞减少症(43.5%)。未发生≥3级腹泻。到目前为止,在整个Ia/Ib期试验的139例患者中,均未报告有间质性肺病(ILD)。
结语
胜败乃兵家常事,放到ADC药物临床同样不例外。应该让失败成为前进的动力,不断改进ADC药物,相信总有一天会绽放光芒。
附录:
ADC的研发之路不可能是一帆风顺的,其中有一些先驱已经倒下了,根据统计,ADC领域有超过100个药物终止研发,其中有一部分就倒在了临床阶段。
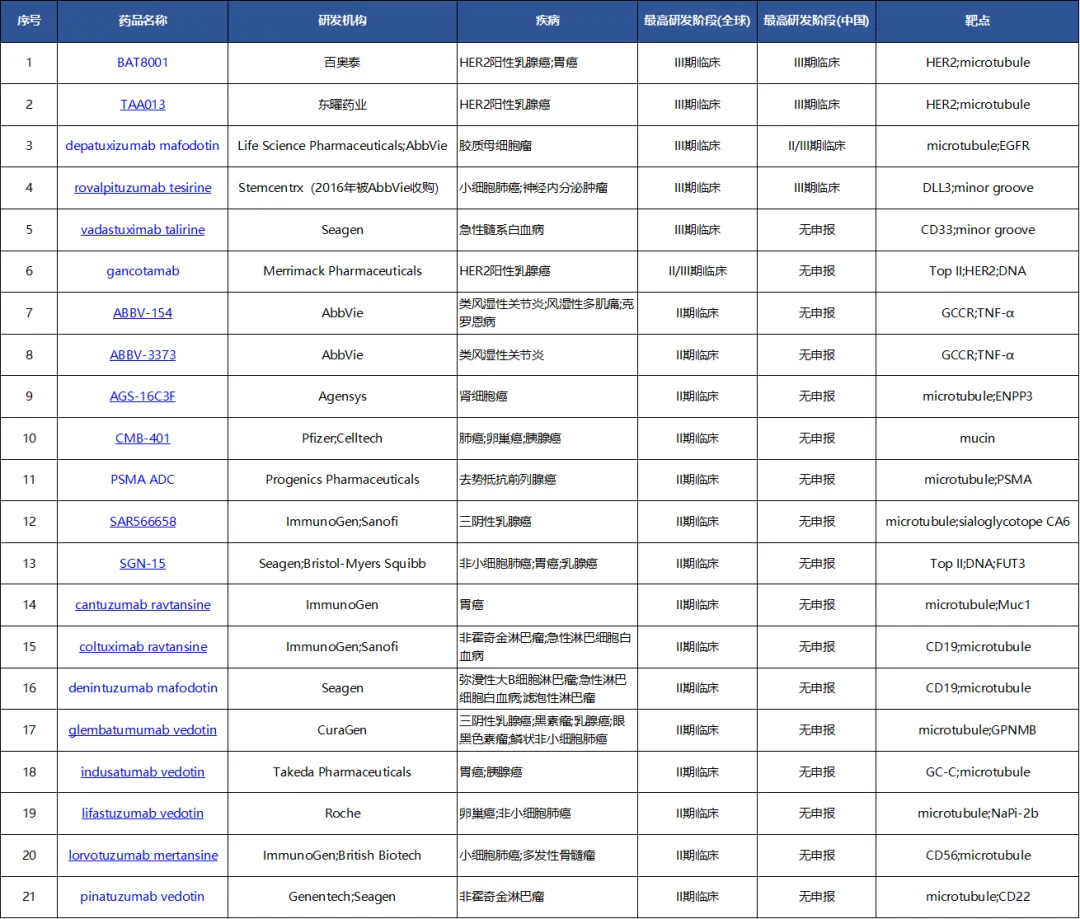
部分临床II期及以上终止研发的ADC药物(来源:医药魔方统计)
资料来源:
1.ASCO官网
2.跨国药企都失败了,中国那么多Trop2 ADC何去何从?.健识局.2024-06-01
3.ADC太浪摔了一跤.瞪羚社.2024-05-28
4.药物研发道阻且长:盘点ADC药物十大失败案例.猎药人俱乐部.2023-06-21
5.ADC的火热新战场,Trop2 靶点繁荣背后.氨基观察.2023-08-16
6.百亿级蓝海赛道,国产药企能否在TROP2 ADC扳回一城?.一度医药.2023-08-28

 产业资讯
产业资讯
 UmabsDB
UmabsDB  2025-06-23
2025-06-23
 2
2

 产业资讯
产业资讯
 支点财经
支点财经  2025-06-23
2025-06-23
 2
2

 产业资讯
产业资讯
 药视声
药视声  2025-06-23
2025-06-23
 2
2