 产业资讯
产业资讯
 医药魔方
医药魔方  2024-06-28
2024-06-28
 1051
1051
癌症,这个现代医学面临的最重大的课题,似乎已变得并非那么不可战胜。尤其是近十年来,以PD-(L)1为代表的免疫肿瘤药物横空出世,多次刷新各个肿瘤领域的治疗标准,在深刻改变了癌症治疗格局的同时也收获了巨大的商业成功,甚至成为化疗之后,又一肿瘤治疗的基石。
正因如此,这一赛道从产品数量到获批适应症都已呈现极为拥挤的态势:一边是全球已有22款PD-(L)1单抗获批上市,其中17款已在中国上市、7款还在等待监管机构批准;另一边则是非小细胞肺癌、胃癌、食管癌等大癌种的单药/联合化疗方案几乎被探索殆尽。留给后来者的市场空间只会越来越小。
另一方面,未被满足的临床需求始终存在,对更高疗效目标的追求也远未到尽头。而疗效的突破往往建立在前人探索的基础之上,正如同PD-(L)1的成功要很大程度上归功于在各种标准化疗方案上做“加法”,在PD-(L)1隐约已成为又一标准治疗的当下,探索“PD-(L)1+”治疗模式——与更多药物组成搭档,或开发PD-(L)1多靶点药物——已成为业界公认的重要突破口之一,各路玩家纷纷围绕不同的思路展开了探索。
各花入各眼,PD-(L)1搭档怎么选?
长期以来,抗血管生成药物是各家PD-(L)1产品除化疗外最常规的搭档,例如卡博替尼、仑伐替尼、阿帕替尼,以及大分子的贝伐珠单抗等。但这种组合疗法的适应症覆盖局限于肝细胞癌、肾细胞癌等几个特定癌种。此外还有一些依赖特定靶点的靶向药物(如抗HER2靶向药物),与PD-(L)1的联用更是仅局限于个别适应症。
近年来,随着多款新型ADC展现出色的疗效数据后,PD-(L)1+ADC组合随即成为如今热点之一,首个PD-1+ADC的联用方案也已于去年4月获FDA批准上市。此外,其他新型方案,如各种新型免疫检查点抑制剂(TIGIT等)与PD-(L)1的联用,以及各种PD-(L)1双抗,如PD-(L)1/CTLA-4双抗、PD-(L)1/VEGF双抗的探索同样如火如荼。
不过,前沿治疗模式的推广总是伴随着长时间的摸索、验证过程。就目前而言,上述新型“PD-(L)1+”模式的探索、应用都还处在起步阶段,其整体的获益-风险比还有待在更大规模的真实世界应用中进一步验证,治疗相关不良事件(TRAE)的管理经验也还需进一步累积。处在当下免疫单药/联合化疗的探索空间逐步缩小、而新型方案仍然“青黄不接”的阶段,面临尚未被满足的治疗需求,临床更亟需的可能是应用范围更广、且既能提升疗效,又具有更高确定性的“PD-(L)1+”方案。
相对而言,在另一条“PD-(L)1+”的路线——双免领域,得益于更早的起步,现有选择已发展得更为成熟。例如,全球首个“PD-1+CTLA-4”双免疫联合方案“O+Y”组合(纳武利尤单抗+伊匹木单抗)至今已经过了近10年长期、广泛的验证,堪称现阶段“PD-(L)1+”方案中的“明牌”。
一方面,“O+Y”的协同作用机制明确,且双免的特点使得其不受特定靶点限制,覆盖瘤种广泛,目前已在全球获批9项适应症,涵盖黑色素瘤、肾细胞癌、结直肠癌、非小细胞肺癌、肝癌、胸膜间皮瘤、食管鳞癌,是迄今为止除联合化疗外,获批适应症最多的PD-(L)1组合疗法。
另一方面,“O+Y”经过了长时间、大规模人群的探索和应用,其开展的10余项III期研究中,多数的最低随访时间已超过4年,部分研究(CheckMate-214/067)最低随访甚至已达到了90个月,有效性明确,安全性可控。
尽管BMS同样手握ADC等新型药物管线,但目前来看,“O+Y”这手“明牌”在阵中仍扮演着不可替代的角色。尤其是近期,可以看到“O+Y”在适应症拓展方面明显发力,仅最近半年,就相继取得了CheckMate-8HW与CheckMate-9DW两项重量级III期临床研究的成功。
值得一提的是,这两项研究对应的癌种分别为结直肠癌和肝细胞癌,均属于消化肿瘤,这也延续了O药一直以来在中国市场深耕高发的消化道癌种、紧盯未满需求的传统:早在胃癌、食管癌等上消化道大适应症仍存未被覆盖的时代,O药就凭借CheckMate-649/648/577等经典研究,在所有PD-(L)1中率先完成了上消化道领域疾病部位和病理类型的全面覆盖,填补了大量临床空白。
从CheckMate-8HW与CheckMate-9DW可以看出,O药在中国市场的扩张步伐仍在延续上述思路,从上消化道拓展到了更广泛的消化肿瘤领域——其实不停变化的不只是持续更迭的治疗方案,疾病负担也在变:根据最新数据[1],肝癌和结直肠癌已超越胃癌,成为中国发病率最高的两类消化肿瘤。不仅如此,中国肝癌和结直肠癌患者也是更容易从免疫治疗获益的群体。因而,于中国患者而言,上述两项免疫治疗的突破显得尤为关键。
但此时毕竟不同于2020年:目前,免疫治疗早已成为了这两大癌种的一线标准治疗。不过,这一背景恰恰也给了“PD-(L)1+”模式更大的施展舞台:通过发掘其中仍未被满足的临床需求,“O+Y”组合在两项研究中均成功突破了现有治疗方式的瓶颈,触达了更高的疗效目标。
接下来,本文也将结合“O+Y”的机制及疗效特点,围绕具体研究试对上述思路做进一步阐释。
优势互补、高效协同:双免组合的机制奥秘
“O+Y”不仅在既往多项III期研究中被证实获益显著,而且在后续随访中表现出长期、持续的应答。以今年的ASCO大会上,针对食管鳞癌一线治疗的III期CheckMate-648研究45个月随访结果为例,经过近4年随访,接受“O+Y”组合治疗的患者在长期生存率和缓解持续时间(DOR)上获益更为明显。这一疗效特点的背后,是“O+Y”明确的作用机制优势。
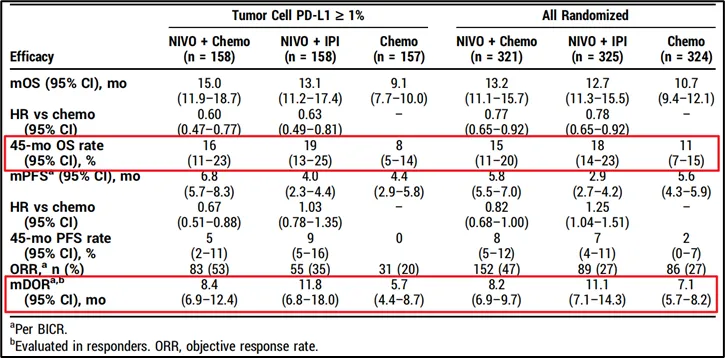
CheckMate-648研究45个月随访结果 来源:ASCO 2024大会摘要[2]
O药和Y药分别靶向的PD-1与CTLA-4均为免疫检查点分子,但两者的作用阶段、机制有所不同,分工明确:
CTLA-4抑制剂——Y药主要作用于T细胞的活化阶段,可控制初始T细胞(包括记忆性T细胞)的活化,激活T细胞识别低亲合力抗原,增殖为效应T细胞,增加能够识别肿瘤的克隆数;
而PD-1抑制剂——O药主要作用于T细胞的效应阶段,直接阻断肿瘤细胞上的程序性死亡配体1(PD-L1)和T细胞上PD-1结合,解除肿瘤细胞的免疫“刹车”作用,重新激活T细胞,增强了T细胞效应功能。
除了上述经典机制解释外,近年来有一种观点认为[3],Y药还可通过其抗体依赖细胞介导的细胞毒性作用(ADCC效应),清除肿瘤微环境内异常高表达CTLA-4的调节性T细胞(Treg)[4],从而进一步解除免疫抑制、加强抗肿瘤效果,这一机制使得“O+Y”有别于现有的PD-1/CTLA-4双抗药物:PD-1/CTLA-4双抗的靶细胞也包括效应阶段的T细胞,因此在药物设计中必须去除其ADCC效应以防止活化的T细胞被吞噬[5],而这也可能导致损失ADCC效应带来的这部分潜在疗效。
总之,“O+Y”组合通过合理的机制互补与协同效应,可以充分调动人体内的免疫“大军”,并改善长期免疫监视,实现高效、持久的抗肿瘤效果。也正是通过将其机制、疗效优势与未满足的临床需求相结合,“O+Y”近期在CheckMate-8HW与CheckMate-9DW两项重磅研究中取得成功,进一步夯实了自身地位。
CheckMate-8HW研究:MSI-H/dMMR结直肠癌一线疗效创新高
国家癌症中心最新数据显示[1],结直肠癌(CRC)已取代胃癌,成为中国最高发的消化肿瘤,在所有癌症中位居第二,仅次于肺癌。CRC的治疗现状不容乐观,其一线治疗首选仍为化疗,但其中有一类人群较为特殊——微卫星高度不稳定/错配修复缺陷表型(MSI-H/dMMR)结直肠癌患者。这类患者对一般的靶向疗法应答不佳,但对免疫检查点抑制剂敏感。因此,这类患者也是免疫治疗的重点人群。
目前,全球仅有一项PD-1单药适应症获批用于一线治疗MSI-H/dMMR CRC。相比于化疗,PD-1单药虽能将患者的疾病进展或死亡风险降低41%,但其在短期和长期获益上仍有提高的空间。短期方面,患者对PD-1单药的应答率较低,约30%的患者无法从中获益,用药后快速出现进展;长期来看,2年PFS率不足50%[6]。
那么,在PD-1单药的基础上加入另一免疫治疗药物,是否会成为该类患者疗效进一步提升的突破口?年初举行的ASCO-GI大会上,CheckMate-8HW研究用震撼性的数据给出了回答:相比于化疗方案,“O+Y”组合可将患者的疾病进展风险降低79%,2年PFS率高达72%[7]。
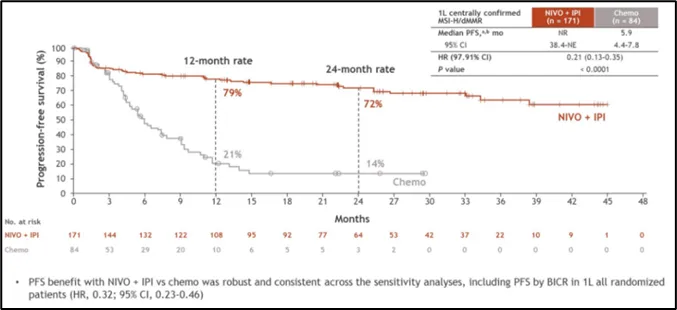
CheckMate-8HW主要终点:PFS
以上数据为双免疗法在机制层面良好的协同效应提供了又一项有力例证,且这一效应在MSI-H/dMMR这一优势人群中可能被进一步放大,最终使得整体疗效在PD-1单药的高水准之上实现了又一次突破。不仅如此,“O+Y”的安全性一如既往得稳定可控,其3-4级TRAE发生率仅为化疗组一半(23% vs. 48%)。
如果说CheckMate-8HW的PFS数据带给人的感受是“震撼”,那么本次ASCO大会上公布的PFS2结果[7](即一线治疗进展+二线治疗进展/死亡的时间)则更深层次地体现了双免治疗强大而独特的“记忆”效应,可为后续免疫治疗的全过程提供获益:在对照组高达67%患者接受后续免疫治疗的情况下,“O+Y”仍可降低73%的二次进展或死亡风险。
值得一提的是,这项研究还包括一个O药单药对照组(尚未披露结果)。从这一设计可以看出来,“O+Y”在追求更高的绝对疗效的同时,也并不回避和目前标准的PD-1单药进行比较,这在PD-(L)1药物逐渐坐稳肿瘤治疗“基石”地位的当下倒是颇有些未雨绸缪的意味。
近期,NMPA已授予“O+Y”组合用于一线治疗MSI-H结直肠癌的新适应症上市申请优先审评资格,国内这类患者有望很快迎来全新的一线治疗方案。
CheckMate-9DW研究:免疫治疗用于肝癌一线首次优于仑伐替尼
而在中国同样高发的肝癌领域,如今已不再缺乏治疗选择,但缺少疗效足够好的药物:
一方面,现有的一线免疫治疗方案ORR多数不足30%,且应答短暂,长期生存获益局限;
另一方面,翻阅这些免疫治疗方案III期研究的设计,会发现获批近20年之久的索拉非尼仍是对照组的“常驻嘉宾”——尽管早在2018年,REFLECT研究就证实仑伐替尼几乎全面优于索拉非尼,但截至CheckMate-9DW前,仍没有任何免疫疗法在III期研究中头对头打败仑伐替尼。
在此背景下开展的CheckMate-9DW并不满足于拿到一个和同类研究相近的结果,从研究设计便足见其雄心勃勃:试验主角选择了“O+Y”组合的同时,挑战对象也从一位(索拉非尼)增加至两位(研究者选择的仑伐替尼或索拉非尼)。
事后来看,CheckMate-9DW的对照组高达85%的患者选用了仑伐替尼,侧面反映出研究的设计不仅更贴合临床实践,以患者为中心,也意在挑战更高的疗效目标。
今年ASCO,CheckMate-9DW研究作为肝胆肿瘤领域唯一的LBA入选大会。结果不负众望,“O+Y”组合成为了第一个在头对头研究中战胜仑伐替尼的肝癌一线治疗方案,将整体疗效提升到了一个新的高度——ORR首次达到36%,而且一旦有效,获益持久:中位获益时间超过30个月,近一半患者的OS可达到两年,使其得以在一众治疗方案中脱颖而出。
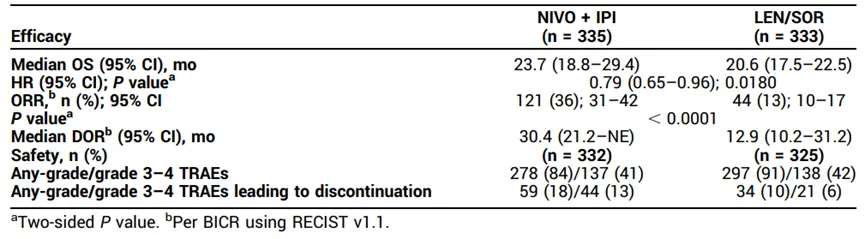
CheckMate-9DW:主要结果 来源:ASCO 2024大会摘要[8]
不仅如此,以上数据都是中期分析的结论(中位随访35.2个月)。考虑到“O+Y”目前表现出的突出应答率、应答持续时间和既往研究中普遍观察到的“长尾效应”,随着随访时间延长,可以期待其长期生存优势还有进一步扩大的空间。
PD-(L)1成为基石后的下一步:变化的环境,与不变的应对
在免疫治疗的竞争进入下半场,“PD-(L)1+”模式的竞争成为主旋律之一的当下,如何才能确保自身的竞争优势?“O+Y“双免组合提供了颇具价值的参考:在不断动态变化的外界环境中,我们仍能总结出一些不变的应对之道。
首先,做好充分的前瞻性布局,才能在转变来临时手握具有确定性的“明牌”,稳健地谋得“先手”;
其次,不止步于现有疗效,不断挑战更高标准:即便是在免疫治疗已成为标准的领域,疗效始终存在进一步提升的空间;
最后,也是最关键的一点:始终将未被满足的临床需求作为突破口:创新药的竞争,归根结底还是洞悉临床需求、满足临床需求的竞争。
参考资料
[1] Cancer incidence and mortality in China, 2022.
[2] Nivolumab (NIVO) plus chemotherapy (chemo) or ipilimumab (IPI) vs chemo as first-line (1L) treatment for advanced esophageal squamous cell carcinoma (ESCC): 45-month (mo) follow-up from CheckMate 648.
[3] https://mp.weixin.qq.com/s/AJ9Xytw2FGEXYxPuYD7FZQ
[4] Anti-CTLA-4 antibodies in cancer immunotherapy: selective depletion of intratumoral regulatory T cells or checkpoint blockade?
[5] Cadonilimab, a tetravalent PD-1/CTLA-4 bispecific antibody with trans-binding and enhanced target binding avidity
[6] Pembrolizumab versus chemotherapy for microsatellite instability-high or mismatch repair-deficient metastatic colorectal cancer (KEYNOTE-177): final analysis of a randomised, open-label, phase 3 study.
[7] Nivolumab (NIVO) plus ipilimumab (IPI) vs chemotherapy (chemo) as first-line (1L) treatment for microsatellite instability-high/mismatch repair-deficient (MSI-H/dMMR) metastatic colorectal cancer (mCRC): Expanded efficacy analysis from CheckMate 8HW.
[8] Nivolumab (NIVO) plus ipilimumab (IPI) vs lenvatinib (LEN) or sorafenib (SOR) as first-line treatment for unresectable hepatocellular carcinoma (uHCC): First results from CheckMate 9DW.

 产业资讯
产业资讯
 E药经理人
E药经理人  2025-07-16
2025-07-16
 43
43

 产业资讯
产业资讯
 识林
识林  2025-07-16
2025-07-16
 41
41

 产业资讯
产业资讯
 胖猫的生命科学札记
胖猫的生命科学札记  2025-07-16
2025-07-16
 42
42