 产业资讯
产业资讯
 药时代
药时代  2024-08-13
2024-08-13
 1569
1569
又一笔出海交易达成。2024年8月9日,默沙东与同润生物宣布,双方就同润生物旗下CD3xCD19双抗CN201达成合作。

根据协定,默沙东将通过子公司引进CN201的全球权益。作为回报,同润生物将获得7亿美元现金预付款,以及最高6亿美元的里程碑付款,交易总额达13亿美元。这笔交易的亮点就是,首付款高。具体而言,7亿美元是中国Biotech出海交易中收到的第二大首付款,仅此于百利天恒。之所以会有如此高的首付款,主要考虑是一次性买断行为,新闻稿中并未提及后续的商业化分成。至于主角同润生物,也成功进入大众视野。
同润生物,对于多数人而言比较陌生,但其背后的药明系,定然耳熟能详。2015年,为了加强投资专业性,药明康德风险投资部门独立出来,更名为毓承资本。2017年,毓承资本与通和资本合并,更名为通和毓承,一举成为医疗健康领域内最大的投资机构之一,李革任董事长,原通和资本创始管理合伙人陈连勇任CEO。而同润生物,这家成立于2018年上海的初创公司,便是由通和毓承孵化而来。公司成立之初,就从淡马锡、通和毓承、博裕资本筹集了1.5亿美元A轮融资。本次交易的CN201,原研为药明生物。CN201采用药明生物WuxiBody双抗技术平台构建,TCR替代CH1和CL,避免轻链错配,根据需要可以采取1:1或2:1价态设计。
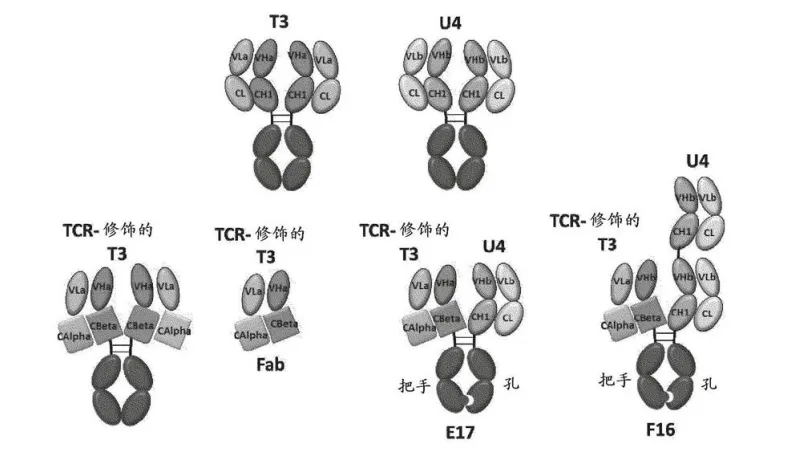
此前,WuxiBody平台已与OBT、Aravive、Almirall等多家海外Biotech达成合作。2023年,GSK一口气从药明生物引进了4款TCE(T cell engager,T细胞衔接器)双抗/多抗产品,交易总金额为15亿美元。其中,首付款为4000万美元。本次交易达成,药明康德作为同润生物大股东的大股东,也可以分上一杯羹。
再看产品数据。
目前,CN201正在进行1期和1b/2期临床试验,分别用于治疗复发或难治性非霍奇金淋巴瘤 (NHL) 和复发或难治性B细胞急性淋巴细胞白血病(R/R B-ALL)。
在今年的ASCO大会上,同润生物公布了CN201用于ALL的早期临床数据。在剂量爬坡至一定水平时,CN201疗效优异。
在目标剂量达到20 mg以上的剂量组,总缓解率达70%以上,且获得缓解的患者90%以上为MRD阴性。
安全性方面,总体CRS发生率不到30%,且以1或2级为主,3级CRS发生率为3.9%,无4级以上CRS发生,目前总共入组51例成人患者,尚未出现ICANS,总体安全性良好。
此外,CN201相较于目前上市的CD3×CD19双抗,如贝林妥欧单抗,还具有良好的依从性。
贝林妥欧单抗在R/R B-ALL治疗中需24h持续静脉输注,共28天,而CN201的输注方法为每周一次,每次持续2-3 h左右。
这里需要注意一点,默沙东理论是不缺TCE多抗开发平台的。
2024年1月,默沙东刚以6.8亿美元的价格收购了Harpoon。通过这次收购,默沙东获得了目前临床中具有前景的DLL3/CD3抗体,以及Harpoon的多个三特异抗体平台。
CN201能被默沙东看中,除了是“野花要比家花香”外,还有一点尤为重要,“拓展自免领域的市场潜力”。
在新闻稿,默沙东实验室总裁 Dean Y. Li 博士表示,“早期临床数据已为CN201靶向和消耗循环和组织B细胞的潜力提供了有力证据,有望治疗一系列恶性和自身免疫性疾病。”
在自免领域,双抗/多抗的布局相对较少,根源仍在于如何达到机制协同的效果,并且满足慢病药物更高安全性门槛的要求。
国内方面,进入临床阶段的自免双抗只有少数几款,包括智翔金泰的TSLP双表位双抗,融捷康生物的IL-4R/IL-5双抗,以及天辰生物、科越医药的补体双功能抗体等。

 产业资讯
产业资讯
 深蓝观
深蓝观  2026-03-31
2026-03-31
 56
56

 产业资讯
产业资讯
 贝壳社
贝壳社  2026-03-31
2026-03-31
 54
54

 产业资讯
产业资讯
 同写意
同写意  2026-03-31
2026-03-31
 56
56