 研发追踪
研发追踪
 抗体圈
抗体圈  2024-09-23
2024-09-23
 3578
3578
2024年欧洲肿瘤内科学会 ( ESMO ) 大会阐明了一系列将重塑肿瘤学领域的变革性进展。今年的活动强调了突破性研究和创新治疗在推进癌症治疗方面的关键作用。那些制药巨头们也在会上带来了产品进展情况,接下来让我们一起来看一下。
默沙东公司四款获批药物和六种在研药物
早期高危三阴性乳腺癌III期KEYNOTE-522研究(#LBA4),高风险局部晚期宫颈癌III期 KEYNOTE-A18研究(#709O),以及不可切除的非转移性肝细胞癌III期LEAP-012研究(#LBA3)被选入大会主席论坛环节。
III期KEYNOTE-522研究首次发布总生存期(OS)数据,评估帕博利珠单抗联合化疗新辅助治疗,并在手术后继续单药辅助治疗用于早期高危三阴性乳腺癌患者。结果显示:帕博利珠单抗可改善高风险早期三阴性乳腺癌 的总体生存率。同样,KEYNOTE-A18 试验数据表明帕博利珠单抗在高风险局部晚期宫颈癌中具有潜力。
其他试验,如 KEYNOTE-006 和 KEYNOTE-811,支持帕博利珠单抗在晚期黑色素瘤和 HER2 阳性胃或胃食管交界处腺癌中的作用。
默沙东还在大会上发布的在研管线数据包括与第一三共公司共同开发的靶向HER3 ADC药物patritumab deruxtecan(HER3-DXd)和ifinatamab deruxtecan (I-DXd,MK-2400),与科伦博泰公司共同开发的在研靶向TROP2抗体偶联物(ADC)药物sacituzumab tirumotecan (sac-TMT,MK-2870/SKB264),以及与Orion公司合作的在研类固醇合成抑制剂opevesostat(MK-5684/ODM-208)。

默沙东官方公众号消息
AbbVie:卵巢癌和 c-Met 过表达实体瘤的新进展
在 ESMO 上,AbbVie 介绍了其 ADC 平台的最新进展,重点关注未满足需求较高的肿瘤类型。他们重点介绍了三种关键药物:mirvetuximab soravtansine、Teliso-V 和 ABBV-400。
Mirvetuximab soravtansine-gynx (MIRV) 是一种针对叶酸受体 α (FRα) 的首创新药偶联物,由抗FRα单克隆抗体、可裂解连接子和美登素衍生物DM4(一种有效的微管蛋白靶向剂)组成,已获得FDA批准用于既往接受过1-3线治疗的铂耐药卵巢癌(PSOC)患者。此次公布的是2期PICCOLO研究,研究结果显示,接受MIRV治疗患者的ORR为51.9%(95% CI 40.4%-63.3%),其中包括6例完全缓解(CR)和35例部分缓解(PR)。DOR为8.3个月(95% CI 5.5-10.8),中位PFS为6.9个月(95% CI 5.9-9.6),OS数据尚未成熟。
Teliso-V 和 ABBV-400(Telisotuzumab Adizutecan)针对的是 c-Met 过度表达的肿瘤,包括非小细胞肺癌 (NSCLC)。c-Met 是一种受体酪氨酸激酶,当被激活时会影响各种细胞信号通路。Teliso-V 对 c-Met 表达高的 EGFR 野生型 NSCLC 患者表现出疗效。AbbVie 计划在 2024 年第三季度提交加速审批申请,预计 2025 年获得 FDA 审查。
ABBV-400是艾伯维筛选了超过400种连接子-载荷后得到c-Met靶向ADC。艾伯维公布了ABBV-400的NCT05029882试验剂量扩展阶段Part2部分入组的2L+ NSQ EGFR WT NSCLC患者的临床数据。
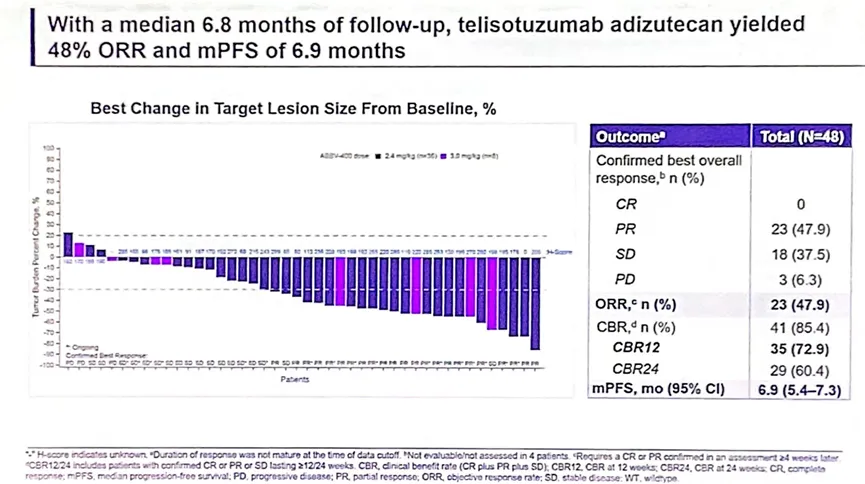
ABBV-400临床结果
结果显示:中位随访时间为6.8个月,ORR为47.9%,中位PFS为6.9个月,中位治疗持续时间为5.6个月。在cMET高表达患者中观察到更优的疗效,在≥25%细胞ICH3+患者和≥50%细胞ICH3+患者中均表现出显著优于2L+ NSQ EGFR WT NSCLC患者(48 pts)的疗效(ORR分别为60.0%和77.8%)。
阿斯利康:非小细胞肺癌脑转移患者疗效获益
阿斯利康公布了TROPION-Lung01研究的NSQ-NSCLC(非鳞状非小细胞肺癌)患者脑转移亚组数据,为Dato-DXd(一种新型的抗体药物偶联物)在晚期经治肺癌合并脑转移患者的疗效提供了进一步的证据支持。以下是对研究结果的总结:
脑转移患者:
中位无进展生存期(PFS):Dato-DXd组为4.9个月,多西他赛组为3.6个月,Dato-DXd降低了41%的疾病进展或死亡风险(HR=0.59,95% CI:0.35-1.00)。
客观缓解率(ORR):Dato-DXd组为30%,是多西他赛组的两倍多。
不伴脑转移患者:
中位PFS:Dato-DXd组为5.7个月,多西他赛组为3.7个月,Dato-DXd降低了36%的疾病进展或死亡风险(HR=0.64, 95% CI:0.50-0.81)。
ORR:Dato-DXd组为31%,多西他赛组为13%。
安全性:
不论是否存在脑转移,Dato-DXd组的总体安全性较多西他赛组更优。
≥3级治疗相关不良事件(TRAE):Dato-DXd组为2%,多西他赛组为8%。
导致减量:Dato-DXd组为12%,多西他赛组为19%。
导致停药:Dato-DXd组为7%,多西他赛组为14%。
这些数据表明,Dato-DXd在治疗晚期经治NSQ-NSCLC患者,无论是否存在基线脑转移,都显示出了显著的疗效和良好的安全性。特别是在脑转移患者中,Dato-DXd不仅展现了令人鼓舞的抗肿瘤活性,而且在安全性方面也表现优异,这为临床治疗提供了重要的参考价值。
百时美施贵宝:长期数据和新试验
百时美施贵宝提交了近 60 篇摘要,其中重点为纳武单抗联合伊匹木单抗(NIVO+IPI)治疗晚期黑色素瘤III期CheckMate 067试验的10年生存结果。经过10年最短f/u后,NIVO+IPI组的中位OS为71.9个月,NIVO组为36.9个月,IPI组为19.9个月。NIVO+IPI v IPI的OS HR为0.53(95%CI 0.44-0.65),NIVO v IPI 的OS HR为0.63(0.52-0.76),不同亚组(包括PD-L1表达和BRAF突变状态)的获益情况一致。CheckMate 067的最终结果继续证明,在含有NIVO的治疗组中,各亚组都能获得持续、长期的生存获益,现在对这些疗法有反应的患者有治愈的可能。
百时美施贵宝还重点介绍了一些新试验,包括一项针对晚期或复发性非小细胞肺癌的 nivolumab 和 relatlimab 的 II 期研究,以及针对广泛期小细胞肺癌的新抗体 BMS-986012。针对去势抵抗性前列腺癌的蛋白质降解剂 BMS-986365 的初步数据也令人鼓舞。
第一三共:肺癌和乳腺癌中的 ADC 发展
第一三共公布了其ADC产品组合的新临床数据,包括datopotamab deruxtecan(Dato-DXd)和靶向 CLDN6 的 ADC DS-9606。
Dato-DXd的TROPION-Lung01研究数据已在上文讲述,因此不再过多赘述。
第一三共首次展示了 DS-9606 的数据,该药物靶向 CLDN6 治疗各种实体肿瘤,其payload非DXd,而是修饰过的PBD。第一三共公布了DS-9606 临床I期初步安全性和有效性数据。有效性方面,在剂量≥ 0.072 mg/kg 时观察到初步疗效,其中有4人有confirmed objective responses(GCT 2人、胃/食管癌和NSCLC各1人)。在 7 名可评估的 GCT 患者中,两名确认客观缓解的患者持续治疗超过6个月。安全性数据显示:爬坡剂量0.016–0.225 mg/kg,无DLT出现。

DS-9606安全性数据
此外,DESTINY-Breast12 试验还揭示了 ENHERTU 对 HER2 阳性乳腺癌的有效性。DESTINY-Breast12是一项3b/4期、开放标签的多中心研究,旨在评估ENHERTU在既往接受过治疗的HER2阳性晚期乳腺癌患者中的疗效和安全性,无论患者是否存在脑转移(BM)。在BM队列中,12个月PFS率为61.6%(95%CI,54.9-67.6),而12个月的中枢神经系统(CNS)PFS率为58.9%(95%CI,51.9-65.3)。稳定性BM患者的CNS ORR为79.2%(95%CI,70.2-88.3),而活动性BM患者的CNS ORR为62.3%(95%CI,50.1-74.5)。研究结论表明,ENHERTU在HER2+转移性乳腺癌患者中(包括稳定性和活动性BM的大型队列)显示出持久的总体和颅内临床活性,并且未发现新的安全性信号。

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 566
566

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 479
479

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 504
504
 热门资讯
热门资讯