 研发追踪
研发追踪
 Insight数据库
Insight数据库  2025-01-06
2025-01-06
 4718
4718
当地时间 12 月 30 日,Axsome Therapeutics 宣布,其 AXS-05(右美沙芬+安非他酮)在治疗患有躁动症的阿尔茨海默病(AD)患者的 III 期 ACCORD-2 研究中达到主要终点。与安慰剂相比,AXS-05 显著延迟了 AD 患者躁动复发时间,同时降低了 AD 总体严重程度的恶化。
Axsome 计划在 2025 年下半年递交AXS-05 治疗 AD 躁动的上市申请。

来源:Axsome 官网
AXS-05 采用右美沙芬和安非他酮的专有配方、剂量,以及 Axsome 代谢抑制技术来调节成分的输送,被开发用于治疗阿尔茨海默病躁动和戒烟。右美沙芬是一种口服 NMDA 受体拮抗剂、sigma-1 受体激动剂,安非他酮是一种去甲肾上腺素和多巴胺再摄取抑制剂,可提高右美沙芬的生物利用度。
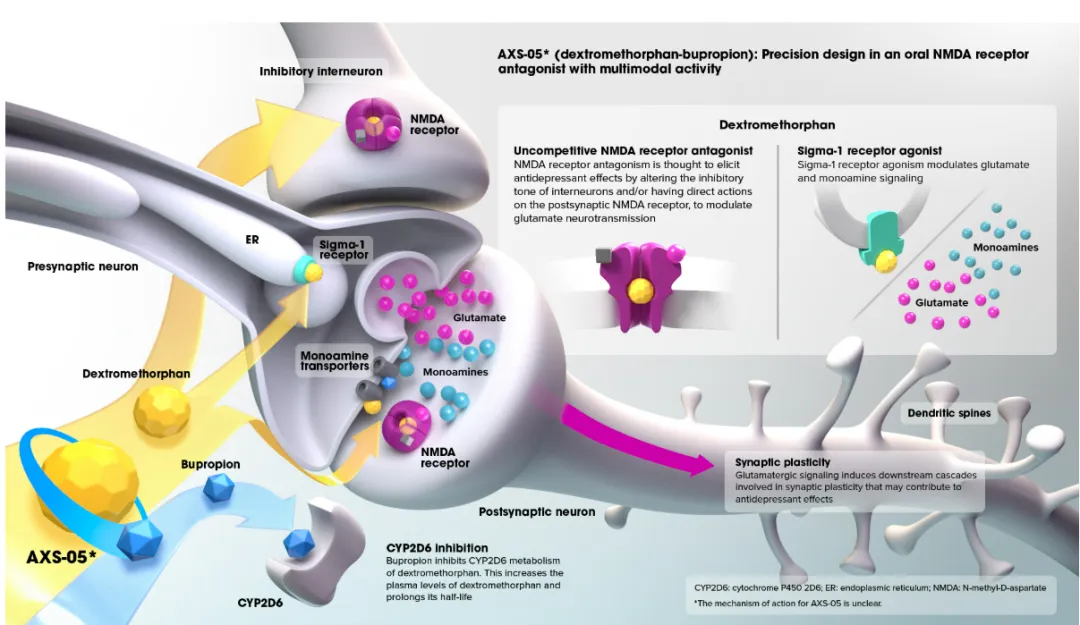
来源:Axsome 官网
ACCORD-2 研究是一项双盲、安慰剂对照、随机停药的 III 期临床试验,包括开放标签和随机双盲治疗期。
开放标签治疗期共有 295 名患有躁动症的 AD 患者接受了长达 12 个月的治疗,基线时,平均柯恩-曼斯菲尔德躁动量表(CMAI)总分为 73.3。结果显示,接受 AXS-05 治疗第 6 周 :
受试者 CMAI 总分较基线平均下降 20.4 分,较平均基线分数下降 46%。
69% 患者实现了临床应答(定义为较基线减少≥30%)。
使用临床医生评定的改良版阿尔茨海默病合作研究-临床总体印象变化 (mADCS-CGIC) 进行评估,78% AD 患者躁动症状得到改善。
随机双盲治疗期,共有 167 名患者纳入研究,随机分组接受 AXS-05(n=83)和安慰剂(n=84)治疗,平均 CMAI 总分分别为 44.3 分和 45.4 分。结果显示:
主要终点方面,与安慰剂相比,AXS-05 显著延迟了 AD 躁动的复发时间,复发风险降低 3.6 倍。
关键次要终点方面,与安慰剂相比,AXS-05 显著降低了 AD 患者躁动的复发率,AXS-05 复发率为 8.4%,安慰剂为 28.6%。
安全性方面, AXS-05 组不良事件发生率为 29.3%,安慰剂组为 32.1%。AXS-05 组有两名受试者(2.4%)跌倒,其中只有一名被认为与研究药物有关。因不良事件而停药的人数很少(AXS-05 为 0%,安慰剂为 1.2%)。
不过,AXS-05 另外一项 III 期 ADVANCE-2 研究未达到主要终点。ADVANCE-2 是一项双盲、安慰剂对照、平行分组的 III 期临床试验,旨在评估 AXS-05 对患有躁动症的 AD 患者的疗效,共入组 408 名受试者,按 1:1 的比例随机接受 AXS-05 或安慰剂治疗,治疗期为 5 周。
结果显示,治疗 5 周后,AXS-05 组和安慰剂组从基线到第 5 周 CMAI 总分分别减少了 13.8 分和 12.6 分,不具有统计学意义。但主要终点和几乎所有次要终点, AXS-05 均优于安慰剂组。
AXS-05 治疗患有躁动症的 AD 患者的III期综合临床开发计划包括 4 项,具体如下。AXS-05 在治疗 AD 躁动方面的长期安全性已在超过 300 名接受治疗至少 6 个月的患者和超过 100 名接受治疗至少 12 个月的患者中得到证实。
ADVANCE-1 研究达到主要终点 (p=0.010)
ADVANCE-2 研究主要终点无统计学意义
ACCORD-1 研究达到主要终点 (p=0.014)
ACCORD-2 研究达到主要终点 (p=0.001)
Axsome 计划根据上述研究的疗效和安全性数据,在 2025 年下半年向 FDA 提交 AXS-05 治疗 AD 躁动症的新药上市申请。此前,AXS-05 已被授予治疗阿尔茨海默病躁动症的突破性疗法认定。

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 560
560

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 472
472

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 500
500
 热门资讯
热门资讯