 产业资讯
产业资讯
 医药魔方Pro
医药魔方Pro  2025-02-25
2025-02-25
 1794
1794
2月18日,多域生物宣布授予Photys Therapeutics靶向IRAK4的蛋白降解剂HPB-143的开发、生产和商业化全球(大中华区和东南亚除外)独家许可[1]。
虽然交易金额尚未披露,但根据协议条款,多域生物除获得首付款和里程碑付款外,还将持有Photys Therapeutics的部分股权,这种策略与当前NewCo出海模式中锁定后期价值的做法不谋而合。
放眼全球,尽管PROTAC领域已吸引了200余家企业布局,但近两年达成的BD交易却屈指可数。此次交易的达成,不仅彰显了国际市场对中国PROTAC药物研发实力的认可,更为近期相对低迷的PROTAC市场注入了新的发展动能。
值得深入探讨的是,多域生物的HPB-143究竟具备哪些独特的竞争优势?Photys Therapeutics为何选中自免PROTAC?这些问题的答案,或许能为我们揭示中国创新药企在全球竞争格局中的新机遇。
挑战“明星项目”:实力显现

自2001年耶鲁大学教授Craig
Crews团队提出PROTAC概念以来,该领域已蓬勃发展了二十余年。医药魔方Nextpharma®数据库显示,全球在研的PROTAC药物超过450种,其中约87%集中在肿瘤治疗领域,但PROTAC的应用潜力远不止于此。
全球PROTAC管线的TOP10适应症(来源:医药魔方NextPharma®数据库)
在全球PROTAC管线中,自免疾病成为了一个新的重要战场,多域生物的HPB-143就是这一领域的代表性产品。
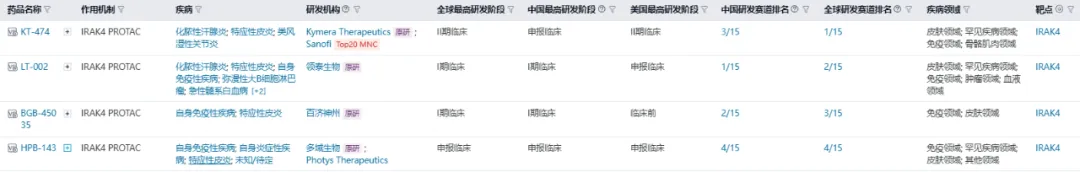
医药魔方Nextpharma数据库®显示,全球共有25款针对自免疾病的PROTAC分子,主要集中在IRAK4、JAK、BTK等靶点。其中,4款药物已进入临床阶段,进展最快的为赛诺菲和Kymera Therapeutics合作开发的IRAK4 PROTAC——KT-474,目前处于II期临床阶段。
临床阶段的自免PROTAC分子(来源:医药魔方NextPharma®数据库)
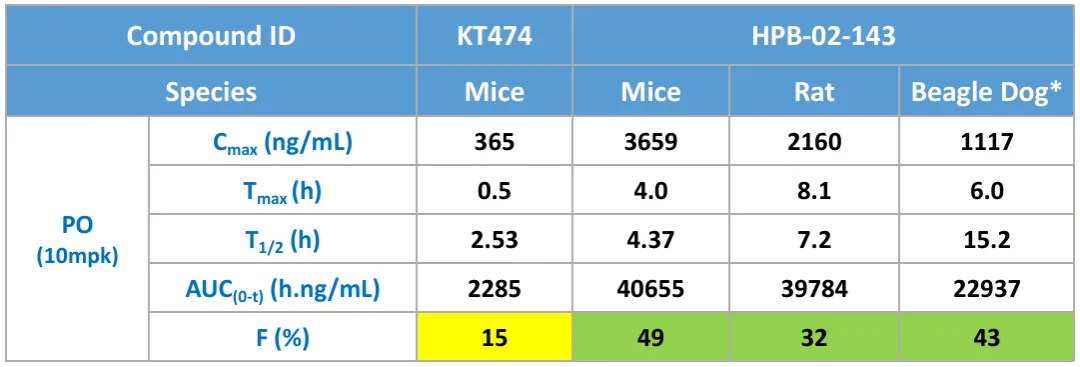
2024年10月,多域生物公布了HPB-143的临床前数据[2],与处于临床II期的KT-474相比,HPB-143展现出更高的口服给药生物利用度(小鼠中达49%)和对心脏离子通道hERG的较弱抑制(hERG IC50>10μM)。
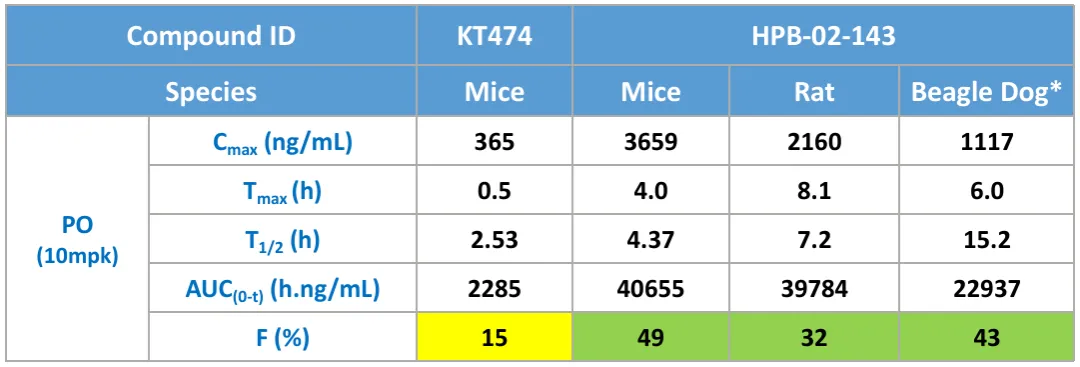
HPB-143与KT-474的药代动力学数据(来源:多域生物官网)
此外,在多种小鼠疾病模型中,HPB-143不仅起效剂量更低,而且药效更优,与KT-474相比显示出显著优势,这或许也是Photys Therapeutics选择HPB-143的重要原因。
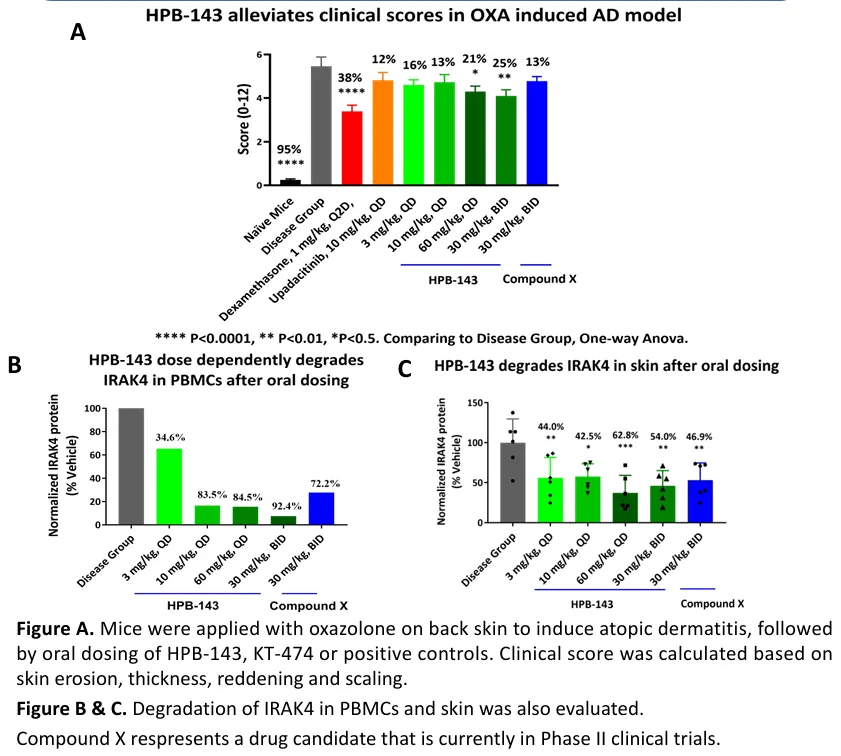
特应性皮炎模型中,HPB-143与KT-474的药效学数据(来源:多域生物官网)
多域生物成立于2018年,致力于开发first-in-class和best-in-class的新药项目,特别是在癌症、自免疾病和抗衰老等领域。
除了这款靶向IRAK4的PROTAC(HPB-143),多域生物还布局了国内首个FLT3/IRAK4双靶点抑制剂HPB-092,其临床研究申请已于2024年9月获FDA批准,即将开展治疗急性髓性白血病(AML)的I期临床研究。
一个月后(2024年10月),多域生物第二款创新分子——IRAK4 PROTAC HPB-143再次获得FDA批准,用于治疗自免疾病。2025年2月,HPB-143在国内的IND申请也顺利获批,计划用于治疗特应性皮炎等自免和炎症性疾病。
此外,多域生物还有两款临床前药物,分别是针对EGFR exon 20的抑制剂,以及靶向KRAS G12C的PROTAC。
降解剂和抑制剂珠联璧合,恰好印证了其管线布局策略——药化平台以人工智能和结构生物学为基础,打造具有生物活性的靶点抑制剂分子和靶点降解剂分子。
新CSO上任三把火
Biotech公司的创新很多源自大学科研人员的智慧结晶。在探索异双功能分子的新用途时,Longwood Fund基金负责人Lizzie Ngo发现了一篇来自Broad研究所Amit Choudhary团队的突破性论文。
该论文阐述了一种名为磷酸化诱导嵌合小分子药物(PHICS)的新技术,其与PROTAC技术相似,均通过诱导接近原理发挥作用,但PHICS通过连接激酶配体(而不是PROTAC中的E3连接酶配体)与靶蛋白配体,促进特定激酶对靶蛋白的磷酸化,从而修复功能失调的蛋白,满足特定疾病的治疗需求。
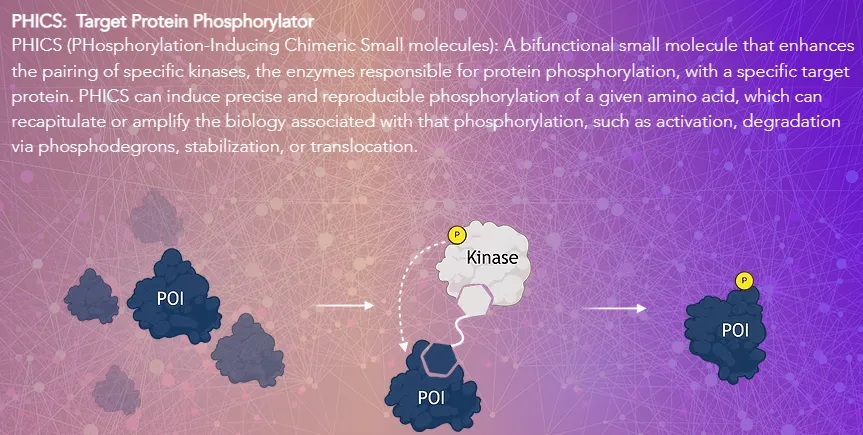
PHICS机制(来源:Photys官网)
这一发现促成了Longwood基金与Amit Choudhary博士的合作,双方于2021年联合创立了Photys Therapeutics。然而,在2022年9月完成7500万美元A轮融资后,Photys Therapeutics却意外地进入了沉寂期,逐渐淡出了行业视野。
转机出现在2024年10月,新任首席科学官(CSO)Alexandra Joseph博士上任后,迅速为Photys Therapeutics燃起了“三把火”,为Photys Therapeutics注入了新的活力:
2024年12月,Photys Therapeutics宣布与诺和诺德达成合作,开发治疗心脏代谢疾病的PHICS分子,交易总金额为1.86亿美元;
2025年2月,公布其基于tPRIME(靶蛋白转录调节因子)技术的p53-Y220C-BET双功能小分子在体外和体内驱动癌细胞死亡的最新数据,该技术在体外和体内实验中均展现出显著的癌细胞杀伤效果[3]。基于这一突破性进展,Photys Therapeutics正式将tPRIME平台纳入公司技术矩阵;
2025年2月,获得多域生物靶向IRAK4的蛋白降解剂HPB-143的开发、生产和商业化全球(大中华区和东南亚除外)独家许可,以加强PROTAC管线。
至于为何要收购多域生物的自免PROTAC分子,答案或许隐藏在Alexandra Joseph的工作经历中。公开资料显示,Alexandra Joseph博士在赛诺菲有着近17年的工作经历,担任免疫学和炎症研究治疗领域的投资组合和运营负责人。

Alexandra Joseph的部分工作经历(来源:LinkedIn)
上文提到,目前全球进展最快的自免PROTAC分子KT-474是由赛诺菲和Kymera Therapeutics合作开发的,Alexandra Joseph又是赛诺菲免疫学领域的相关负责人,所以主导Photys Therapeutics收购多域生物的自免PROTAC分子也不足为奇了。
PROTAC:进军自免赛道
作为全球进展最快的自免PROTAC,赛诺菲和Kymera Therapeutics早在2023年12月就在Nature Medicine杂志公布了KT-474在中重度特应性皮炎(AD)和化脓性汗腺炎(HS)患者中研究了靶向IRAK4的蛋白降解剂KT-474的安全性、耐受性、药代动力学(PK)和药效(PD)特征以及临床活性[4]。
I期临床试验(NCT04772885)的结果初步证实,KT-474在治疗炎症性皮肤疾病方面具有潜力,标志着蛋白降解领域向非肿瘤疾病的扩展迈出了重要一步。另外,针对HS和AD的KT-474的II期临床试验也正在进行中。
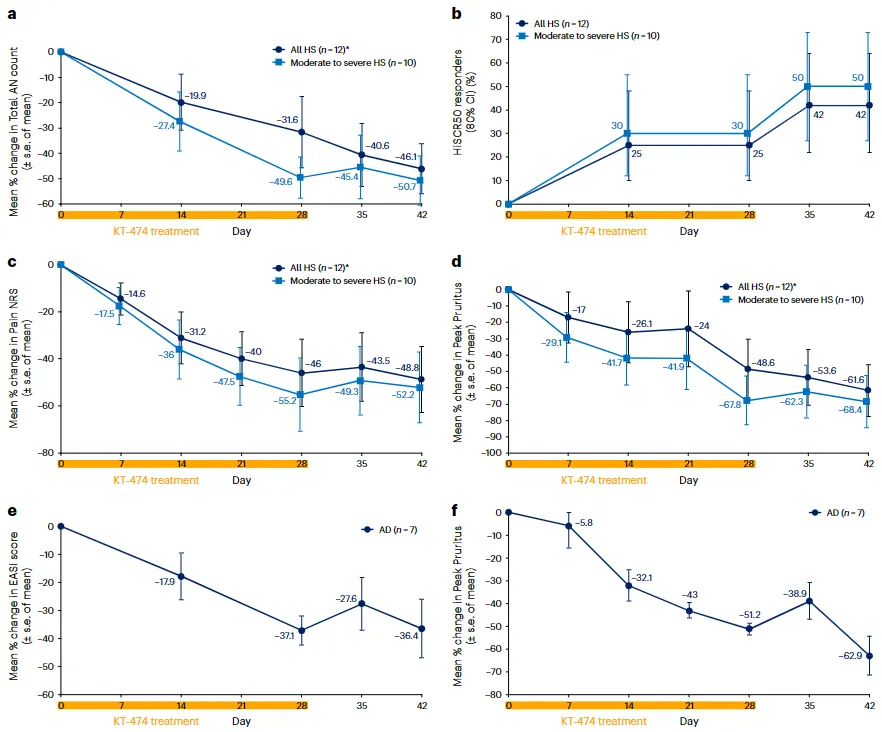
HS和AD患者对KT-474的临床反应[4]
为了加速KT-474的临床开发进度,赛诺菲在2024年7月宣布扩大以上两项临床研究的入组规模,可见对于KT-474抱有极大期望。
此外,领泰生物的IRAK4 PROTAC分子LT-002在中美均已获批进入临床研究,用于治疗自免疾病;百济神州在2023年末公开了IRAK4 PROTAC专利,2024年8月,IRAK4 PROTAC分子BGB-45035在国内获批临床,拟开发治疗中重度特应性皮炎。
迄今为止,针对IRAK4靶点的药物尚未问世,这一领域仍然是一片蓝海。与传统的小分子抑制剂相比,PROTAC技术展现出其独特的优势,它能够彻底降解IRAK4蛋白,不仅抑制其激酶活性,还能破坏其支架结构的功能。这种双重作用机制在理论上有望带来更为全面和高效的作用,为自免疾病的治疗提供了新的策略。
在全球范围内,自免药物市场正呈现出前所未有的热度,2024年并购交易规模创历史新高。除了传统小分子、单抗药物,CAR-T、双抗等前沿技术已成为自免赛道的新生力量。以IRAK4 PROTAC为代表的自免PROTAC项目也正逐渐成为业界关注的焦点。自免掘金热潮下,PROTAC技术究竟能够焕发怎样的光彩,静待更多临床数据的揭晓。
参考资料:
[1]https://mp.weixin.qq.com/s/F1Ns4my58yOjAWS93AcU1w
[2]https://www.polymedbiopharma.com/upload/File/20241014/6386449329080537909333283.pdf
[3]https://www.photys.com/_files/ugd/8c4eaf_04e219baf9864bbaa8b4fb3d462d883c.pdf
[4]https://www.nature.com/articles/s41591-023-02635-7.pdf
 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-05-07
2026-05-07
 135
135

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2026-05-07
2026-05-07
 165
165

 产业资讯
产业资讯
 药渡
药渡  2026-05-07
2026-05-07
 149
149
 热门资讯
热门资讯