 研发追踪
研发追踪
 药视点
药视点  2025-03-17
2025-03-17
 3521
3521
近日,Beam Therapeutics公布实验性基因编辑疗法BEAM-301的首批临床试验数据。该疗法针对罕见遗传病α1-抗胰蛋白酶缺乏症(AATD),目前已在9名患者身上测试,数据显示该疗法可以降低突变蛋白水平并提高正常蛋白水平。这是全球首次利用碱基编辑技术直接纠正致病突变的临床结果,同时也是Beam在体内基因编辑(in vivo)领域的首个临床试验数据。

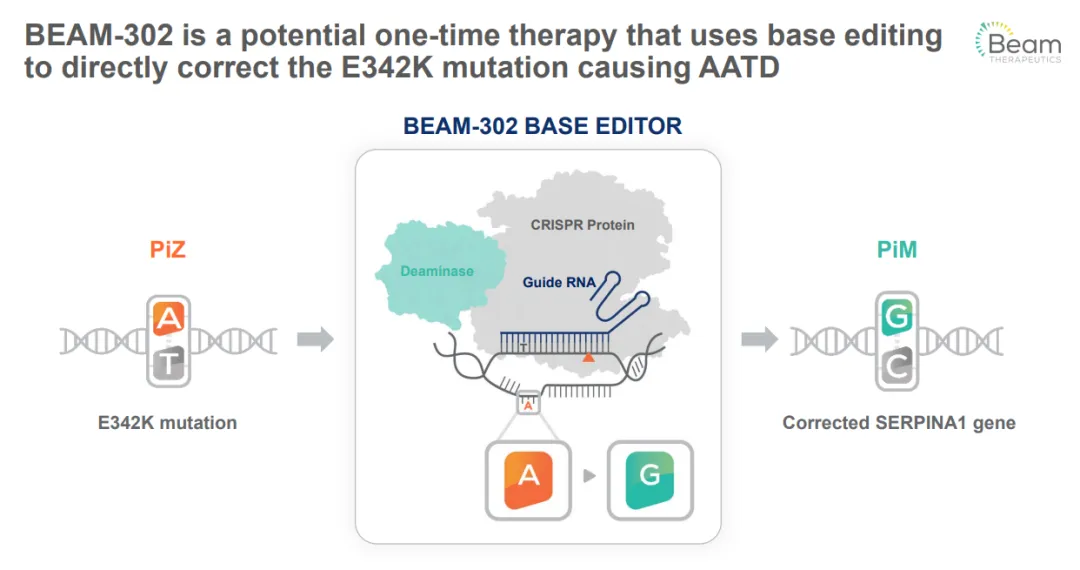
AATD是一种由SERPINA1基因突变导致的罕见遗传病,受影响的人体内无法生成正常水平的α1-抗胰蛋白酶(AAT),这是一种由肝脏合成的蛋白质,主要作用是保护肺部免受炎症损伤。由于蛋白质异常,AATD患者导致早发性肺气肿和肝病,BEAM-302是一种针对肝脏的脂质纳米颗粒(LNP)配方,内含指导RNA(gRNA)和编码碱基编辑器的mRNA,旨在修正致病的PiZ突变。携带该突变纯合子的患者,其血液循环中功能性AAT蛋白水平极低,且全部为突变型(称为Z-AAT),该突变蛋白会积聚并引起肝脏毒性。
通过在DNA水平上修正PiZ突变,BEAM-302有望成为一次性治疗方法,既能降低循环中Z-AAT的含量,又能产生具有治疗水平的修正蛋白(M-AAT),并将血液循环中总AAT及功能性AAT提高至超过11 µM的保护阈值,从而解决肝病和肺病的基础病理生理问题。
实验数据表明:该疗法可以降低突变蛋白的水平,减少其在肝脏中的有毒积累。同时,它还可以增加正常α1-抗胰蛋白酶的生成,恢复肺部保护功能,首次人体试验结果呈现剂量依赖性效果。
Beam目前在英国、新西兰、澳大利亚和荷兰开展I/II期临床试验,共测试了3个剂量水平(15mg、30mg、60mg),每组有3名患者,总计9名患者接受治疗。
15mg剂量组:突变蛋白减少11%
30mg剂量组:突变蛋白减少38%
60mg剂量组:突变蛋白减少78%(单个患者数据)
治疗3天内,即可检测到正常AAT蛋白的增加,并且随着剂量增加,AAT蛋白水平提升更明显。从这些数据可以看出,该疗法呈现剂量依赖性,即较高剂量可更有效降低突变蛋白,并增加正常蛋白。
在安全性方面,Beam表示未出现严重不良事件(SAE),仅观察到1级(轻度)肝酶升高,且这些患者无临床症状。这一结果令人鼓舞,因为此前Verve Therapeutics曾因安全问题终止了其基因编辑临床项目,而Beam的技术似乎未出现类似问题。
Beam的竞争对手Intellia Therapeutics今年早些时候已停止AATD基因编辑项目,而RNA编辑公司(如Wave Life Sciences和Korro Bio)仍在开发基于RNA编辑的AATD疗法,但尚未进入临床。相比之下,Beam的技术更接近实际应用。
免责声明:本公众号专注介绍全球生物医药健康研究进展,仅作信息分享,不代表药视点立场和观点。本文仅作信息交流之目的。文中图片、视频、字体、音乐等素材取自各大公司官网/网络,版权归拥有者,药视点尽力注明来源。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
原文:

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-05-18
2026-05-18
 345
345

 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2026-05-18
2026-05-18
 410
410

 研发追踪
研发追踪
 药研网
药研网  2026-05-18
2026-05-18
 326
326
 热门资讯
热门资讯