 产业资讯
产业资讯
 医药魔方
医药魔方  2025-07-01
2025-07-01
 1337
1337
继首季度盈利之后,近日举办的投资者研发日活动让百济神州又一次站在聚光灯下。
全新的管线布局再次验证,百济神州的研发底蕴足够深厚。在泽布替尼已长成全球大单品之际,血液瘤领域的下一次胜利也在酝酿之中,索托克拉已经申报上市,实体瘤领域孵化的一系列待爆潜力分子有望在今年斩获多个概念验证(POC)里程碑。
透过管线布局释放的一个更深层信号是,百济神州正在向全球肿瘤药巨头迈进,它在用MNC的体系与打法持续创新输出,用全球化的能力去托举全球化的愿景。
血液瘤领域的下一次胜利
百济神州在血液肿瘤领域找准锚点,聚焦细分市场大、增长快的CLL并持续深耕,成为了唯一一家在3个CLL基础作用机制中均拥有潜在BIC产品的公司。

泽布替尼的成功已无须多言。尽管在美国市场上未占据先机,尤其是在CLL适应症分别比伊布替尼和阿可替尼晚获批9年和3年的情况下,泽布替尼仍实现了赶超。这一成功的核心逻辑在于,锁定“大药”品种并基于BIC理念进行分子迭代。泽布替尼只是开始,百济神州血液瘤的上市产品格局即将焕新,新王牌索托克拉已在华申报上市,并预计在今年下半年推进全球申报。
作为新一代BCL-2抑制剂,索托克拉正试图复制泽布替尼的成功路径。相较于维奈克拉,索托克拉的药效提高了14倍、选择性提高了6倍,以及半衰期也明显缩短。分子设计上的优化将转化为更好的疗效、安全性和用药便利性。
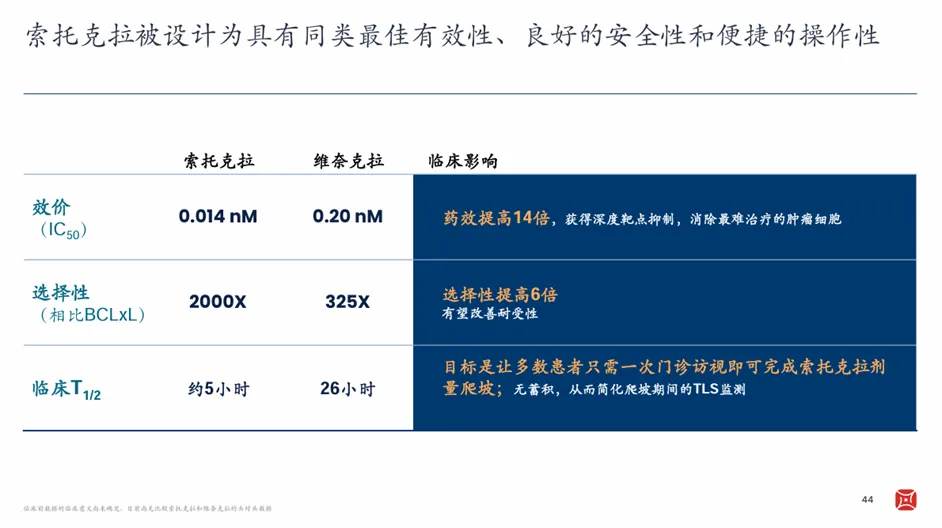
两子落下,百济神州布局的高明之处就显露出来了,它并不局限于单兵作战的思维,而是在单药足够强的基础上打出更强的组合拳。现有临床数据提示,全口服索托克拉+泽布替尼在初治CLL/SLL或复发/难治性(R/R)CLL/SLL等多种血液瘤中均展现出深度且持久的缓解效果,有望成为最佳联合治疗方案。基于这些积极结果,百济神州已开启3项头对头全球III期临床。
如果说索托克拉代表着百济神州在血液瘤领域的一次横向扩张,那么BTK CDAC药物BGB-16673则是其推进纵深布局的落子,有望克服传统BTK抑制剂的耐药性问题,同时也意味着百济神州有能力打造更稀缺的FIC药物了。
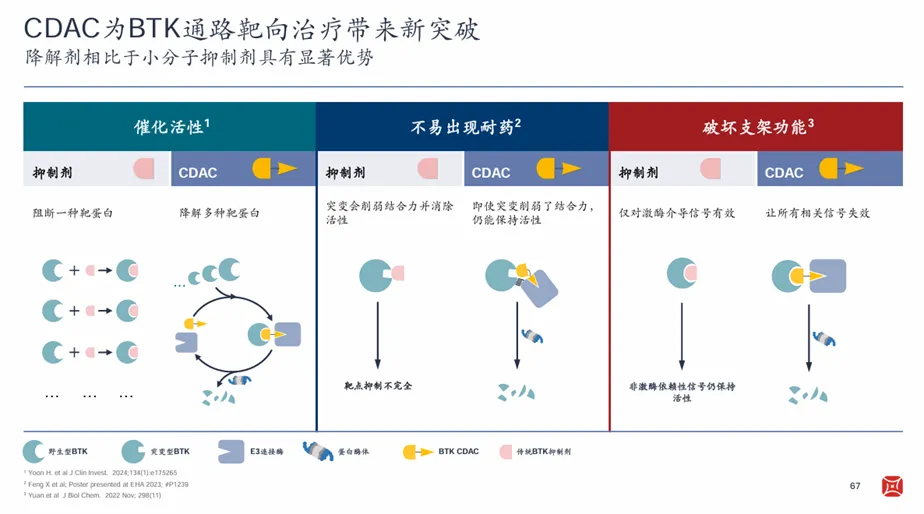
开发FIC分子是风险最高的一条创新药开发路径。但从现有数据上看,BGB-16673的成药已经具有一定的确定性。I期CaDAnCe-101研究显示,BGB-16673在R/R
CLL、R/R WM、R/R
FL、MZL患者中的ORR分别为84.8%、84.4%、41.7%、50%,并在预后极差的Richter's转化患者中观察到缓解。也就是说,BGB-16673的适应症范围可能相当广阔。
优效性验证的临床开发思路也在BGB-16673身上得到体现。瞄准既往接受过共价BTK抑制剂治疗的R/R CLL/SLL患者,百济神州启动了BGB-16673对比匹妥布替尼的全球III期CaDAnCe 304研究。
上述三大主力将奠定百济神州在血液瘤领域的基本盘,未来还将有更多新疗法助力百济神州扩大版图,包括T细胞衔接器(TCE)、细胞疗法和巨噬细胞衔接器。在TCE赛道,百济神州已有一些差异化早期资产储备,CD19/CD20/CD3三抗、BAFFR/CD22/CD3三抗和CD20/CD28双抗均已推进至IND阶段。
实体瘤实力来到重估时刻
在血液瘤持续高光之外,百济神州在实体瘤领域也悄然织就了层次分明的布局网络,即将上演一场多赛道同时发力的接力突围赛。竞赛背后,是百济神州战略纵深与执行力的显露,其被低估的实体瘤实力也将来到重估时刻。
百济神州在实体瘤的故事由替雷利珠单抗领衔讲述。故事的开端并不算惊艳——作为PD-1赛道的后来者,替雷利珠单抗面对的是已被K药、O药占据主要份额的市场格局。然而,百济神州依然稳扎稳打地展开了替雷利珠单抗的实体瘤版图扩张之路。替雷利珠单抗的适应症拓展效率令人瞩目,自2019年末获批上市至今已经覆盖尿路上皮癌、非小细胞肺癌、肝细胞癌等10大类癌种。
更具战略意义的是其全球化能力的验证。迄今为止,替雷利珠单抗已在欧洲获批7项适应症、美国获批3项适应症,海外落地广度仅次于K药和O药。这不仅是商业版图的扩张,更是百济神州全球临床开发与注册能力的硬核验证。
在PD-1疗法覆盖范围的边界之外,百济神州正在构建更加多元化的治疗矩阵。HER2双抗泽尼达妥单抗于上个月在中国获批上市,直指HER2阳性实体瘤群体尚未满足的临床需求。
真正的突围力量,藏在更深层的管线孵化中。百济神州有侧重地在肺癌、乳腺癌/妇科癌症和胃癌三大治疗需求强烈的肿瘤领域,培育了一系列高度差异化的潜力分子。
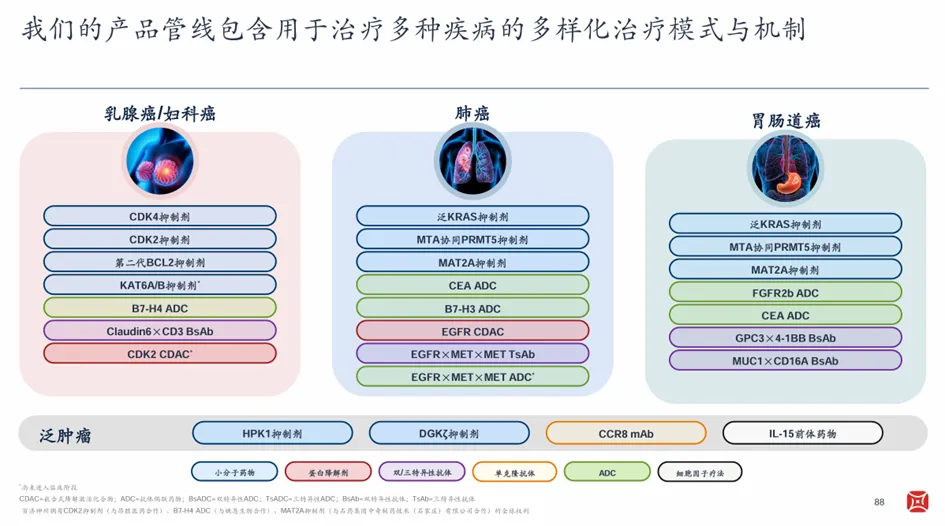
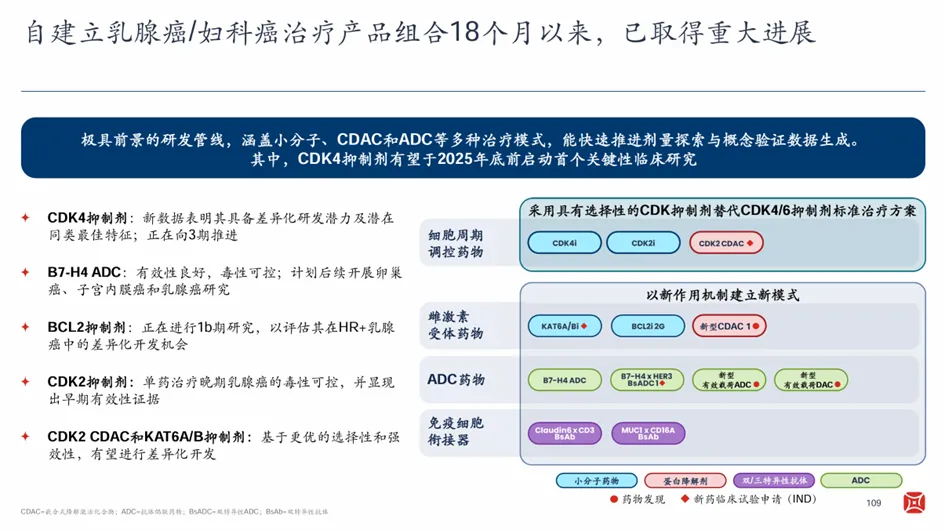
在乳腺癌/妇科癌症领域,百济神州的布局呈现出“精准打击”的特点。针对HR+/HER2-乳腺癌人群的治疗痛点,百济神州在CDK靶点上进行了多层次布局,高选择性抑制剂与强效降解剂并行开发,双管齐下解决CDK4/6抑制剂的耐药及血液学安全性问题。
率先完成POC的BGB-43395(CDK4抑制剂)已经在早期研究中展现出良好的耐受性、药效学性质及明确的临床反应,具有潜在同类最佳血液学安全性特征。待剂量优化随机化扩展阶段的数据读出后,BGB-43395将在下半年进入III期阶段。
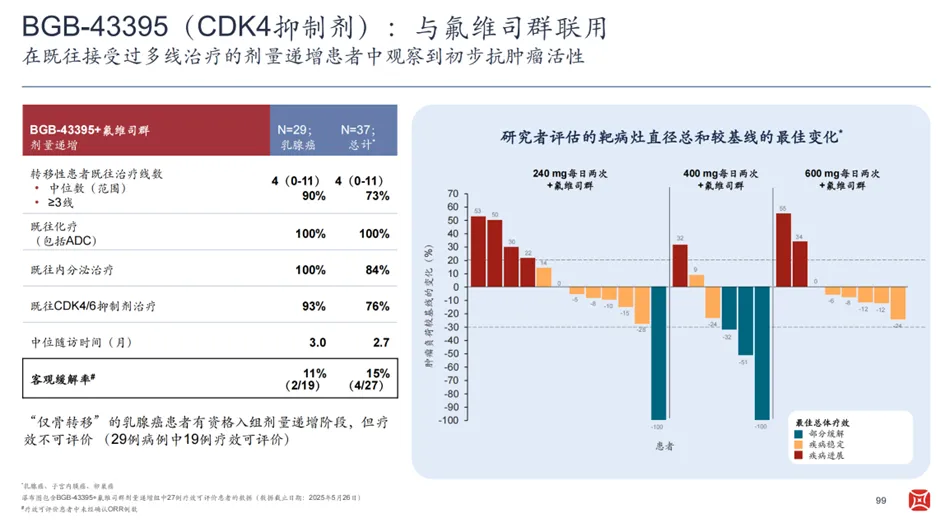
BG-68501(CDK2抑制剂)同样在早期研究中展现出可控的安全性和初步抗肿瘤活性,在剂量递增至200mg时仍未观察到剂量限制性毒性(DLT),疾病控制率为51.5%(17/33)。在相同的布局逻辑下,百济神州还开发了选择性更优且更加强效的CDK2降解剂BF-75098,该分子将在年底前进入临床。
BG-C9074(B7-H4 ADC)在首个人体研究中展现了初步疗效,经确认的客观缓解率(cORR)为24%,其中6mg/kg剂量组的cORR达到了43%。从生物标志物的结果来看,BG-C9074对B7-H4较高表达肿瘤患者的获益更加明显。基于此,百济神州将在今年Q3开放乳腺癌和妇科恶性肿瘤的肿瘤特异性扩展队列,以进一步确认BG-C9074在B7-H4高表达肿瘤患者中的疗效和安全性。
在肺癌领域,百济神州正在打造行业领先的产品组合。BGB-58067(PRMT5抑制剂)和BG-89894(MAT2A抑制剂)在单药剂量递增研究阶段未出现DLT,有少数患者在早期即开始实现客观缓解。值得一提的是,百济神州在肺癌领域再次展现了管线布局的全面性和前瞻性——唯一一家在PRMT5和MAT2A两大肺癌高潜力靶点同时拥有临床阶段项目的公司。
在胃癌领域,百济神州注重创新生物学机制的探索,尤其是对RAS通路的深度开发。围绕RAS通路,百济神州开发了泛KRAS抑制剂、KRAS CDAC、RAS(ON)抑制剂等药物,其中KRAS CDAC在临床前研究中实现了对KRAS的近乎完全降解,将在2026年下半年进入临床。

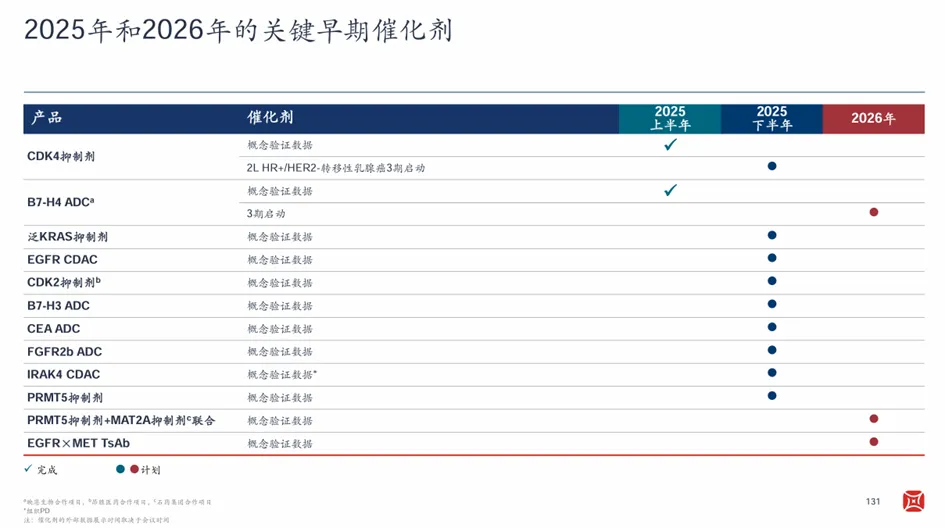
接下来半年的时间窗口对百济神州实体瘤管线具有关键意义——8个POC里程碑将陆续达成,包括BG-T187(EGFR/MET三抗)、BG-60366(EGFR
CDAC)、BG-C137(FGFR2b ADC)等药物。这些潜力分子的涌现,让百济神州的靶点挖掘、机制探索和技术创新能力更加具象化了。
向全球肿瘤药巨头迈进
审视百济神州的研发管线,无论是血液瘤的持续进化,还是实体瘤的多元迸发,其布局的广度(覆盖主要癌种)与深度(FIC/BIC潜力分子涌现)已具备全球肿瘤巨头的发展态势。不过,管线布局仅是冰山显露的一角,真正的蜕变发生在最底层的研发体系重构。
所有体系的构建与演进都立足于团队建设。百济神州的研发团队高产且能力成熟。其中,临床前团队汇聚1200+科研人员,是全球最大的专注于肿瘤药物发现的团队之一。在临床前团队的协作下,百济神州的临床前项目规模已经扩大到82项。规模跃迁的同时,百济神州也在不断推进技术平台的创新升级,CDAC、ADC、双抗/多抗等平台高效运转,持续为管线的深度布局赋能。
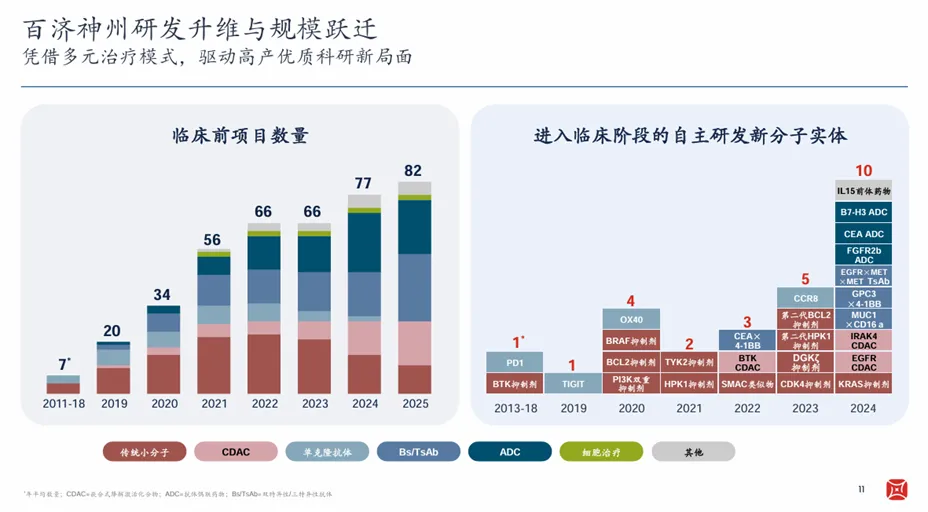
当然,如果单纯追求管线数量的增长,那么就很容易陷于同质化的内卷之中。事实上,百济神州对于临床前项目的评估相当严苛,未达其标准就终止。三年半时间,百济神州已终止60+临床前项目,体现了其对资源配置效率的重视。
临床开发团队从2013年开始搭建,如今规模达3700+员工,精细化覆盖多种职能。这支团队给百济神州带来了真正意义上的全球临床开发能力,完全摆脱了CRO依赖,自主推进96项临床试验,涉及30款临床产品。在具体执行中,百济神州始终坚持多区域覆盖的全球入组策略,不仅保证了患者人种的多样性,也能触达特定的难招募人群,从而兑现对全球患者的承诺。
POC阶段,百济神州强调效率至上,比如剂量递增队列平均用时仅7.1周;确定推荐剂量后,启动剂量扩展平均用时4.4周。未来它还将利用自动化和AI技术,最大限度提升临床试验效率。
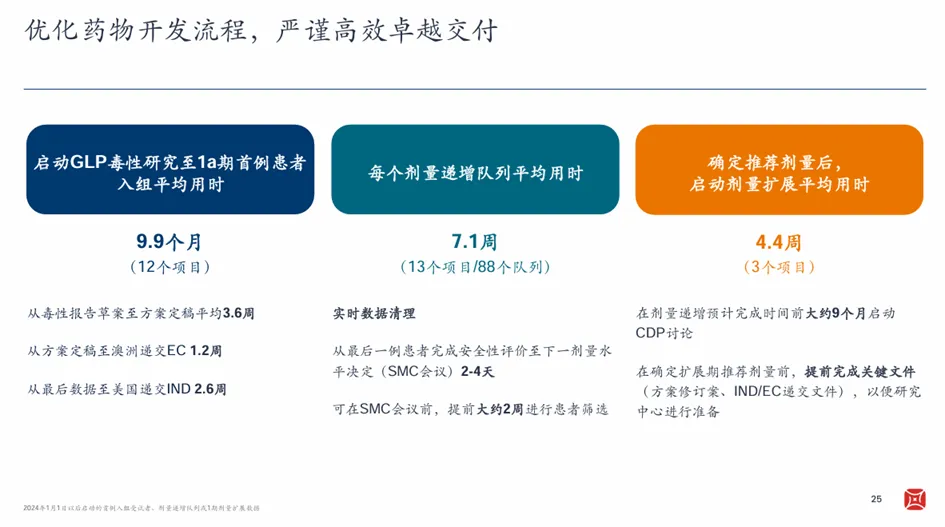
依托于强大的全球研发组织架构,百济神州在管线开发上创造了时间、成本及质量等优势,显著压缩了创新药研发周期,并能够并行推进数十个高复杂度项目,确保更多“接力赛”能顺利进行。
从血液瘤的全面开花到实体瘤的多点突破,百济神州正在用实际行动诠释什么是真正的全球肿瘤治疗创新公司。在这个过程中,它不仅在产品层面接续实现突破,更重要的是在体系能力上完成了蜕变。当下一个重要节点到来时,这些积累将成为百济神州在下一个5年、10年继续跃迁,并最终跻身全球顶尖制药企业行列的关键支撑。

 产业资讯
产业资讯
 同写意
同写意  2026-03-18
2026-03-18
 42
42
 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-03-18
2026-03-18
 38
38

 产业资讯
产业资讯
 赛柏蓝器械
赛柏蓝器械  2026-03-18
2026-03-18
 38
38