 产业资讯
产业资讯
 正大天晴药业集团
正大天晴药业集团  2025-07-05
2025-07-05
 1213
1213
首个国产重组人凝血因子Ⅶa类生物制品获批上市!7月3日,正大天晴收到国家药品监督管理局(NMPA)核准签发的《药品注册证书》,批准注射用重组人凝血因子Ⅶa N01用于凝血因子Ⅷ或Ⅸ抑制物>5个Bethesda(BU)单位的成人及青少年(12岁以上)先天性血友病患者的出血治疗。

独特凝血机制助力临床获益 首家国产七因子上市提升药物可及性
全球血友病患者人数呈持续增长趋势,根据《世界血友病联盟2023年度全球调查报告》,全球血友病患者约 83.6万人,其中严重型约 28.4万人[1]。重型血友病A患者抑制物发生率约为30%,非重型为3%-13%,而血友病B患者为1%-6%[2],抗体阳性会导致传统替代治疗效果不佳,严重影响患者生存质量。重组人凝血因子Ⅶa因其高效止血作用和独特的旁路效应,已成为抑制物阳性患者的重要治疗选择[3],并在全球范围内得到广泛应用。
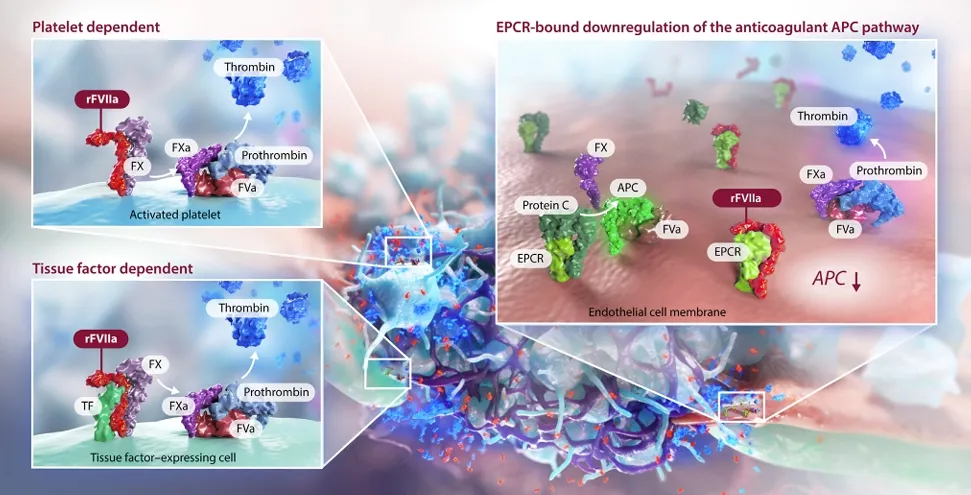
重组人凝血因子Ⅶa(rFⅦa)作用机制
注射用重组人凝血因子Ⅶa N01(安启新®)含有活化的重组凝血因子Ⅶa。血管损伤发生时,凝血因子Ⅶa与暴露的组织因子(TF)结合形成凝血因子Ⅶa-TF复合体,激活外源性凝血途径,进而发生凝血级联反应。凝血因子Ⅶa-TF复合体具有双重底物特异性,一方面,直接激活凝血因子Ⅹ成为凝血因子Ⅹa,激发凝血酶原向凝血酶的转换,进而使纤维蛋白原向纤维蛋白转换形成止血栓;另一方面,激活凝血因子Ⅸ成为凝血因子Ⅸa,增加内源性途径,大量激活凝血因子Ⅹ,将纤维蛋白原转化为纤维蛋白,形成稳固的血栓,从而起到止血的作用。
作为国内唯一疗效和安全性通过Ⅲ期临床试验确证的重组人凝血因子Ⅶa,安启新®的获批基于一项在伴有抑制物血友病患者中的多中心、单臂、开放评估有效性和安全性的Ⅲ期临床研究,本研究共入组60例受试者,均至少使用过一次试验药物,其中53例受试者累计发生559次出血事件。对551次可评估的出血事件进行分析,止血有效率为88.93%(95% CI 86.01,91.43)。
攻克工艺难关 双专利护航生产
工艺方面,重组人凝血因子Ⅶa存在结构复杂、降解和氧化位点较多、杂质种类较多等挑战,公司药学团队创新性地开发了细胞培养、分离纯化和制剂处方等具有自主知识产权的工艺,并获得“人凝血因子Ⅶa的纯化方法(ZL202010330060.5)”和“重组人凝血因子Ⅶa的药物组合物(ZL202410278314.1)”两项原创专利,成功进行了多批次商业化生产放大,产品批间质量一致性良好,充分证明了生产工艺的稳健性。
安启新®作为国内首个获批的国产注射用重组人凝血因子Ⅶa产品,填补了国产空白,为患者提供更经济优质的治疗选择。此前,正大天晴注射用重组人凝血因子Ⅷ(安恒吉®)已获批上市。未来,通过安恒吉®与安启新®的组合治疗方案,公司将构建更完善的血友病治疗产品矩阵,覆盖从常规替代治疗到抑制物管理的全病程需求,显著提升患者生活质量,惠及中国更多血友病患者群体及其家庭。

 产业资讯
产业资讯
 同写意
同写意  2026-03-18
2026-03-18
 38
38
 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-03-18
2026-03-18
 34
34

 产业资讯
产业资讯
 赛柏蓝器械
赛柏蓝器械  2026-03-18
2026-03-18
 33
33