 研发追踪
研发追踪
 药明康德
药明康德  2025-07-28
2025-07-28
 2487
2487
Apnimed公司今日宣布,其潜在“first-in-class”口服候选药物AD109在第二项关键性3期临床试验LunAIRo中达成主要终点。患有轻度、中度和重度阻塞性睡眠呼吸暂停症(OSA)成人患者在接受每日睡前一次AD109治疗后,其OSA症状获得显著改善。Apnimed计划于2026年初向美国FDA递交AD109的新药申请(NDA)。

打呼虽然常见,但有时可能是严重疾病的征兆。医学上看,经常打呼可能意味着患有OSA。这是由于患者在睡眠时上呼吸道扩张肌放松,导致呼吸道阻塞。全球约10亿人受到OSA的影响,患者在一个夜晚可能经历数百次呼吸暂停事件,反复缺氧会损害正常细胞功能,显著增加心血管疾病、神经认知障碍、代谢紊乱和早期死亡等严重长期健康风险。过去40年以来,常见治疗手段为在睡眠时佩戴特定装置来给气管“通气”,但治疗效果有限,很多患者也难以忍受佩戴装置带来的不适。若能有口服疗法问世,将为患者提供更便利的治疗选择。
LunAIRo研究为期12个月,旨在评估AD109在不同体重范围内轻中重度OSA成人患者中的疗效和安全性。分析显示,试验达成主要终点,在第26周显示出临床意义显著且具有统计学意义的气道阻塞改善效果。接受AD109治疗的受试者在第26周平均呼吸暂停低通气指数(AHI)较基线降低46.8%,此数值在对照组为6.8%(p<0.001)。到研究结束时(第51周),患者的AHI改善仍具有统计学意义(p<0.001)。AD109整体耐受性良好,最常见的不良事件为轻度或中度,且与既往研究结果一致。LunAIRo试验中未报告与AD109相关的严重不良事件。
值得一提的是,LunAIRo试验的主要研究结果与Apnimed此前公布的SynAIRgy临床3期试验的积极结果一致。这些数据支持AD109用于治疗轻度、中度和重度OSA成年患者的NDA审评。
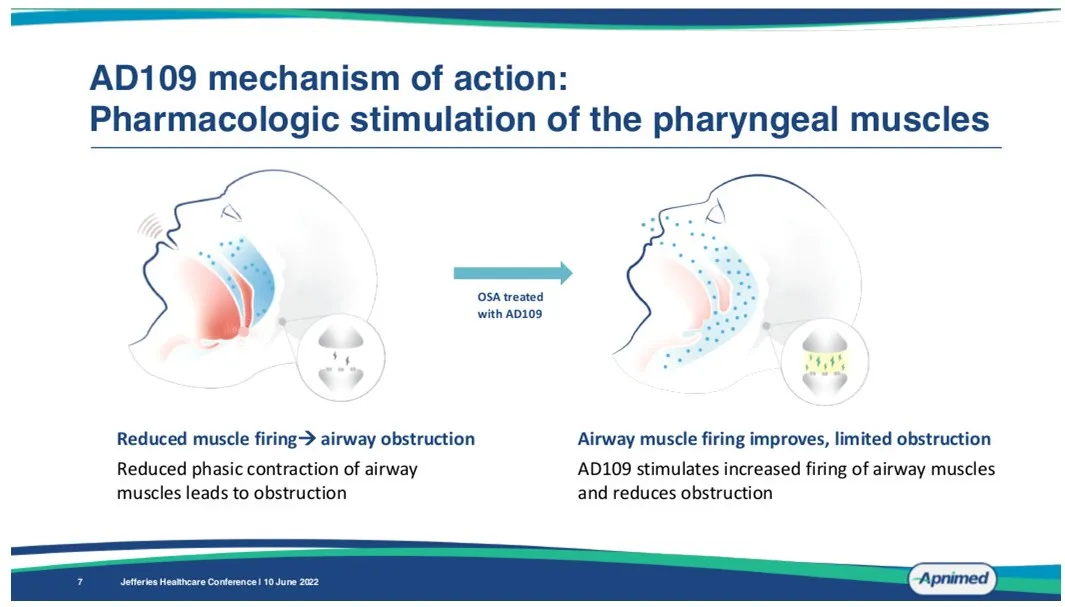
▲AD109的作用机制(图片来源:参考资料[2])
AD109是一种潜在“first-in-class”抗睡眠呼吸暂停神经肌肉调节剂。它是一种由选择性去甲肾上腺素再摄取抑制剂托莫西汀(atomoxetine)与抗毒蕈碱药物aroxybutynin构成的组合配方。AD109靶向OSA关键的神经通路,通过激活上呼吸道扩张肌,使得患者在睡眠时仍可维持呼吸道的畅通。该药物为每日一次、睡前口服剂型,有望简化治疗流程,帮助更多患者实现高质量、恢复性的睡眠。
原文链接:

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 557
557

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 470
470

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 496
496
 热门资讯
热门资讯