 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2026-02-12
2026-02-12
 2702
2702
2 月 11 日,礼来宣布,米吉珠单抗(Mirikizumab)国内获批上市,这是一款选择性靶向 IL-23p19 亚基的单抗,本次同时获批了 2 个适应症,分别用于克罗恩病和溃疡性结肠炎。
图片来源:企业官微
米吉珠单抗通过选择性靶向 IL-23 的 p19 亚基,阻断与 IL-23 受体的相互作用,抑制促炎细胞因子和趋化因子的释放,从而控制炎症。
该药物于 2023 年 3 月 27 日率先在日本获批上市,此后又分别在 EMA 和 FDA 获批上市,用于治疗溃疡性结肠炎。2025 年 1 月至 3 月,FDA、EMA 和日本先后批准该药用于治疗克罗恩病。根据礼来最新披露的财报数据,米吉珠单抗 2025 年收入 2.65 亿美元,同比增长超 100%,正在快速放量中。
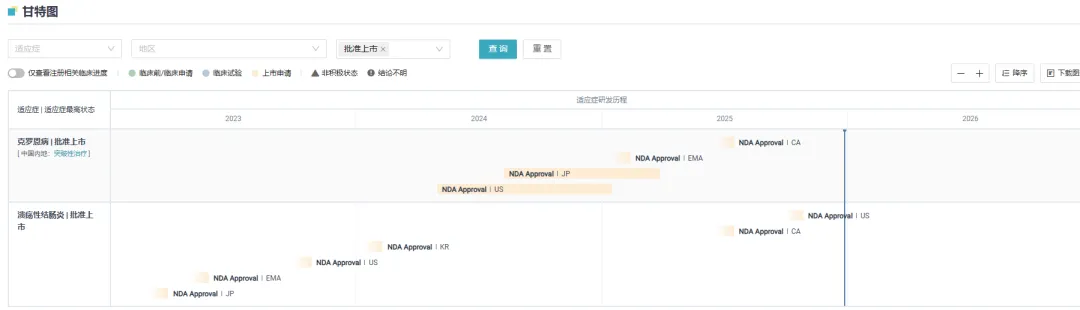
图片来源:Insight 数据库
2025 年 10 月,礼来在中华医学会第二十五次消化系病学术会议(CGC)上披露了米吉珠单抗在克罗恩病和溃疡性结肠炎中的 III 期临床试验数据。
克罗恩病
VIVID 系列研究是探索米吉珠单抗在成人中重度克罗恩病中疗效和安全性的 III 期临床试验。在会议上,被披露的中国亚组数据显示中国中重度活动性克罗恩病患者在接受米吉珠单抗治疗后,相较安慰剂,在联合主要终点和所有关键次要终点均达到了有临床意义的改善。
在 VIVID-1 研究中,共纳入 152 名中重度活动性中国克罗恩病成人患者。与全球人群一致, VIVID-1 中国亚组中,与安慰剂组相比,米吉珠单抗组的联合主要终点和所有关键次要终点均达到了有临床意义的改善。
与接受乌司奴单抗治疗的患者相比,接受米吉珠单抗治疗的患者在第 52 周均有更高比例的患者达到内镜应答(49.4% vs 27.5%)、CDAI 临床缓解(48.2% vs 20.0%),以及 CDAI 临床缓解且内镜应答(32.5% vs 10.0%),显示出与整体人群一致且稳健的临床意义的改善。中国人群中,米吉珠单抗组治疗期间不良事件(TEAE)、严重不良事件和导致研究治疗终止的不良事件的经暴露校正发生率均低于安慰剂组。中国人群大多数 TEAE 的严重程度为轻度至中度。
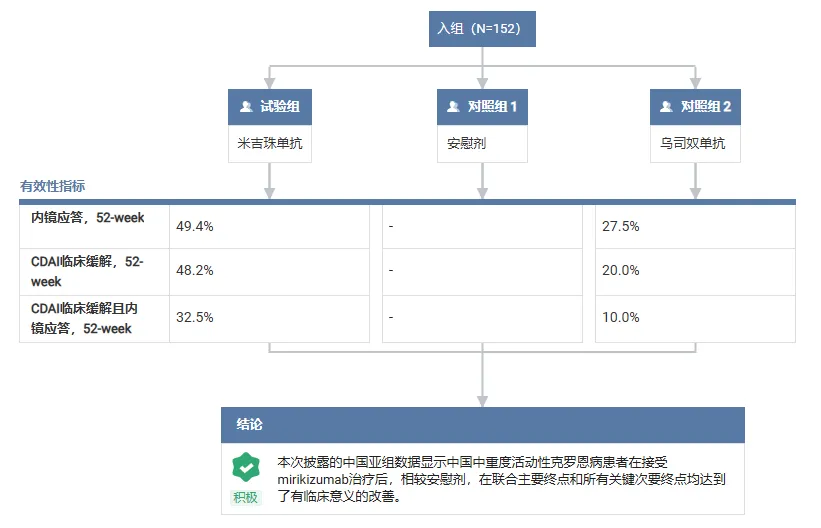
图片来源:Insight 数据库
溃疡性结肠炎
LUCENT 系列研究是探索米吉珠单抗在成人中重度溃疡性结肠炎中疗效和安全性的 III 期临床试验,礼来在此次大会上公布了 LUCENT-1/2 研究中国亚组的诱导期和维持期研究结果。
数据显示,中国中重度活动性溃疡性结肠炎患者在接受米吉珠单抗治疗后,诱导期和维持期临床缓解率均高于安慰剂组,在其他关键次要终点方面也表现出改善结果。
此次公布的研究结果中,中国亚组数据主要包括:
在 LUCENT-1 研究中,共纳入 184 名中重度活动性中国溃疡性结肠炎成人患者。第 12 周时,米吉珠单抗组临床缓解率高于安慰剂组。
在对米吉珠单抗诱导治疗有应答的中国患者中,维持治疗期有 50.0% 的患者在持续治疗后的第 52 周达到临床缓解,显示出与 LUCENT-2 总体人群一致的临床意义的改善。
在中国患者中,各治疗组治疗期间不良事件的发生率相似。与安慰剂组相比,米吉珠单抗组患者的严重不良事件和不良事件导致停药的情况更少。
Insight 视角
Insight 数据库显示,目前国内已批准 8 款 IL-23 靶向药:
其中 5 款作用于 IL-23 p19 亚基,分别是信达的匹康奇拜单抗、艾伯维的利生奇珠单抗、康哲药业引进的替瑞奇珠单抗、强生的古塞奇尤单抗、礼来的米吉珠单抗;
另外 3 款通过结合 IL-12/23 的 p40 亚基发挥作用,分别是康方的依若奇单抗、荃信生物/华东医药的乌司奴单抗-QX001S(生物类似药)、强生的乌司奴单抗。

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-05-18
2026-05-18
 414
414

 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2026-05-18
2026-05-18
 477
477

 研发追踪
研发追踪
 药研网
药研网  2026-05-18
2026-05-18
 390
390
 热门资讯
热门资讯