 会员动态
会员动态
 米内网
米内网  2025-08-19
2025-08-19
 1138
1138
精彩内容
日前,信达生物公布2025年半年报,报告期内总产品收入超52亿元,同比增长35%以上。今年以来,信达生物新药研发进展不断:拿下全球首个GCG/GLP-1双靶点药物及国内首个IGF-1R抗体;7款1类新药首次获批临床等。目前公司有52款新药(50款1类新药)在国内处于申请临床及以上阶段,涵盖小分子、单抗、双抗、ADC、CAR-T等药物形式,其中6款新药已处于NDA或III期临床阶段,上市可期。
拿下16款重磅新药!新型降脂药销售暴涨
8月7日,信达生物公布2025年二季度产品收入情况。2025年上半年,公司总产品收入超52亿元,同比增长35%以上,延续了强劲的增长态势。
通过自研+合作的形式,信达生物目前已有16款新药获批上市(6款已纳入国家医保乙类目录),包括13款创新药及3款生物类似药,形成了以抗肿瘤为核心,代谢、自免、眼科三大领域为补充的丰富产品线。
8月12日,国家医保局公示通过2025年医保目录及商保创新药目录调整初步形式审查的药品及相关信息,替妥尤单抗N01注射液、利厄替尼片、氟泽雷塞片、己二酸他雷替尼胶囊、匹妥布替尼片、塞普替尼胶囊赫然在列。
信达生物已获批上市的新药
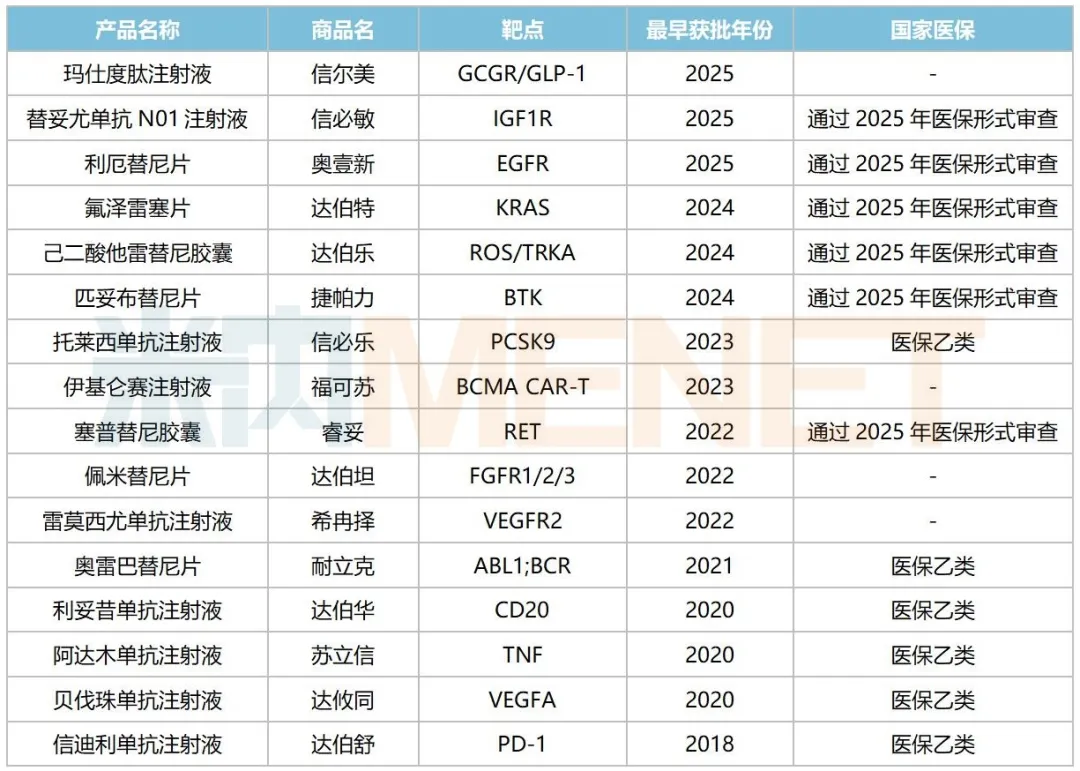
来源:米内网中国上市药品(MID)数据库
在抗肿瘤领域,信达生物的拳头产品达伯舒(信迪利单抗)是国内获批的第2款国产PD-1单抗,自2018年上市至今已累计拓展8个适应症(含附条件批准),其中有7个已被纳入国家医保。随着适应症的不断扩大,叠加医保的积极作用,该药近年来在中国三大终端六大市场(统计范围详见本文末)的销售额保持以两位数的增速增长,2024年其销售额超过40亿元,2025年一季度超过15亿元,其中院内市场(公立医院+公立基层医疗)销售占比超过90%。
近年来中国三大终端六大市场达伯舒销售情况(单位:万元)
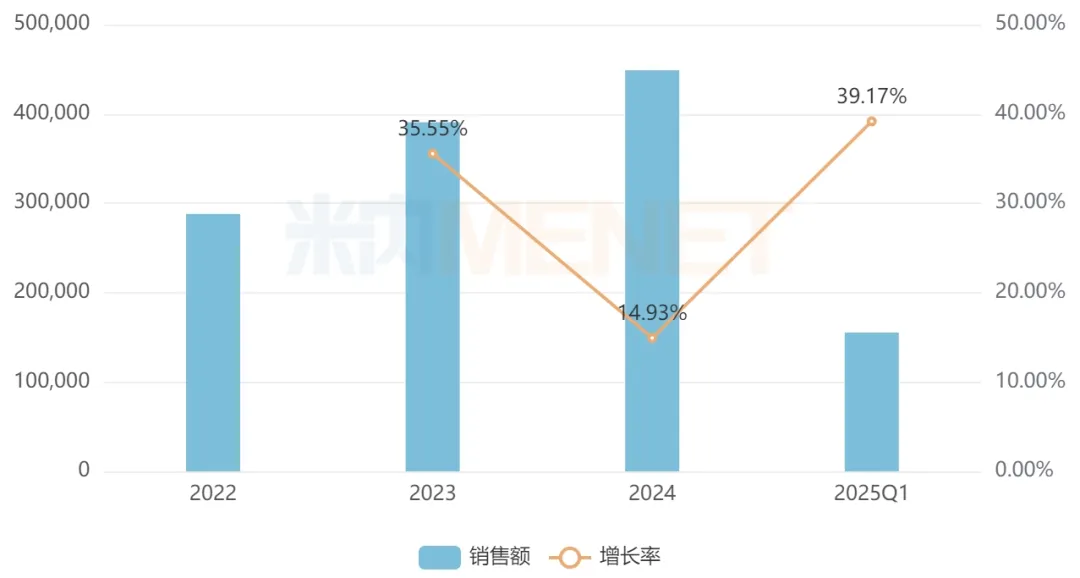
来源:米内网格局数据库
达攸同(贝伐珠单抗)是信达生物获批的首款生物类似药,目前已成长为公司第二大支柱产品。米内网数据显示,达攸同近年来在中国三大终端六大市场的销售额持续增长,且增速呈逐年递增态势,2024年其销售额突破20亿元,2025年一季度超过6亿元。
近年来中国三大终端六大市场达攸同销售情况(单位:万元)
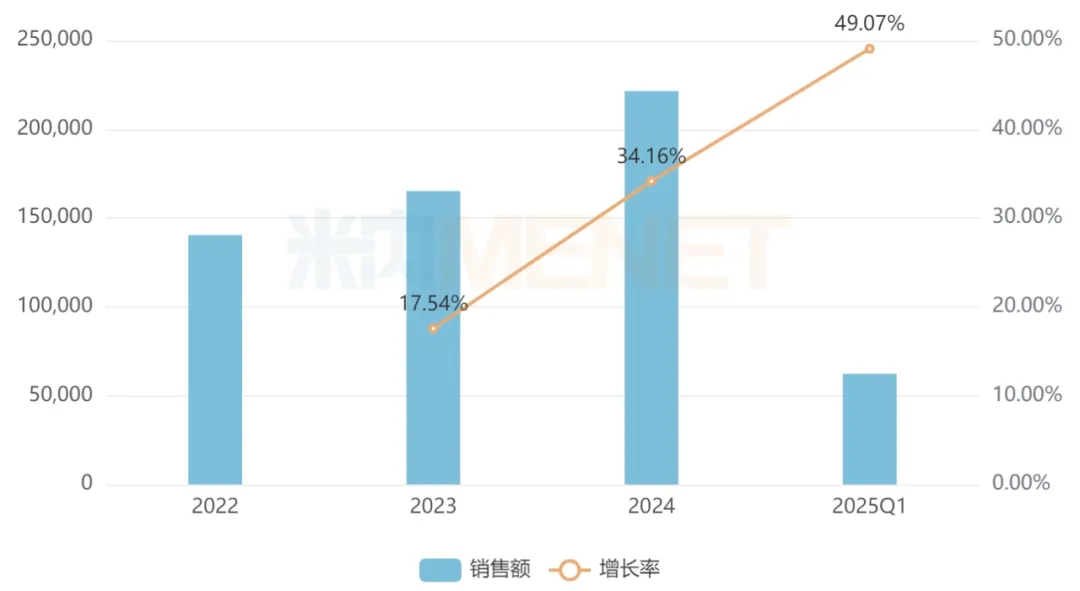
来源:米内网格局数据库
在非肿瘤领域,信达生物的信必乐(托莱西单抗)最早于2023年11月获批,为国内首个本土原研的PCSK9抑制剂,2024年12月纳入国家医保目录,2025年一季度在中国三大终端六大市场的销售额增速超过900%;信尔美(玛仕度肽)于2025年6月获批,为全球首个GLP-1R/GCGR双靶点激动剂,分析师预测其销售峰值有望突破80亿元。
50款1类新药亮眼!6款新药上市可期
除了丰富的商业化产品外,信达生物还有52款新药(不含已获批/撤回品种)在国内处于申请临床及以上阶段,包括47款大分子生物药及5款小分子化学药,其中生物药涵盖单抗、多抗、免疫细胞因子、融合蛋白、抗体偶联药物、细胞治疗等多种药物形式,而化学药聚焦GLP-1、PDE4、XOI等创新治疗靶点。
信达生物国内在研新药
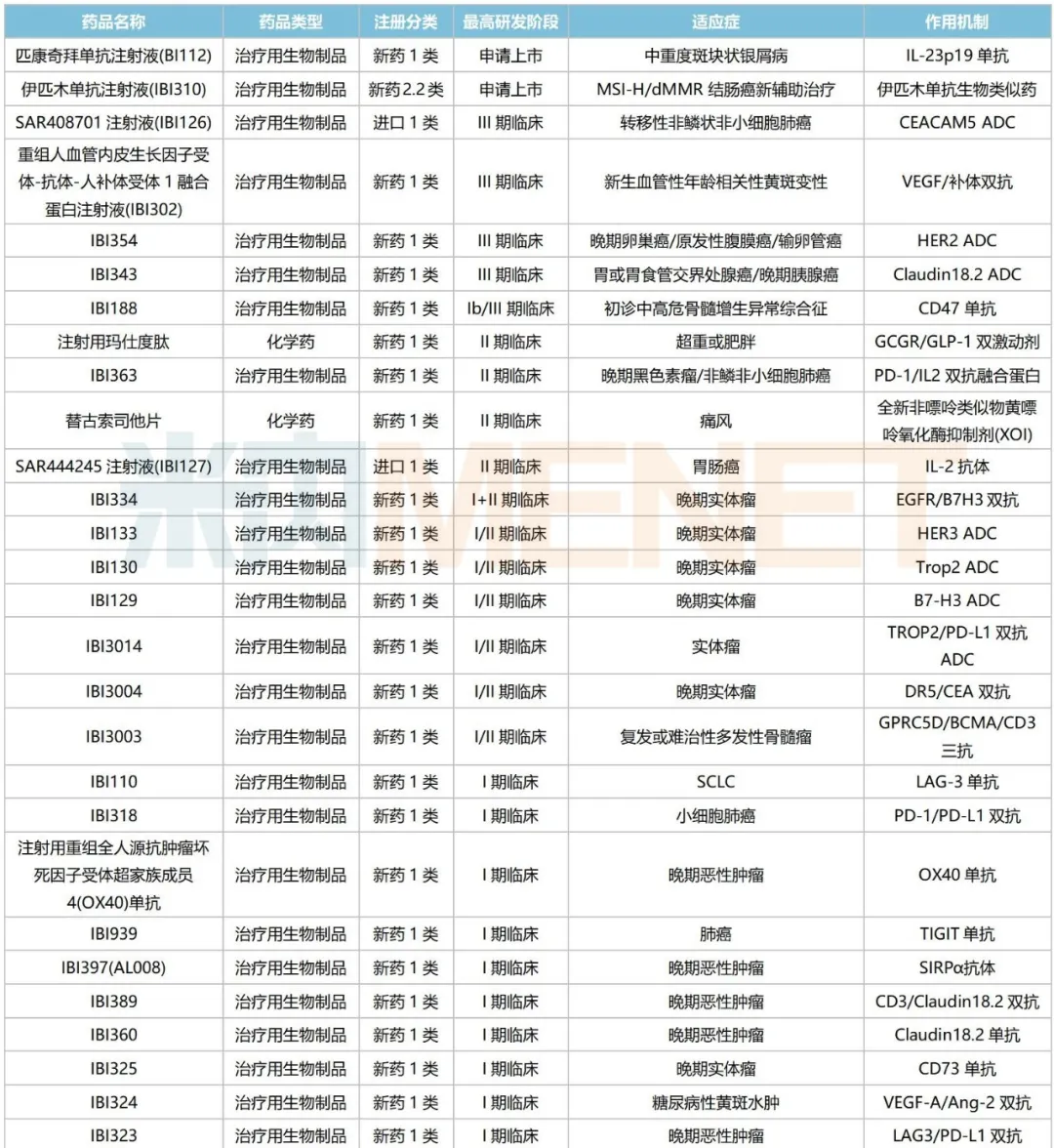
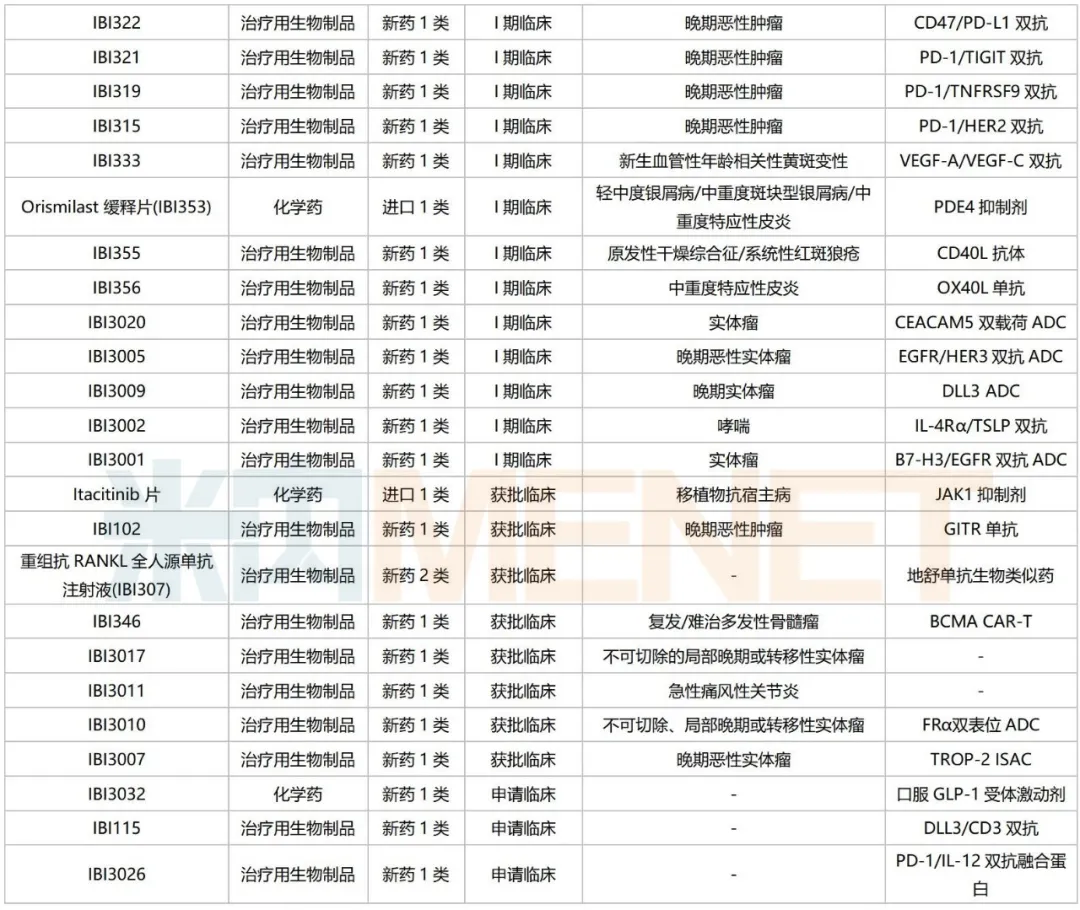
来源:米内网综合数据库
信达生物的新药管线覆盖了肿瘤、自身免疫、眼科、消化代谢等多个疾病领域。
在抗肿瘤领域,4款新药处于III期临床及以上阶段,其中伊匹木单抗于2025年2月提交NDA在审,有望成为国内首个伊匹木单抗生物类似药,原研产品2024年全球销售额超过25亿美元;IBI126、IBI354、IBI343三款ADC处于III期临床,分别靶向CEACAM5、HER2及Claudin18.2,目前全球暂无靶向CEACAM5、Claudin18.2的ADC获批,信达生物均处于研发第一梯队。
此外,20余款抗肿瘤1类新药处于I期或II期临床,涉及多个IO(免疫肿瘤)疗法及ADC。其中,PD-1/IL-2a偏向双特异性抗体融合蛋白IBI363步入II期临床,有望为冷肿瘤和免疫耐药患者提供新的用药选择;三特异性T细胞连接器IBI3003(BCMA/GPRC5D/CD3)处于I/II期临床,该药具备超越CAR-T和双抗的潜力。在新一代ADC方面,信达生物前瞻性布局了双抗ADC和双载荷ADC,包括IBI3014(TROP2/PD-L1双抗ADC)、IBI3020(CEACAM5双载荷ADC)、IBI3005(EGFR/HER3双抗ADC)等。
在自身免疫领域,在研新药聚焦银屑病、特应性皮炎、系统性红斑狼疮、移植物抗宿主病等细分疾病,其中匹康奇拜单抗于2024年9月提交NDA在审,有望成为国内获批的首款国产IL-23 p19靶向药物;IBI353(PDE4抑制剂)、IBI355(CD40L抗体)、IBI356(OX40L单抗)步入I期临床。
在眼科领域,在研新药聚焦新生血管性年龄相关性黄斑变性、糖尿病性黄斑水肿等细分疾病,其中,VEGF/补体双抗IBI302已步入III期临床,VEGF-A/Ang-2双抗IBI324、VEGF-A/VEGF-C双抗IBI333等处于I期临床。
融资、海外BD......国际化进程提速
信达生物是国内率先出海的药企之一。
2020年,信达生物以超10亿美元的交易额,将信迪利单抗在海外的独家权利授权给礼来;2021年初,礼来向FDA递交该药上市申请获受理,却因仅基于国内临床试验,在审核尺度收紧下未通过组委会投票;2022年底,礼来退还了信迪利单抗海外权益。
虽然PD-1出海受挫,但信达生物一直没有放弃海外市场。
今年6月,信达生物宣布完成配股融资超43亿港元(约5.5亿美元),是过去4年港股生物医药行业规模最大、折价最低的一次。据悉,本次配售事项所得净款项约90%将用于推进公司丰厚的临床及临床前重点创新管线的全球研发,以及全球设施设备布局,这将更好地支持公司的全球化布局,并赋予公司在管线开发上更多支持和灵活性。
而在今年1月,信达生物以一场重磅交易震动行业,公司将潜在同类最佳的新型靶向DLL3 ADC药物IBI3009的全球权益授予罗氏,将获得8000万美元的首付款,以及最高达10亿美元的潜在里程碑付款,有望为信达生物的现金流提供强有力支撑。
目前全球暂无靶向DLL3的ADC药物获批,在研新药中,再鼎医药的ZL-1310、恒瑞医药的SHR-4849等处于II期临床,信达生物的IBI3009、成都百利多特的BL-M14D1、上海复旦张江的FZ-AD005等处于I期临床。
除了海外BD,信达生物还有多款创新药正在海外开展临床试验。公司表示:预计到2030年将至少有5款创新管线推进至全球多中心III期注册研究,包括IBI363(全球首创PD-1/IL-2α-bias双抗融合蛋白)、IBI343(CLDN18.2 ADC)、IBI3009(DLL3 ADC)、IBI3001(EGFR/B7H3双抗ADC)、IBI3003(BCMA/GPRC5D/CD3三抗)、IBI3020(全球首个进入临床的CEACAM5双载荷ADC)等。
资料来源:米内网数据库、公司公告等

 会员动态
会员动态
 维健医药
维健医药  2026-04-27
2026-04-27
 356
356

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-27
2026-04-27
 355
355

 会员动态
会员动态
 中国医药创新促进会
中国医药创新促进会  2026-04-20
2026-04-20
 529
529
 热门资讯
热门资讯