 产业资讯
产业资讯
 生物药大时代
生物药大时代  2025-08-28
2025-08-28
 1320
1320
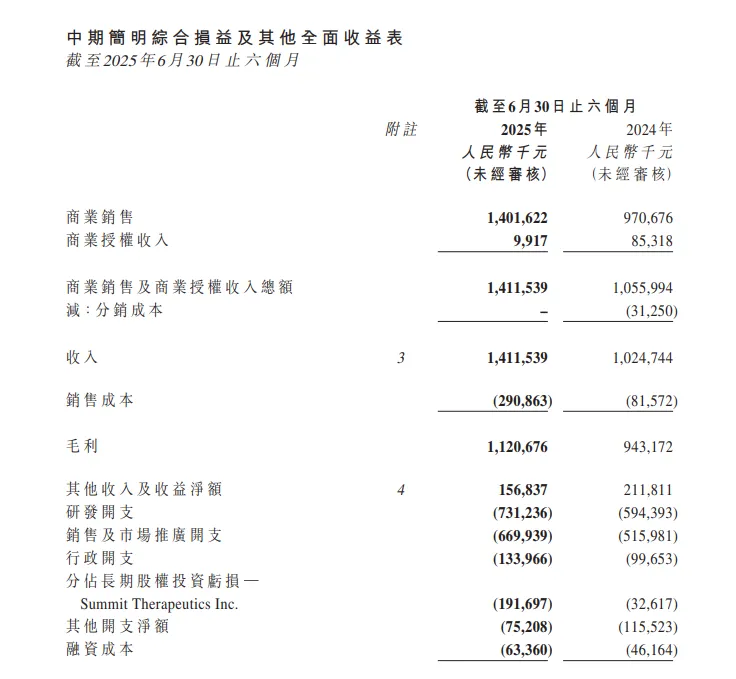
8月26日,康方生物发布2025年中期业绩公告:公司上半年总收入达14.12亿元,同比增长37.75%,商业销售收入达14.02亿元,同比49.20%,占总收入99.3%。营收增长主要得益于两款核心产品卡度尼利与依沃西在去年被纳入国家医保目录适应症后销售显著增长,以及新获批的一线适应症的贡献。报告期内,公司研发投入约7.31亿元,公司现金及其他短期金融资产合计约为71.38亿元。
报告期内,公司不断强化卡度尼利和依沃西在一线大瘤种、冷肿瘤和IO耐药大适应症的全球布局,目前2个IO双抗在全球范围内已开展23项注册性/III期临床研究,并分别开展了近20项II期临床研究,实现了在肿瘤免疫领域深度而科学的布局,为IO双抗全面开拓国际市场奠定重要基础。
尤其重要的是,依沃西单抗(AK112)于2024年5月获得国家药品监督管理局的批准,用于EGFR-TKI治疗进展的局部晚期或转移性非鳞状非小细胞肺癌(nsq-NSCLC),针对该适应症的中国III期HARMONi-A研究(AK112-301)已达到总生存期(OS)临床终点,展现出具有统计学和临床意义的OS获益,详细数据将在未来国际学术会议上发表。
在海外,康方生物的合作伙伴Summit主导开展了依沃西单抗联合化疗用于经第三代EGFR-TKI治疗进展的EGFR突变、局晚期或转移性nsq-NSCLC的国际多中心III期临床研究(HARMONi研究),这也是依沃西首个国际多中心注册性III期临床研究。依沃西首个III期临床研究OS最终分析结果取得了统计学显著获益结果,这有力地证实了依沃西在包括PFS和OS等多个疗效指标中的突破性价值。

此外,继单药“头对头”帕博利珠单抗的随机、双盲、对照III期临床研究(HARMONi-2)获得的显著阳性结果,并成功获批一线治疗PD-L1阳性NSCLC适应症(依沃西第二个获批上市的适应症),依沃西联合化疗对比替雷利珠单抗联合化疗一线治疗鳞状NSCLC的头对头III期临床研究再次取得显著阳性结果。
这证明,无论是在肿瘤免疫领域对比PD-1单药疗法,还是对比PD-1+化疗(当前众多肿瘤治疗最优SOC),还是在肿瘤抗血管生成领域对比VEGF相关疗法,双抗疗法都拥有显著的临床突破性,凸显了依沃西在肿瘤治疗中强大的迭代能力。
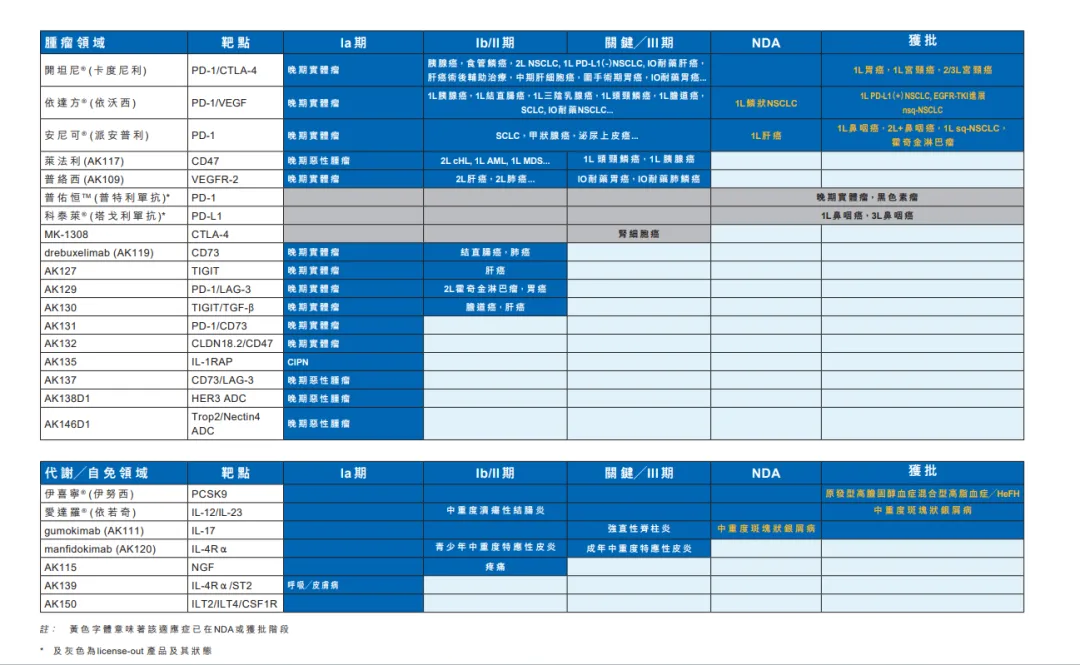
在不断证明自身重大临床价值和迭代临床标准疗法的同时,依沃西也在不断拓展在肿瘤免疫核心适应症的布局:

另一方面,IO+ADC已经成为肿瘤联合疗法发展的重要方向,康方生物凭借卡度尼利和依沃西获批上市而成为全球唯一拥有2个肿瘤免疫双抗的公司。康方生物双抗ADC药物Trop2/Nectin4
ADC(AK146D1)、新一代差异化HER 3
ADC(AK138D1)均已进入全球临床开发阶段,AK138D1和AK146D1联合卡度尼利、依沃西治疗肿瘤的相关临床研究正在筹备中。
特别值得一提的是,公司自研差异化PD-1抑制剂派安普利单抗已经获得美国药品与食品监督管理局(FDA)批准上市,这是康方生物首个在美国获批的自研创新药物,是首个由中国公司全程独立主导(研发,临床,生产供药和申报注册)且成功获得FDA批准上市的创新生物药。
报告期内,公司其他肿瘤药物也取得了多项重要里程碑发展:公司自研新一代CD47单抗莱法利单抗(AK117)目前已与卡度尼利和依沃西等药物开展了多个肿瘤领域的临床研究,包括2个实体瘤的III期临床研究,莱法利单抗在血液瘤领域的全球临床开发也在高效开展;公司自研肿瘤新药普络西单抗(VEGFR-2)也已联合卡度尼利等药物开展了多项临床研究,包括正在筹备的或已经开展的III期临床研究。
非肿瘤业务也在实现破局,随着依若奇单抗、古莫奇单抗、伊努西单抗、曼多奇单抗等产品相继上市,以及IL-4R/ST2双抗、神经系统疾病等非肿瘤创新靶点药物的高效深度开发,公司产品组合力愈发强劲,非肿瘤板块的全球竞争力正不断增强。
肿瘤治疗领域正从“单抗纪元”大步跨入“双抗纪元”:一边是跨国巨头豪掷数十亿美元扫货全球管线,一边是本土新锐以光速递交临床申请,千亿级赛道早已硝烟弥漫,竞争维度也从早期的“谁先做出分子”升级为“谁能在临床价值、工艺产能、商业化打法与医保准入”四维战场同时得分。在这场关乎未来十年的高阶混战中,康方生物以全球首个获批上市的PD-1/CTLA-4双抗卡度尼利为矛,以年产能超过2万升的智能化商业化基地为盾,再以纵深覆盖20余款双抗/多抗的管线为粮仓,率先完成了从“做出双抗”到“卖好双抗”的惊险一跃,让市场看到了双抗长跑的真正价值锚点。

 产业资讯
产业资讯
 医药魔方
医药魔方  2026-03-14
2026-03-14
 107
107
 产业资讯
产业资讯
 会会药咖
会会药咖  2026-03-14
2026-03-14
 107
107

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-03-14
2026-03-14
 108
108