 研发追踪
研发追踪
 Bio Journey
Bio Journey  2025-08-30
2025-08-30
 2081
2081
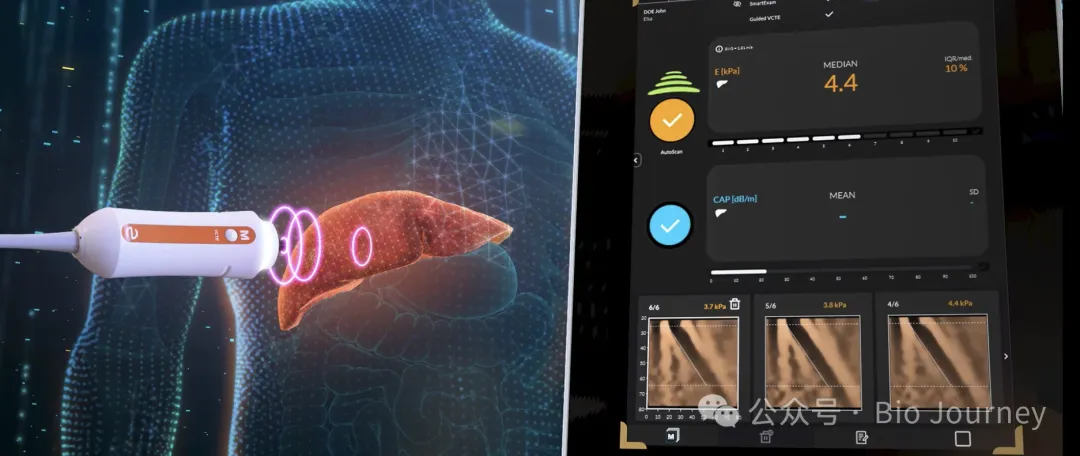
摘要: 美国食品药品监督管理局 (FDA) 正在考虑在部分MASH(代谢功能障碍相关脂肪性肝炎)药物的试验中,使用一种无创检测方法来替代肝活检以确定结果。此举最终可能使患者入组和药物进展评估变得更加容易。
告别肝活检?FDA受理VCTE资格认证申请
本周三(8月27日),FDA宣布已受理一家公司提交的意向书,该公司寻求将通过振动控制瞬时弹性成像 (VCTE) 进行的肝脏硬度测量,认证为用于中度至晚期纤维化的成年MASH患者临床试验的“合理可能替代终点 (reasonably likely surrogate endpoint)”。
这项技术通过使用超声波信号来测量肝脏的硬度,从而帮助评估瘢痕或纤维化程度。
Leerink的分析师表示,这一宣布是朝着使用无创检测迈出的“重要的第一步”,而此前用于加速批准的“历史标准”一直是肝活检。肝活检有时需要将一根长针刺入腹部以从器官中取样,从而衡量患者病情是否改善。
“我们认为这对MASH领域的临床开发是一个重大利好,”Leerink的分析师在给投资者的一份报告中写道。
漫长的资格认证之路
尽管前景乐观,但分析师也指出,由于资格认证过程可能需要一年以上的时间,其全部影响可能难以预测。
FDA的生物标志物资格认证项目是一个三步流程:
1)意向书 (Letter of Intent)
2)资格认证计划 (Qualification Plan)
3)完整的资格认证包 (Full Qualification Package)
根据FDA官网信息,该机构的目标是分别在6个月和10个月内完成对“资格认证计划”和“完整的资格认证包”的审查。然而,Leerink的分析师指出,“时间表还取决于申办方提交补充信息的情况,这也可能有所不同。”
MASH领域的“重大利好”
Madrigal Pharmaceuticals的创始人Becky Taub向媒体表示,这一步对于“MASH领域来说是个好消息”。Madrigal公司的药物Rezdiffra于2024年成为首款获批用于治疗MASH的药物。

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 563
563

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 477
477

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 501
501
 热门资讯
热门资讯