 研发追踪
研发追踪
 求实药社
求实药社  2025-09-22
2025-09-22
 2209
2209
当地时间 9 月 17 日,赛诺菲宣布 Brivekimig 在治疗化脓性汗腺炎(HS)IIa 期研究中取得积极成果。该研究结果将在 2025 年欧洲皮肤病和性病学会 (EADV) 年会上以口头报告形式分享。

截图来源:企业官网
这是一项随机、双盲、安慰剂对照、概念验证性研究,旨在评估 Brivekimig 对中重度 HS 成人患者的疗效和安全性。
主要分析人群为未接受过生物制剂治疗的 HS 患者,按 2:1 的比例随机分配接受 Brivekimig 150 mg 或安慰剂皮下注射,每两周一次。主要疗效终点是未接受过生物制剂治疗的参与者在第 16 周达到 HiSCR50(定义为总脓肿和炎性结节数量减少 ≥50%,且脓肿或引流瘘数量相对于基线没有增加)的百分比。
16 周时观察到以下情况:
Brivekimig 组(n=48)的中位反应率为 67%,而安慰剂组为 37%(n=23)。
与安慰剂相比,Brivekimig在 HiSCR75 和 HiSCR90 的更严格的次要疗效终点方面也表现出了具有临床意义的改善。
接受 Brivekimig 治疗的患者中有 54% 达到了 HiSCR75,而接受安慰剂治疗的患者中这一比例为 22%(p=0.0171)。
接受 Brivekimig 治疗的患者中 31% 达到了 HiSCR90,而接受安慰剂治疗的患者中只有 9% 达到了 HiSCR90(p=0.0576)。
与基线相比,Brivekimig 组的引流瘘数量平均变化百分比为 -56.0%,而安慰剂组为 +10.9%(p=0.005)。
在安全性方面,最常见的不良事件(发生在 >10% 的参与者中,并且使用 Brivekimig 的发生率高于使用安慰剂的发生率)是鼻咽炎和头痛。
Brivekimig 是一种双靶点纳米抗体分子,可抑制肿瘤坏死因子(TNF)和 OX40 配体(关键的免疫调节因子)。赛诺菲正在研究该药物在一系列免疫介导疾病和炎症性疾病中的潜在应用。
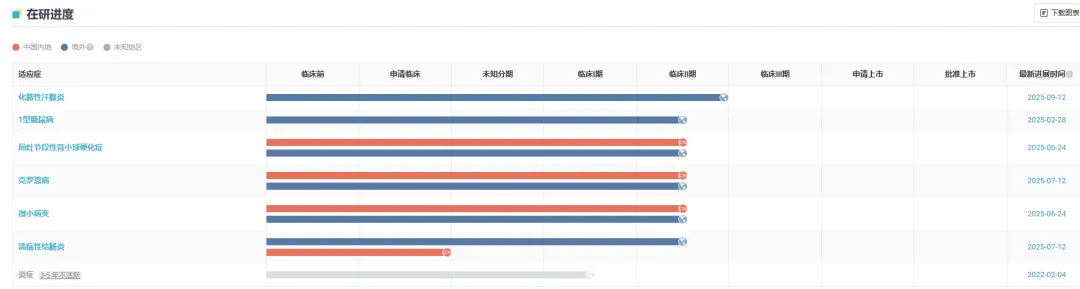
截图来源:Insight 数据库
Insight 数据库显示,目前全球范围内共有 3 款 TNF/OX40L 双抗在研,Brivekimig 是全球进展最快的。
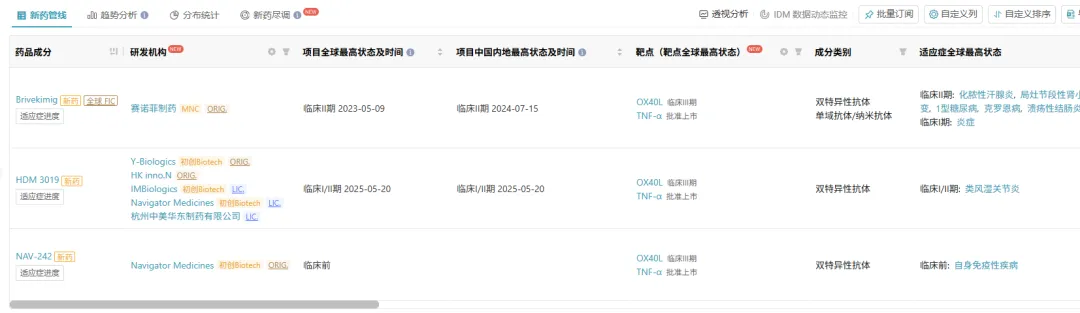
截图来源:Insight 数据库
值得一提的是,在此前公布一季度业绩时,赛诺菲认为 Brivekimig 是一款具有竞争力的药物,基于 Amlitelimab(OX40L 单抗)在 HS II 期临床试验(NCT06118099)中的疗效未达预期,赛诺菲决定将 Brivekimig 的开发优先级提高。
原文链接:
https://www.sanofi.com/en/media-room/press-releases/2025/2025-09-17-05-00-00-3151353

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 568
568

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 481
481

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 507
507
 热门资讯
热门资讯