 研发追踪
研发追踪
 医药魔方Info
医药魔方Info  2025-09-29
2025-09-29
 3082
3082
9月24日,全球临床试验收录网站显示,赛诺菲的TSLP/IL-13双抗Lunsekimig(SAR443765)推进至II/III期阶段,针对慢性阻塞性肺病(COPD)启动了两项II/III期临床试验(THESEUS和PERSEPHONE)。

两项研究拟纳入1884例患者,旨在评估Lunsekimig(两个剂量,皮下注射)对比安慰剂治疗控制不佳的嗜酸性粒细胞表型COPD成人患者的有效性和安全性。研究的主要终点为基线至第48周中重度COPD恶化的年化发生率。
此前,赛诺菲曾公布Lunsekimig治疗哮喘的Ib期概念验证研究数据。数据显示,哮喘患者经400mg Lunsekimig治疗28天后,呼出一氧化碳分数(FENO)较基线显著降低,较安慰剂组降幅为40.9ppb(p<0.0001)。此外,患者的2型炎症反应生物标志物水平亦显著降低。
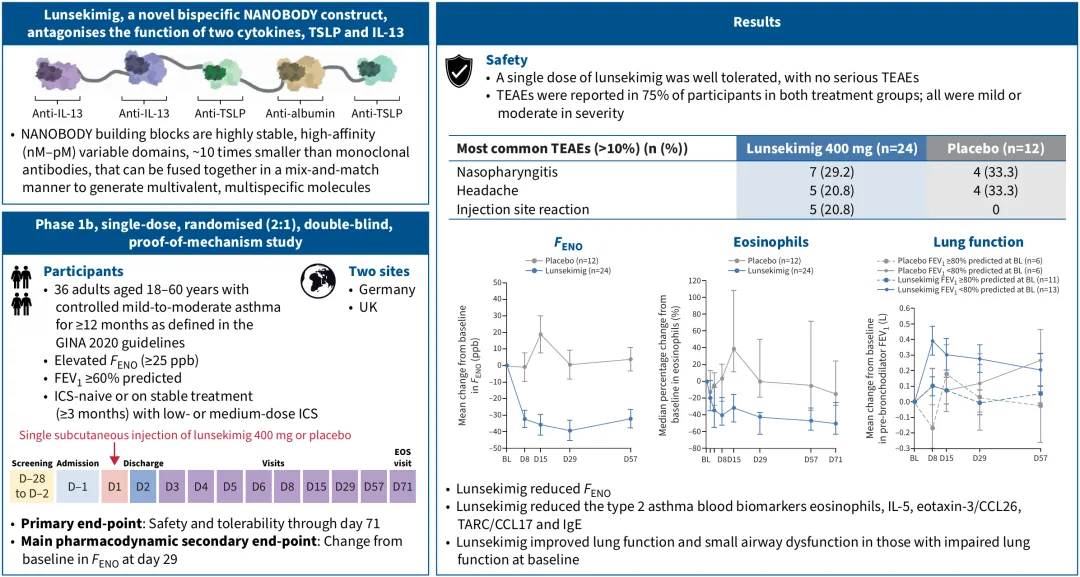
来源:European Respiratory Journal
据医药魔方数据库统计,全球共22款在研TSLP双抗药物,其中7款处于临床阶段,包括两款TSLP/IL-13双抗(Lunsekimig和CM512)、一款TSLP/IL-11双抗HB0056、一款TSLP双抗GR2002、一款TSLP/IL-4Rα双抗IBI3002、一款TSLP/SCF双抗CDX-622和一款TSLP/IL-4Rα双抗BSI-502。
英文:https://clinicaltrials.gov/study/NCT07190222

 研发追踪
研发追踪
 药融圈
药融圈  2026-06-01
2026-06-01
 730
730

 研发追踪
研发追踪
 细胞基因研究圈
细胞基因研究圈  2026-06-01
2026-06-01
 819
819

 研发追踪
研发追踪
 药时代
药时代  2026-06-01
2026-06-01
 699
699
 热门资讯
热门资讯