 产业资讯
产业资讯
 氨基观察
氨基观察  2025-11-18
2025-11-18
 2285
2285
在肿瘤药创新的浪潮中,谁能执掌下一代IO疗法的话语权?
这个问题很难回答。但有一点是确定的,那就是药企必须手握一款足以替代PD-1的基石级药物。
经历TIGIT、CD47的预期落空之后,PD-(L) 1/VEGF双抗已然成为迭代PD-1的核心方向,不仅被MNC视为IO领域的现象级候选,更催生了一场有望重塑未来十年行业格局的白热化竞赛。
曾经由Summit/康方生物独领风骚的赛道,如今已迎来BioNTech、BMS、辉瑞等巨头的全速入局。
有趣的是,辉瑞与BioNTech相继围绕各自从中国引进的引进的PD-(L) 1/VEGF双抗召开投资者活动,并抛出了类似的“Displace、Establish、Expand”与“Establish、Expand、Elevate” 三步走策略,在迭代、联用与适应症拓展上展开激烈角逐。
辉瑞更是年内第二次举办该活动,计划近期启动7项临床,明年再添10项单药及10项联用临床,足见其对从三生制药引进的SSGJ-707/ PF-08634404的重视。BioNTech则将 PD-(L) 1/VEGF双抗定义为“下一代 IO”,希望联手BMS加速推进,并借助联合疗法来超越“增量效应”。
这场竞赛的升级,本质是生物制药技术大航海时代的必然。创新迭代的加速让竞争维度不断提升,大药企凭借资金、资源与经验优势,可以在全球一口气开数个甚至十数个大三期,同步推进多适应症、多治疗线、多联合方案的全球临床探索。
这也倒逼着所有参与者加速进化:无论巨头还是biotech,必须深刻洞察临床需求的本质、认真评估市场需求与技术趋势,同时保持高度创新的敏捷性。
/ 01 /
BioNTech的野心
在BioNTech首席医学官Özlem Türeci眼中,PD-(L) 1/VEGF双抗绝非TIGIT、CD47这类“昨日黄花”,而是下一代IO”,“这类分子已经成熟,具备进行泛肿瘤开发潜力,有望取代第一代 PD-(L) 1 疗法”。
因此,BioNTech在2023年11月收购普米斯获得PD-L1/VEGF双抗BNT327除大中华区外的全球权益后,高速推进临床。
在2024年一季报中,BioNTech对于BNT327的研发,只有2项临床。而截至2025年6月末,BNT327已经推动20项临床落地。
在最新的投资者会议上,BioNTech重申了“Establish、Expand、Elevate”三步走策略,并详细列出了临床试验列表。

如上图所示,在建立(Establish)阶段,BNT327正在小细胞癌(ES-SCLC)、非小细胞癌(NSCLC)和三阴性乳腺癌(TNBC)三大领域开展3期临床,以验证其临床实力。并且,BioNTech的入组迅速,其中针对ES-SCLC的3期试验(ROSETTA-Lung-01)以阿替利珠单抗联合化疗这一当前ES-SCLC一线治疗的标准方案为对照,半年时间就招募了439名患者,顺利完成全部入组。
BioNTech曾表示,一旦数据阳性,即可直接向美国FDA、欧洲EMA及中国NMPA提交上市申请,大幅缩短从临床到商业化的周期。
拓展(Expand)阶段聚焦泛癌种布局,通过12项研究、10多个新适应症来扩展BNT327的布局,覆盖胃癌、结直肠癌、肝癌、头颈癌、肾癌、乳腺癌、胰腺癌等等。并且,对于未来的卡位,BNT327也正在进行升级(Elevate)布局。
BioNTech正瞄准下一代联合疗法,推进BNT327与HER2、B7-H3、Trop2等靶点 ADC,以及新型免疫靶点药物(如PVRIG抑制剂BNT3213)的1/2期临床试验。
与BMS的合作更是加速关键。BioNTech首席执行官Uğur Şahin直言,“2025年底或2026年初再行动就太迟了”,合作的关键原因就是为了 “加速”。
于是我们看到,继6月双方达成合作后,BMS于10月底快速主导启动胃癌、结直肠癌两项2/3期临床,其在肿瘤免疫领域的深厚积累,无疑将为BNT327的研发注入强劲动力。
/ 02 /
辉瑞开启“闪电战”
在与诺和诺德争夺下一代减肥药资产的同时,辉瑞正以同样决心推进肿瘤布局。日前,其再次召开PD-1/VEGF投资人会议,宣布即将启动7项近期临床,包括一线非小细胞肺癌和一线结直肠癌的两项全球多中心三期临床试验,以及其他5项研究。
显然,辉瑞将从三生制药引进的SSGJ-707/ PF-08634404作为其肿瘤管线中最重要的资产来推进。与BioNTech类似,辉瑞也放出了三步走的口号“Displace,Establish,Expand”。
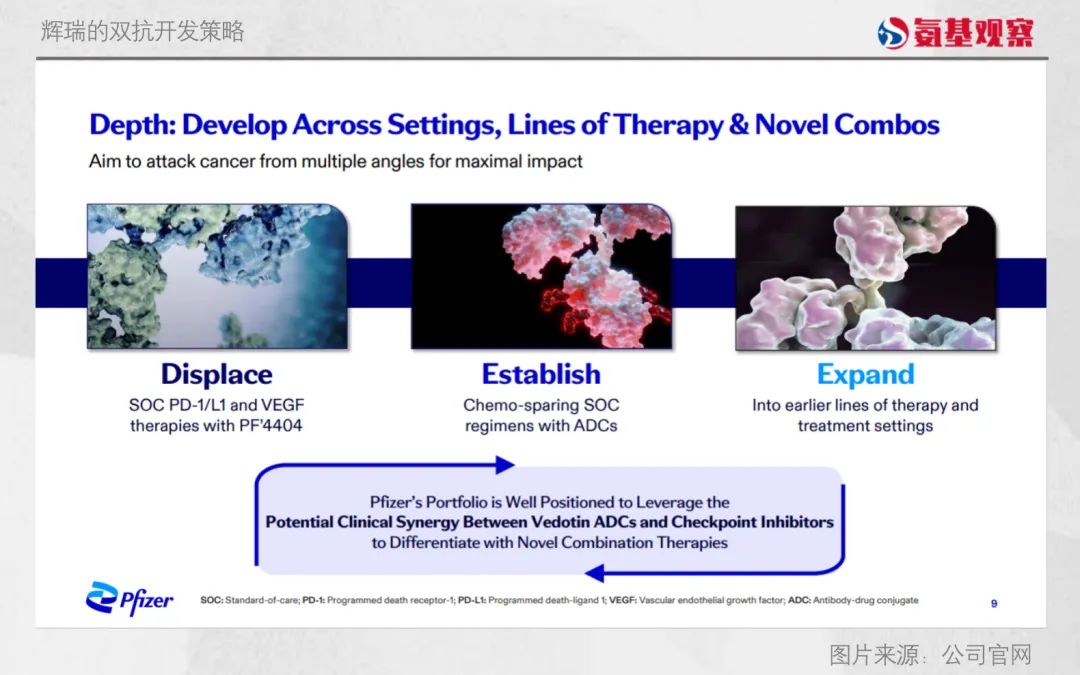
简单来说,辉瑞希望通过替代现有PD-1/PD-L1及VEGF单抗,让PD-1
VEGF双抗成为新的基石疗法;同时其计划在不同治疗线来探索4404与ADC的联用,进而建立新一代“去化疗化”方案;其还计划推动4404拓展至更早期肿瘤治疗,包括新辅助和辅助治疗阶段。
不同于BioNTech,这三步走只是辉瑞在更大的“Speed,Breadth,Depth”中,关于Depth的规划。
由于全球布局起步较晚,辉瑞将“速度(Speed)”置于首位,依托强大的全球开发能力追赶进度:
自完成授权交易后3个多月,已向FDA提交了5项新的IND;遴选 500 余个全球临床中心覆盖 25 国以上,推进4404研究;加速了技术转移时间表,并已在美国成功完成4404药品生产。
广度(Breadth)层面,辉瑞依托在多个关键疾病领域的布局,对4404进行多癌种开发。这在近期的临床试验已展现端倪,除了非小细胞肺癌、结直肠癌,还有广泛期小细胞肺癌、肝癌、尿路上皮癌和肾癌。
在适应症方面,BioNTech当前布局更广。辉瑞则表示正在积极准备第二波临床,计划 2026 年底前启动10个新适应症及10项以上新型联用方案研究。
深度(Depth)则源自辉瑞多种药物形式、聚焦领域和能力方面的组合,在不同亚组、不同线数以及新型联用方案中开发4404。
在肺癌等愈发拥挤的领域,辉瑞希望通过简单的加法,即在标准治疗之上叠加4404,来改善并取代现有化疗方案。与此同时,辉瑞表示接下来新一波的创新会进入新型联合方案。
11月12日,其已经在clinical trials网站上,登记了一项4404联合整合素β6 ADC药物Sigvotatug Vedotin的一项1/2期临床试验NCT07227298,预计2025年11月启动。这是4404首次启动的联合ADC临床。
辉瑞对4404的重视,既源于PD-(L)1/VEGF双抗已验证的替代潜力,也得益于其与管线产品的协同效应。通过既快速又具有临床意义的终点改进以及新型联用方案,辉瑞正试图在下一代肿瘤竞赛中确立差异化优势。
这也再次提醒我们,BD找一个好队友的重要性。
/ 03 /
肿瘤竞赛上了新高度
这场肿瘤竞赛正在持续加温。
辉瑞与BioNTech这对曾在新冠疫苗上创造奇迹的合作伙伴,将展开正面角逐。Uğur Şahin直言,“如果你拥有这样一个最终可能成为下一代标杆的化合物,与大药企竞争将不可避免”。
有意思的是,11月13日有报道称,辉瑞计划计划出售其持有的BioNTech SE剩余股份,拟通过隔夜大宗交易方式出售约455万股,潜在出售股份的所得约为5.08亿美元。同日,BioNTech股价大跌7%。
当然,更重要的是,透过BioNTech/BMS、辉瑞的布局来看,三步走的研发策略已经成为PD-(L)1/VEGF双抗开发的标配,而双抗+ ADC的联用则成为进一步突破的关键方向。
这也预示着,下一代肿瘤竞赛被拉到了一个全新高度。大药企有钱有资源有经验,可以一口气开数个甚至十数个大三期,而且还是多适应症、多治疗线、多联合方案,同步探索。
尤其是随着PD-1+ADC的疗效被反复验证后,PD-1/VEGF双抗的联用正迅速铺开。
比如荣昌生物正推进CLDN18.2 ADC(RC118)联合PD-1/VEGF双抗(RC148)的研究,用于CLDN18.2阳性的胃食管癌患者,初步数据显示出可观的缓解率与PFS改善趋势。
BioNTech则是目前双抗PD-1+ADC临床进展最快的公司;辉瑞同样在强化这一方向。继5月引进SSGJ-707后,目前已登记了首项ADC联用临床,按照投资者会议的说法,后续将继续推进新型联用。
所谓新型联用,指的是与其Vedotin类 ADC资产的联用。辉瑞表示,当与Vedotin载荷而非 TOPO1载荷联合时,能够提升PD-1抑制剂的免疫原性潜力。三生制药也在探索SSGJ-707与EGFR/HER3双抗ADC(BL-B01D1)的联用。
肿瘤领域的技术迭代本就迅猛,竞争思路与格局也在持续升级。这自然对药企提出了更高要求:后来者需在管线研发、BD 策略层面寻求突破,而默沙东等先行者则要思考如何守擂,同时布局未来行业制高点。
当然,尽管今年PD-1/VEGF双抗势头凶猛,但要验证上述那些雄心勃勃的开发计划是否有效,还需要时间。
接下来几年将是关键催化剂期,多项III期试验数据的读出的进展,将决定PD-(L)1/VEGF双抗能否成功跻身跨瘤种基石疗法,填补全球肿瘤治疗的巨大未满足需求。
在翻涌的创新浪潮中,期待着更多突破的早日到来。

 产业资讯
产业资讯
 医药地理
医药地理  2026-05-22
2026-05-22
 489
489

 产业资讯
产业资讯
 药智数据
药智数据  2026-05-22
2026-05-22
 75
75

 产业资讯
产业资讯
 细胞基因治疗前沿
细胞基因治疗前沿  2026-05-22
2026-05-22
 401
401
 热门资讯
热门资讯