 研发追踪
研发追踪
 药智网
药智网  2025-11-20
2025-11-20
 703
703
靶点表位的选择,是创新药开发中决定命运的一场豪赌。
它奠定了药物开发的方向,但其对药物安全性的影响往往要到临床阶段才能“见真章”。此前,吉利德Magrolimab,艾伯维Lemzoparlimab和辉瑞TTI-621等靶向CD47抗体先后因药物诱发的严重靶细胞毒性而折戟,而新一代“后浪”中的AK117(Ligufalimab)通过差异化的CD47表位选择,在非临床和早期临床中展现出高度优于竞品的安全性。可见表位选择的成功与否,极有可能赋予品种完全不同的潜力。
近期,发表于Journal of Biological Chemistry的文章“Structural basis of nectin-4 recognition by the antibody–drug conjugate 9MW2821”揭示了迈威生物的在研ADC品种结构和结合表位。这或许又将是一个表位选择影响药品安全性的典型案例。
01
靶向毒性,仍待解决
Nectin-4因其在尿路上皮癌、乳腺癌、胰腺癌、肺癌、卵巢癌、头颈部癌、食管癌等多种实体瘤组织中的高表达[1]而被寄予厚望。首个获批上市的维恩妥尤单抗Padcev证实了这一靶点在尿路上皮癌的治疗效果,但随之而来的FDA黑框警告多少让其显得“美中不足”。
PADCEV临床上常见的血液毒性外的不良反应主要集中在皮肤和眼部,皮肤毒性包括脱发、瘙痒、斑丘疹等,眼部毒性包括干眼、角膜炎、视力模糊、溢泪和角膜缘干细胞功能不全等[2]。此外,它还可能导致重度和致死性皮肤不良反应,包括史蒂文斯-约翰逊综合征(Stevens-Johnson Syndrome,SJS)和中毒性表皮坏死松解症(Toxic Epidermal Necrolysis,TEN),因此说明书被FDA加上了黑框警告。
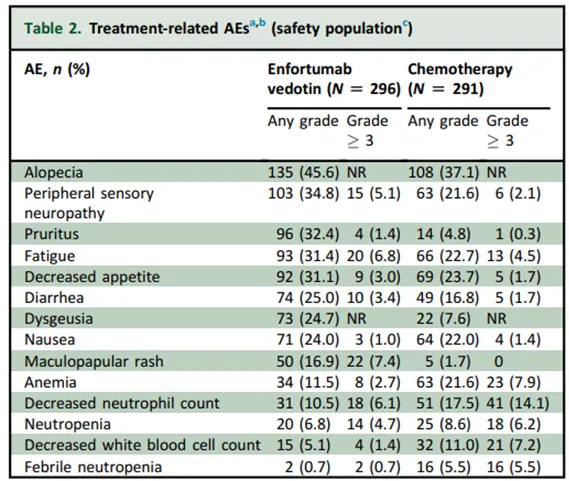
图1 PADCEV的常见不良反应[9]
这些靶向毒性可能与Nectin-4在正常组织中的表达有关。人类蛋白质图谱数据库(HPA)显示,Nectin-4蛋白在皮肤、膀胱、唾液腺、食管、乳腺和胃等正常组织中呈中低水平表达。此外,DISCO单细胞测序数据库显示,正常眼部中结膜上皮细胞和角膜细胞均有Nectin-4表达。
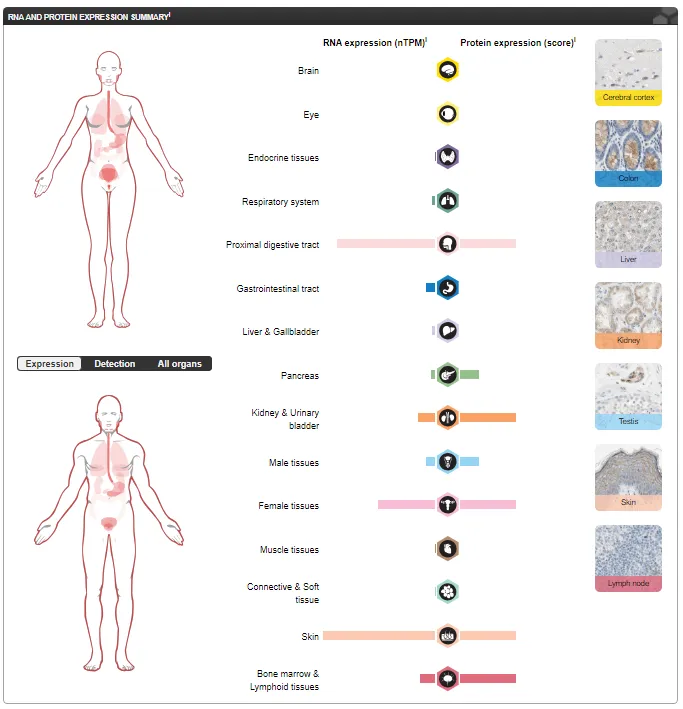
图2 Nectin-4在正常组织中表达情况
https://www.proteinatlas.org/ENSG00000143217-NECTIN4/tissue
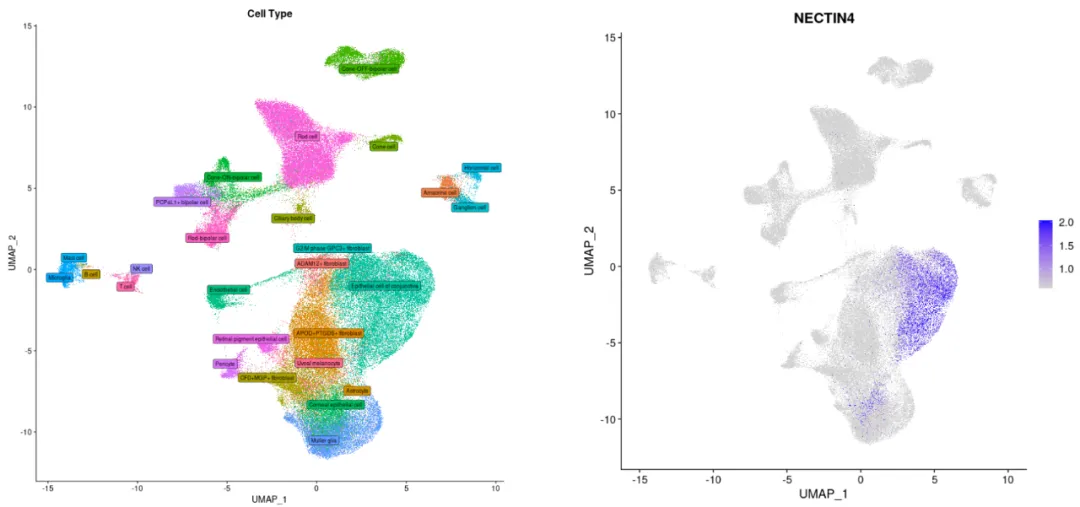
图3 DISCO数据库中眼部细胞Nectin-4表达情况
https://www.immunesinglecell.com/genepage/NECTIN4
而这也是Nectin-4 ADC的“后浪”们需要面对的挑战。目前,临床阶段的Nectin-4 ADC产品包括迈威生物的9MW2821,恒瑞医药的SHA-A2102,石药的SYS6002等,其中9MW2821在尿路上皮癌、宫颈癌开启了共3项三期研究,在国产品种中处于领跑地位。
02
抗原表位,选择决定命运
对于Nectin-4这类在正常组织中有低表达的靶点,在筛选ADC抗体时,抗原表位的选择就显得至关重要。一方面,ADC与抗原结合后,可能会改变Nectin-4蛋白的天然结构和功能,直接导致组织损伤和炎症反应。另一方面,正常组织器官中的Nectin-4呈现出一定的规律性紧密排列以维持上皮细胞的功能,Nectin-4的表位可能无法充分暴露,但肿瘤细胞由于过度增殖呈现无序排列,Nectin-4结合表位将得以充分暴露。
选择合理的抗原表位,即正常细胞中因紧密连接而被屏蔽的表位,可有效避免正常组织的靶向毒性。反之,当表位选择不当时,ADC能轻易结合正常组织的Nectin-4,加重靶向毒性,如皮肤毒性和眼部毒性,严重时可能导致失明和致死性皮肤不良反应。
近期迈威生物在Journal of Biological Chemistry上发表了其在研ADC品种9MW2821与Nectin-4复合物的抗原-抗体结构和结合表位[4]。研究人员通过冷冻电镜技术解析了9MW2821与Nectin-4复合物结构,其分辨率达到3.26Å(图4)。研究结果显示,9MW2821与Nectin-4结合的表位与Nectin-4同源二聚体、Nectin-4/Nectin-1异源二聚体结合表位重叠,提示9MW2821可能因空间位阻无法与正常组织中的Nectin-4结合。这种特性使其能有效区分正常组织与肿瘤细胞——后者因Nectin-4大量表达且存在形式不同,表位更易暴露,从而在保证疗效的同时,从结构设计上源头性地降低了正常组织靶向毒性风险。
9MW2821抗原结合表位的选择还涉及了另一免疫检查点抑制剂TIGIT。TIGIT在肿瘤浸润淋巴细胞中上调表达,通过抑制T细胞和NK细胞功能来产生免疫抑制性肿瘤微环境,在NK细胞上也有表达,而Nectin-4与TIGIT之间的相互作用可抑制NK细胞的细胞毒性[4]。根据迈威生物公布的体外实验数据,9MW2821可阻断Nectin-4与NK细胞上TIGIT结合,增强NK细胞的细胞毒性,表现为CD107a表达增加和IFN-γ的释放增多[5]。这意味着新一代Nectin-4靶向药物可能具备“ADC+免疫疗法”的双重抗肿瘤机制。
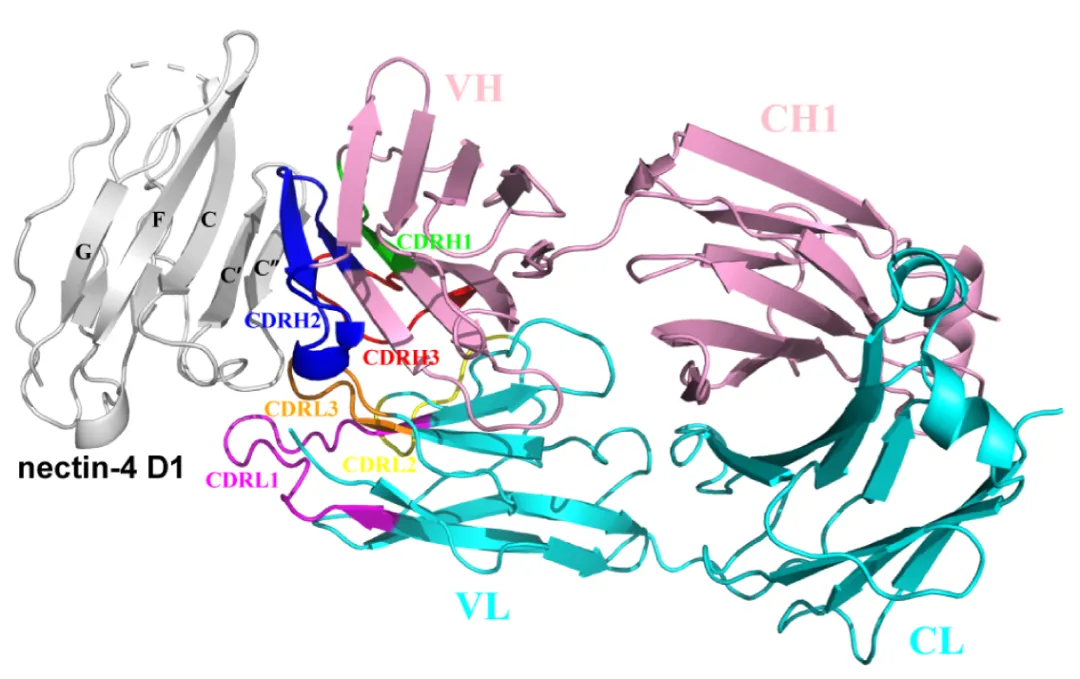
图4 9MW2821和Nectin-4复合物结构[5]
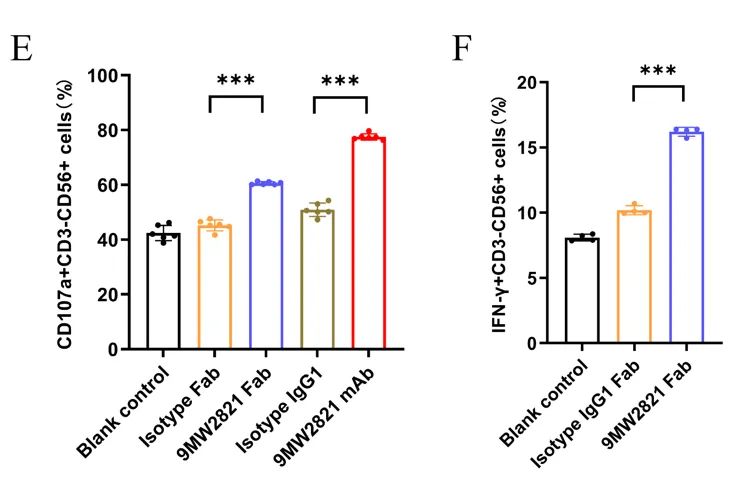
图5 9MW2821增强NK细胞功能[5]
03
安全性的临床答卷
在有效性方面,9MW2821已多次在ESMO、ASCO大会上公布了包括尿路上皮癌、宫颈癌、三阴性乳腺癌、食管癌等适应症的数据,在多个适应症上具备同类最佳潜力。而其在安全性方面的表现也不遑多让。
根据迈威生物公开的1/2期临床(NCT05216965)数据,9MW2821在多个实体瘤中展现出良好的抗肿瘤活性,也披露了一些安全性数据。在接受9MW2821治疗后,常见的(>20%发生率)治疗相关不良反应主要是血液毒性和肝功能异常[7]。从迈威生物公布的临床数据看,9MW2821未见眼部毒性,皮肤毒性仅仅为皮疹和瘙痒,未见PADCEV报道的严重皮肤毒性。
9MW2821与Padcev不良反应对比[8][9][10][11][12]
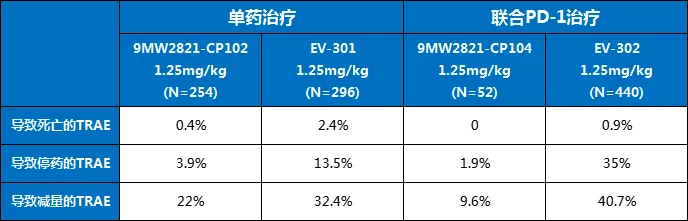
04
结语
抗原表位的选择是决定ADC临床成败的核心环节之一,一个经过科学选择的表位,不仅能确保ADC与肿瘤表面靶标高效结合内化、有效激发抗肿瘤活性,更可最大程度降低对正常细胞的损伤,从源头上降低潜在的靶向毒性。9MW2821的答卷让我们看到了Nectin-4 ADC的更高上限,能否成为这一赛道表位选择的经典案例仍值得期待。

 研发追踪
研发追踪
 医麦客
医麦客  2026-02-12
2026-02-12
 22
22

 研发追踪
研发追踪
 研发客
研发客  2026-02-12
2026-02-12
 20
20

 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2026-02-12
2026-02-12
 20
20