 产业资讯
产业资讯
 BioArt
BioArt  2020-04-20
2020-04-20
 5447
5447
2020年4月15日,美国艺术与科学院院士、美国国家科学院院士、Amgen Research高级副总裁、PROTACs技术创始人之一的Raymond J. Deshaies教授针对制药行业当前的最热门话题“多特异性药物(multispecific drug)”,在Nature杂志上发表题为Multispecific drugs herald a new era of biopharmaceutical innovation的独家综述。该综述简述了现代制药业发展历程,重点对带来第四次制药业革命的多特异性药物进行了全面详实的阐述,并对多特异性药物将来的发展指出方向,也强调了可能存在的挑战。

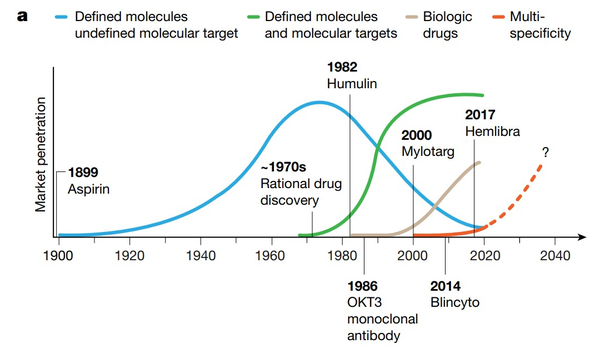
现代生物医药工业发迹于上世纪初,以神药阿司匹林等为标志,此后催生了一大批造福人类的现代药物。直至自上世纪70年代,药物开发都主要依赖于经典的经验药学,此后出现了两个成功的变革创新的浪潮:一个是70年代的理性药物设计方法学,另一个是80年代的基于重组蛋白的治疗药物(图1)。
近年来,多特异性药物崭露头角,造就了新一波浪潮。这些具有前瞻意义的多特异性分子的成功开发让科学家不得不重新思考如何开展靶向性药物的研究和应用。在该综述中,Raymond概述了两类主要的多特异性药物:一种能够在特定位置发挥作用,而另一种则是将治疗药物与生物效应器进行偶联。
以前的药物设计普遍要求药物分子与靶标进行结合并对其进行调节,而第二类多特异性药物则完全脱离了这个约束,使得理论上可以靶向任何蛋白,尤其是那些过去被认为不可成药(undruggable)的靶点。
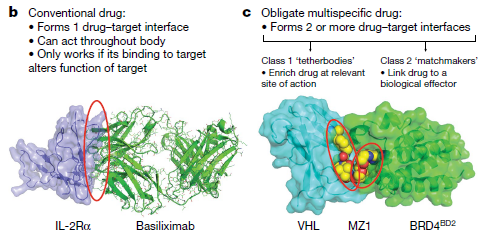
什么是多特异性药物,与经典的理性药物设计有什么区别?如图2左侧所示,理性药物设计一般是先明确一个靶点,然后针对该靶点进行药物筛选和设计,即一个靶点一个药(one target:one drug,1T1D)。药物与靶点直接结合,形成一个明确的药物-靶点结合界面,这种结合需要改变靶点的功能才能发挥作用,或促进靶点功能,或抑制靶点功能。另外,经典药物的一个特点是它们通常在全身都能发挥作用,不具有组织特异性。
与之不同的是,专性多特异性药物则是在经典药物设计的基础上,增加了另外一重功效:要么让药物在特定位点发挥作用(目的主要是减小药物副作用),要么将靶标锚定到细胞的特定效应器旁边,使该效应器对靶标进行调节(能够对那些不可成药的靶标作用)。它的特点主要是形成2个或多个药物-靶点结合界面,如图2右侧所示,MZ1同时结合靶标BRD4和效应器VHL泛素连接酶,让VHL能够对BRD4进行泛素化修饰,然后被蛋白酶体降解。
多特异性药物的分类:Tetherbody(包括SOMs 和COMLs)和Matchmaker(COMMS)。SOM (sequentially obligate multispecific drugs) ,即依序专性多特异性药物,如常见的抗体偶联药物,该多特异性药物首先需要进行锚定到特定位置,如细胞表面的受体,然后药物进入细胞将细胞杀死,其中锚定过程和药物杀死细胞具有先后顺序,因此得名。
COML (Concurrent obligate multispecific drugs that mediate localization) ,即定位向同时专性多特异性药物,与SOMs不同,COML的锚定位点和药物作用靶点在同一位置(比如都定位在细胞膜),锚定过程和对靶点的调节过程同时发生,因此得名。值得注意的是,由于SOM中对靶点进行调节的药物是经过改进,使得其只能在SOM与发生锚定的时候才能与药物靶点进行结合,以避免非特异性效应。
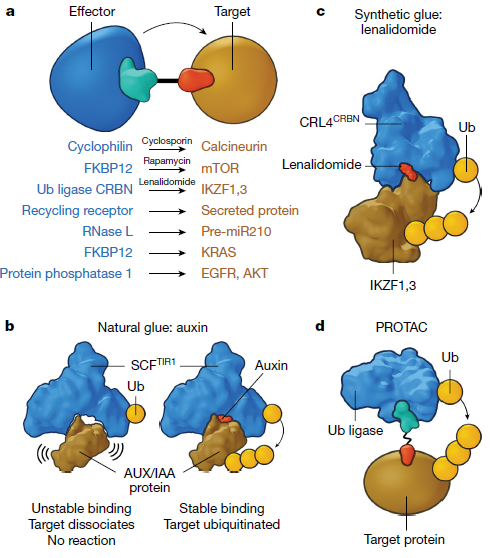
COMMS(Concurrent obligate multispecific drugs that function as molecular matchmakers),即分子匹配向同时专性多特异性药物。与COML不同,COMM的特点不在于定向,而在于实现药物靶点与锚定位点的匹配,使得锚定位点能够对靶点进行调节。COMMS又可以细分为两类,一类是基于小分子的COMM,如分子胶水(molecular glue)和PROTAC(靶向蛋白水解嵌合体,Proteolysis-targeting chimeric molecules)(图3)【1】【2】【3】;另外一类则是基于生物大分子的COMM,如双特异性CD3激动剂BCEs和异源性双功能IgG(图4)。
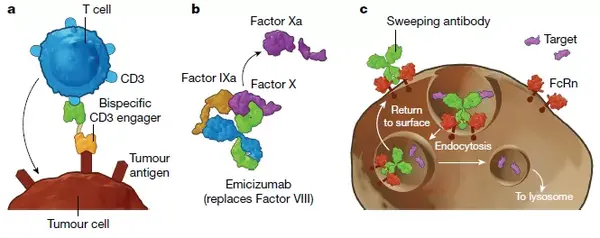
最后,Raymond提出,我们处于变革的边缘,可以预见在不久的将来,我们将看到大量的多特异性药物的诞生,包括基于小分子的和基于生物大分子的,而且这些药物将可能变得越来越复杂,也将获得新的特征。特别是,多特异性小分子,由于其独特的优越性,可望在将来成为众多不可成药靶点的新希望。前途是光明的,但是道路也一样坎坷,前路充满了艰难险阻,如何在确保药物有效性的前提下,降低潜在的安全风险,是迫在眉睫的问题。要想这些前沿研究成果能够落实到临床应用中治病救人,还需要考虑生产的难易程度、药物稳定性、和给药的方便性等,这些迫切问题,还需广大制药人众志成城!

 产业资讯
产业资讯
 米内网
米内网  2025-11-11
2025-11-11
 25
25

 产业资讯
产业资讯
 药智网
药智网  2025-11-11
2025-11-11
 23
23

 产业资讯
产业资讯
 医麦客
医麦客  2025-11-11
2025-11-11
 27
27