 产业资讯
产业资讯
 Insight数据库
Insight数据库  2021-07-13
2021-07-13
 2805
2805
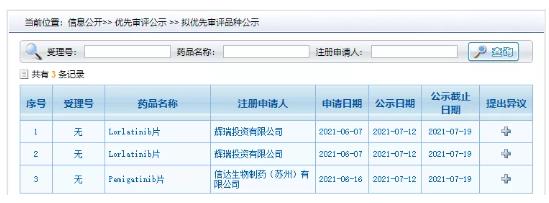
7 月 12 日,CDE 优先审评栏目更新,两款小分子抗癌药拟优先审评:
信达的 FGFR 抑制剂 Pemigatinib,用于既往至少接受过一种系统性治疗的 FGFR2 融合或重排的晚期、转移性或不可手术切除的胆管癌成人患者的治疗;
辉瑞的第三代 ALK 抑制剂劳拉替尼(Lorlatinib),用于既往接受过一种或多种 ALK-TKI 治疗的 ALK 阳性局部晚期或转移性非小细胞肺癌 (NSCLC) 患者。
信达 FGFR 抑制剂
Pemigatinib 由 Incyte 和信达生物共同开发,2018 年 12 月,两家公司达成战略合作,信达生物负责中国大陆、香港、澳门和台湾地区的商业化。目前,pemigatinib 已经在美国、欧洲、日本以及台湾市场获批上市;上周五,信达宣布在国内递交了 pemigatinib 的上市申请获受理(受理号 JXHS2101026/7/8),今日拟纳入优先审评。
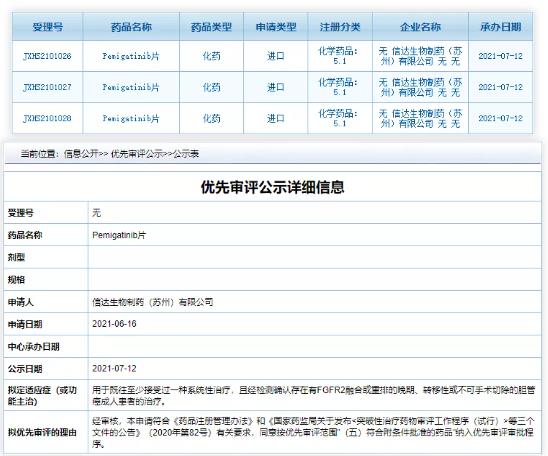
Pemigatinib 在国内的上市申请是基于一项在既往经过至少一线系统性治疗失败的、伴 FGFR2 融合或重排的、手术不可切除的局部晚期、复发性或转移性胆管癌受试者中评价 pemigatinib 的疗效和安全性的 II 期、开放性、单臂、多中心的研究,即 CIBI375A201 研究(NCT04256980)。这项研究是国外的 FIGHT-202 研究(NCT02924376)的桥接试验,其主要终点为基于独立影像委员会(IRRC)根据实体瘤评价标准 V1.1 评价的客观缓解率(ORR)。
在 FIGHT- 202 研究中,共入组 108 例胆管癌受试者,接受 pemigatinib 13.5 mg 口服治疗,其中基于 IRRC 评估的已确认的 ORR 为 37%(95% CI:27.94%,46.86%),包括 4 例完全缓解(3.7%)和 36 例部分缓解(33.3%),中位缓解持续时间(DOR)为 8.08 个月(95% CI:5.65,13.14),中位无进展生存期(PFS)为 7.03 个月(95% CI:6.08,10.48),pemigatinib 可引起持久的肿瘤缓解,中位总生存期(OS)达 17.48 个月(95% CI:14.42,22.93)。
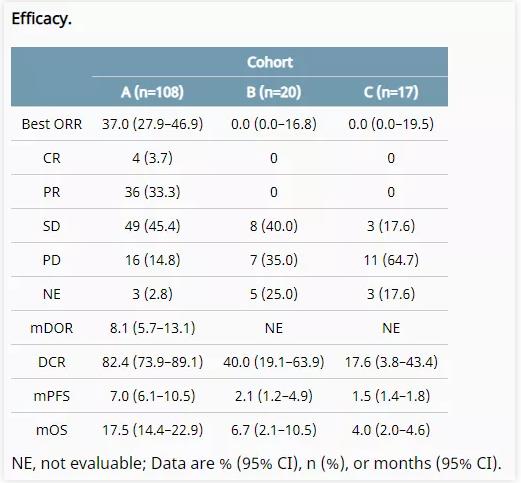
DOI: 10.1200/JCO.2021.39.15_suppl.4086
Journal of Clinical Oncology 39, no. 15_suppl (May 20, 2021) 4086-4086.
安全性方面,pemigatinib 具有良好的耐受性。在 147 例纳入安全性分析的受试者中,高磷酸血症为最常见的不良反应,发生率为 58.5%。有 68.7% 的受试者发生 3 级或 3 级以上的不良反应,最常报告的为低磷酸血症(14.3%),其他包括关节痛和口腔黏膜炎(各 6.1%)、腹痛、疲乏和低钠血症(均为 5.4%),其他还有掌跖红肿综合征和低血压,发生率分别为 4.8% 和 4.1%。
胆管癌是一种起源于胆管上皮细胞的恶性肿瘤,是第二常见的原发于肝脏的恶性肿瘤。由于乙肝病毒及其他肝脏寄生虫的感染,胆管癌在亚洲地区发病率较高,因此亟待有竞争力的新疗法为患者带来临床获益。
辉瑞 ALK 抑制剂
劳拉替尼(Lorlatinib)是一种具中枢神经系统穿透力的第三代 ALK/ROS1 酪氨酸激酶抑制剂(TKI)。2018 年 11 月,劳拉替尼获 FDA 批准用于既往接受过一线及以上治疗的 ALK 阳性晚期/转移性 NSCLC 患者;2021 年 3 月,劳拉替尼再次获 FDA 批准一线治疗 ALK 阳性晚期/转移性 NSCLC。而在国内,辉瑞在今年 4 月份刚刚递交劳拉替尼上市申请获 CDE 受理。
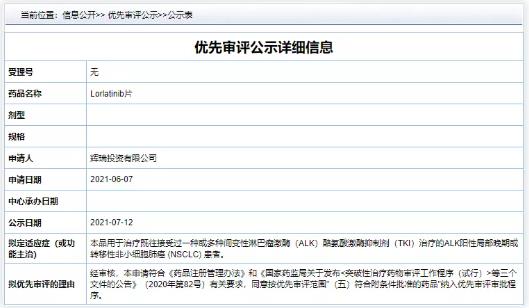
ALK(间变性淋巴瘤激酶)是肺癌靶向治疗中的一个重要靶点,是 NSCLC 重要的致癌驱动因子之一,被称为「钻石突变」,在 NSCLC 中的发生率为 4% ~ 7%。
目前全球已经获批 6 款 ALK 抑制剂,一代 ALK-TKI 克唑替尼(crizotinib,辉瑞);二代 ALK-TKI 赛瑞替尼 (ceritinib,诺华) 、阿来替尼 (alectinib,罗氏)、布加替尼 (brigatinib,武田),以及国内贝达药业的恩沙替尼;三代 ALK-TKI 劳拉替尼(Lorlatinib)。而在国内,除处于上市申请阶段的布加替尼和劳拉替尼外,其他 4 款均已获批。
根据 Insight 数据库,目前劳拉替尼已有多条临床试验结果数据在期刊或医学会议中公布。其中值得注意的是,CROWN 研究结果显示,与克唑替尼相比,劳拉替尼一线治疗 ALK 阳性晚期 NSCLC 表现出了显著的临床获益。
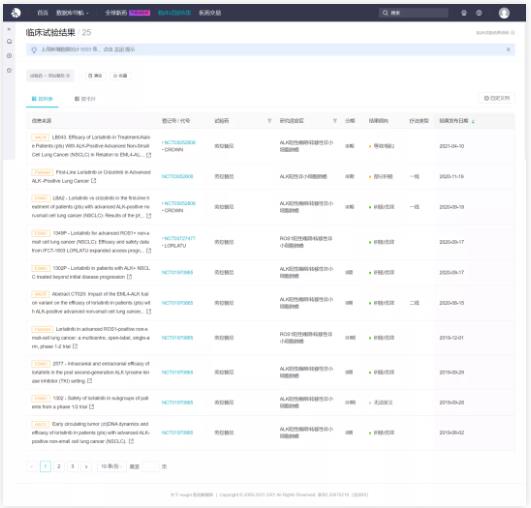
*图中包括同登记号不同数据截止时间的临床结果,篇幅有限仅展示 10 条
本次劳拉替尼在国内申报上市,为首款申报的三代 ALK-TKI。同时,今年 6 月 15 日辉瑞还和基石药业宣布达成合作,在国内展开合作研究,共同开发劳拉替尼用于 ROS1 阳性晚期 NSCLC。

 产业资讯
产业资讯
 医药魔方Invest
医药魔方Invest  2025-08-19
2025-08-19
 17
17
 产业资讯
产业资讯
 药研网
药研网  2025-08-19
2025-08-19
 17
17

 产业资讯
产业资讯
 药视声
药视声  2025-08-19
2025-08-19
 20
20