 产业资讯
产业资讯
 生物药大时代
生物药大时代  2021-12-28
2021-12-28
 2648
2648
据不完全统计,2021年全球批准了多款可以冠以“首个”药物,包括新靶点药物、新疗法等。
2021年全球至少批准7个新靶点药物,详见下表。
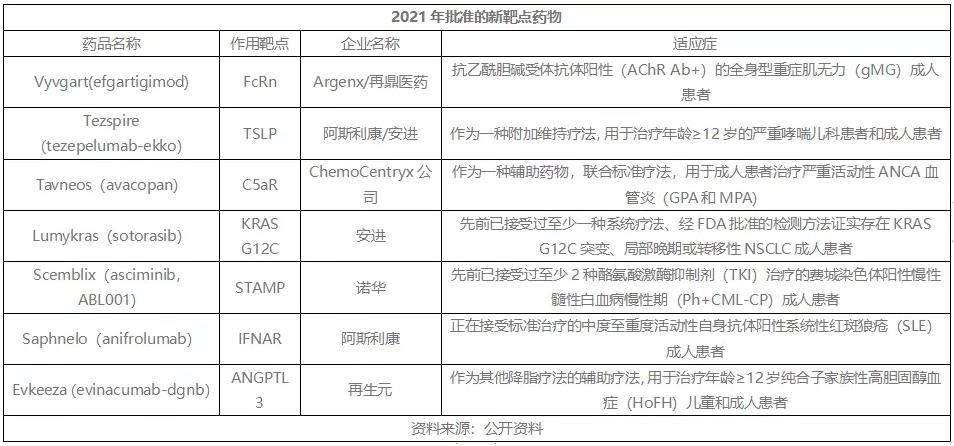
Vyvgart(efgartigimod)是全球批准的首个新生儿Fc受体(FcRn)拮抗剂,12月被FDA批准用于治疗抗乙酰胆碱受体抗体阳性(AChR Ab+)的全身型重症肌无力(gMG)成人患者。
Tezspire(tezepelumab)是首款获批的抗胸腺间质淋巴细胞生成素(TSLP)单抗,12月被FDA批准作为一种附加维持疗法,用于治疗年龄≥12岁的严重哮喘儿科患者和成人患者。
Tavneos是首款获批的口服给药选择性补体C5a受体(C5aR)抑制剂,9月在日本被批准与标准疗法联用,辅助治疗两种主要的抗中性粒细胞胞浆自身抗体(ANCA)相关血管炎:显微镜下多血管炎(MPA)和肉芽肿伴多血管炎(GPA)。
Lumakras/Lumykras(sotorasib)是首款获批的针对KRAS G12C突变的靶向疗法,5月在美国被批准用于治疗先前已接受过至少一种系统疗法、经FDA批准的检测方法证实存在KRAS G12C突变、局部晚期或转移性NSCLC成人患者。
Scemblix活性药物成分asciminib是一款STAMP抑制剂,特异性靶向BCR-ABL1蛋白肉豆蔻酰口袋(STAMP),将BCR-ABL1锁定为非活性构象。而目前已上市的竞争药物,是通过与BCR-ABL1蛋白的ATP结合位点结合。10月,该药被FDA批准用于治疗先前已接受过至少2种酪氨酸激酶抑制剂(TKI)治疗、费城染色体阳性慢性髓性白血病慢性期(Ph+CML-CP)成人患者。
Saphnelo是一种首创I型干扰素受体(IFNAR)抗体,8月被FDA批准用于治疗正在接受标准治疗的中度至重度系统性红斑狼疮(SLE)成人患者,也是过去10年来FDA唯一批准的SLE新疗法。
Evkeeza是FDA批准的第一种靶向结合并阻断血管生成素样蛋白3(ANGPTL3)功能的药物,2月被FDA批准作为其他降脂疗法的辅助疗法,用于治疗年龄≥12岁纯合子家族性高胆固醇血症(HoFH)儿童和成人患者。
而且,CAR-T疗法和ADC药物也迎来了新靶向药物。
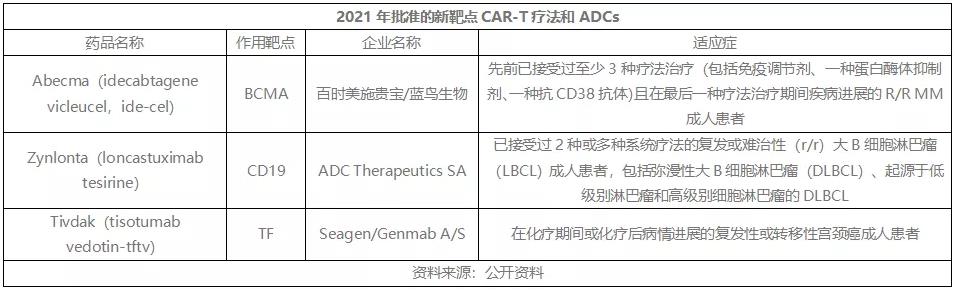
Abecma是全球批准的首款B细胞成熟抗原(BCMA)靶向CAR-T疗法,3月被FDA批准用于治疗既往接受过三种以上疗法的成人复发/难治性多发性骨髓瘤(R/R MM)。
Zynlonta是第一个获批的CD19靶向抗体偶联药物(ADC),4月被FDA批准用于治疗已接受过2种或多种系统疗法的复发或难治性(r/r)大B细胞淋巴瘤(LBCL)成人患者,包括弥漫性大B细胞淋巴瘤(DLBCL)、起源于低级别淋巴瘤和高级别细胞淋巴瘤的DLBCL。
Tivdak是全球批准的首款组织因子(TF)靶向抗体药物偶联物(ADC),9月被FDA批准用于治疗在化疗期间或化疗后病情进展的复发性或转移性宫颈癌成人患者。
此外,2021年一些疾病还获批了新作用机制药物。
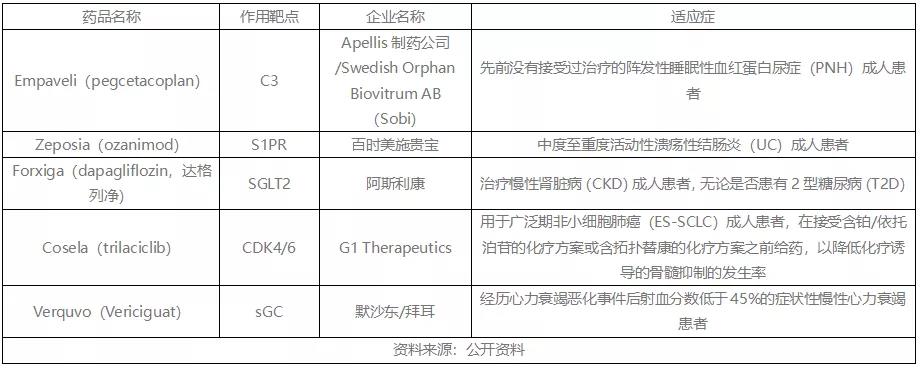
Empaveli是获得监管批准的第一个治疗PNH的C3靶向疗法,5月被FDA批准用于先前没有接受过治疗的PNH成人患者,以及从C5抑制剂(Soliris和Ultomiris)转换治疗的PNH成人患者。
Zeposia是第一个被批准治疗溃疡性结肠炎(UC)的口服鞘氨醇-1-磷酸(S1P)受体调节剂,5月被FDA批准用于治疗成人中重度活动性结肠炎(UC)。此前该药于2020年3月被FDA批准用于治疗成人复发型多发性硬化症(RMS),包括临床孤立综合征、复发缓解型疾病和活动性继发性进展性疾病。
Farxiga/Forxiga于4月被FDA批准用于治疗慢性肾脏病(CKD)成人患者,无论是否患有2型糖尿病(T2D),是第一个被批准治疗慢性肾脏病(CKD)患者(无论是否患有T2D)的SGLT2抑制剂。
Cosela是一种首创的短效CDK4/6抑制剂,2月被FDA批准用于广泛期非小细胞肺癌(ES-SCLC)成人患者,在接受含铂/依托泊苷的化疗方案或含拓扑替康的化疗方案之前给药,以降低化疗诱导的骨髓抑制的发生率,成为全球第一款可降低化疗诱导的骨髓抑制发生率的骨髓保护疗法。
Verquvo是第一个被批准用于治疗心力衰竭的可溶性鸟苷酸环化酶(sGC)刺激剂,1月被FDA批准用于射血分数<45%的有症状的慢性心力衰竭患者,降低发生恶化心力衰竭事件(定义为:心力衰竭住院或在未住院的情况下接受门诊静脉[IV]利尿剂治疗心力衰竭)后的心血管死亡和心衰住院的风险。
而且,2021年全球多种疾病迎来了新疗法。
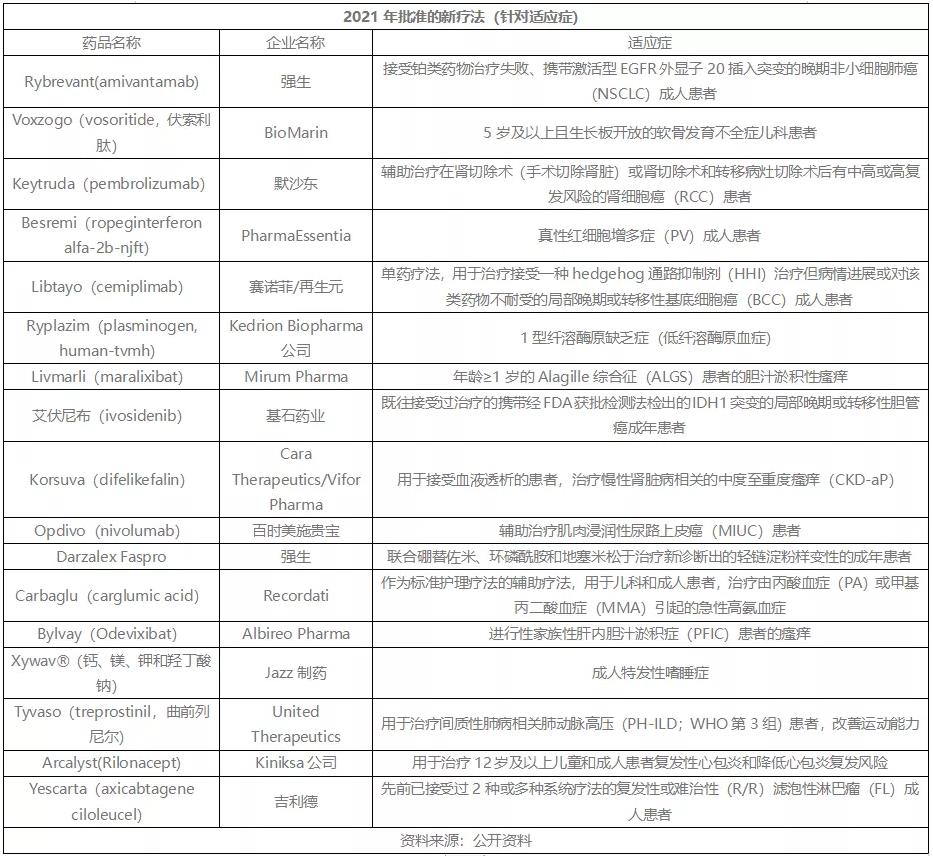
Rybrevant (Amivantamab-vmjw)一种具有免疫细胞导向活性的EGFR-MET双特异性抗体,5月被FDA批准用于治疗在接受含铂化疗失败后病情进展、EGFR基因外显子20插入突变阳性(EGFRex20ins+)的转移性非小细胞肺癌(mNSCLC)成人患者,成为全球首款获批治疗EGFRex20ins+ NSCLC的靶向疗法。
Voxzogo是一种每日注射一次的C型利钠肽(CNP)类似物,11月被FDA加速批准用于治疗5岁及以上且生长板开放的软骨发育不全症儿科患者,增加线性生长,是全球第一个被批准治疗软骨发育不全症儿童患者的药物,可治疗疾病的根本原因。
Keytruda于11月被FDA批准用于辅助治疗在肾切除术(手术切除肾脏)或肾切除术和转移病灶切除术后有中高或高复发风险的肾细胞癌(RCC)患者,是第一个被批准用于辅助治疗上述RCC患者的免疫疗法。
Besremi是一种创新的单PEG化长效干扰素,11月被FDA批准用于治疗真性红细胞增多症(PV)成人患者,成为FDA批准的第一种治疗PV的药物(无论患者有无治疗史均可使用),同时也是第一种专门批准用于治疗PV的干扰素疗法。
Libtayo是第一个获批治疗晚期基底细胞癌(BCC)的免疫疗法,2月被FDA批准作为单药疗法,用于治疗接受一种hedgehog通路抑制剂(HHI)治疗但病情进展或对该类药物不耐受的局部晚期或转移性BCC成人患者。
Ryplazim的活性成分为纤溶酶原,从人血浆中提取纯化。6月,该药被FDA批准用于治疗1型纤溶酶原缺乏症(低纤溶酶原血症)患者,成为FDA批准的第一个治疗纤溶酶原缺乏症的药物。
Livmarli口服液活性药物成分maralixibat是一种口服给药、具有最小化吸收的回肠胆汁酸转运体(IBAT)抑制剂,10月被FDA批准用于治疗年龄≥1岁的Alagille综合征(ALGS)患者的胆汁淤积性瘙痒,是第一个被批准用于治疗ALGS胆汁淤积性瘙痒的药物。
艾伏尼布成是全球首个获FDA批准用于IDH1突变胆管癌患者靶向治疗的药物,8月被FDA批准用于既往接受过治疗的携带经FDA获批检测法检出的IDH1突变的局部晚期或转移性胆管癌成年患者。
Korsuva活性药物difelikefalin是一种首创外周κ阿片受体(KOR)激动剂,8月被FDA批准用于接受血液透析的患者,治疗慢性肾脏病相关的中度至重度瘙痒(CKD-aP),成为FDA批准的第一个治疗血液透析成人患者慢性肾脏病相关瘙痒的药物,有潜力从根本上改变接受透析的成人患者CKD-aP的治疗模式。
Opdivo是第一个在辅助治疗中被批准用于治疗尿路上皮癌(UC)的PD-1抑制剂,8月被FDA批准用于辅助治疗肌肉浸润性尿路上皮癌(MIUC)患者,具体为:进行根治性切除后有高复发风险、无论之前是否进行了新辅助化疗或淋巴结受累或PD-L1状态的MIUC患者。
Darzalex Faspro于1月被FDA加速批准与硼替佐米、环磷酰胺、地塞米松联合用药(D-VCd方案),用于治疗新诊断的轻链(AL)淀粉样变性成人患者,成为首个治疗AL淀粉样变性的药物。
Carbaglu作为N-乙酰谷氨酸(NAG)的替代物,通过激活氨甲酰磷酸合成酶(CPS 1),改善或恢复尿素循环功能,促进氨解毒和尿素生成。1月,该药被FDA批准作为标准护理疗法的辅助疗法,用于儿科和成人患者,治疗由丙酸血症(PA)或甲基丙二酸血症(MMA)引起的急性高氨血症,成为第一个获FDA批准治疗PA和MMA引起的急性高氨血症药物。
Bylvay是一种强效、非全身性回肠胆汁酸转运抑制剂,7月获欧盟批准,成为全球第一个被批准用于治疗进行性家族性肝内胆汁淤积症(PFIC)所有亚型的药物。
Xywav是专门为发作性睡病患者提供低钠羟丁酸疗法而开发的产品,具有一种独特的阳离子组分(钙镁钾钠),可大大减少患者服药后的慢性钠负荷,8月被FDA批准用于治疗成人特发性嗜睡症,是FDA批准的首个用于治疗特发性嗜睡症新药。
Tyvaso活性药物曲前列尼尔是一种人工合成的前列环素模拟物,主要通过直接舒张肺和全身动脉血管床并抑制血小板聚集发挥作用。6月,Tyvaso吸入性溶液被FDA批准用于治疗间质性肺病相关肺动脉高压(PH-ILD;WHO第3组)患者,改善运动能力,成为美国首个获批治疗PH-ILD的疗法。
Arcalyst是一种每周一次的、皮下注射重组融合蛋白,可阻断白细胞介素-1α(IL-1α)和白细胞介素-1β(IL-1β)信号,3月被FDA批准用于治疗12岁以上复发性心包炎患者和减轻心包炎的复发风险,是FDA批准的首个治疗复发性心包炎的药物。
Yescarta是一款CD19靶向CAR-T疗法,3月被FDA批准用于治疗先前已接受过2种或多种系统疗法的复发性或难治性(R/R)滤泡性淋巴瘤(FL)成人患者,成为第一款被批准用于治疗惰性FL的CAR-T疗法。
而且,一些疾病还迎来了新的给药方式。
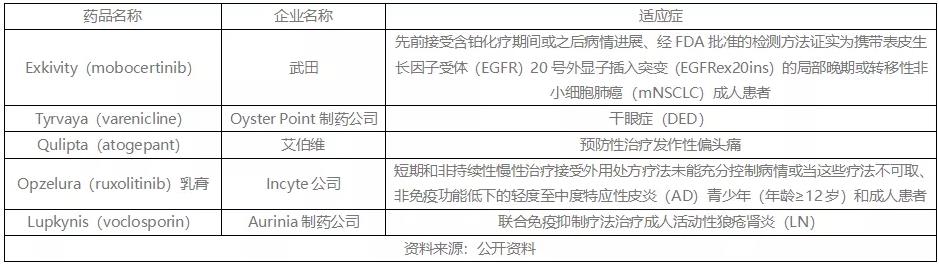
Exkivity是一款专门设计用于EGFRexon20 插入突变的口服酪氨酸激酶抑制剂 (TKI),9月被FDA批准用于治疗先前接受含铂化疗期间或之后病情进展、经FDA批准的检测方法证实为携带EGFRex20ins突变的局部晚期或转移性非小细胞肺癌成人患者,是首款获批治疗EGFRexon20 NSCLC的口服靶向疗法。
Tyrvaya鼻喷雾剂是一种高选择性胆碱能激动剂,10月被FDA批准用于治疗干眼症(DED)的症状和体征,成为第一款被批准用于治疗干眼症的鼻喷雾剂。
Qulipta是第一个也是唯一一个专门为偏头痛预防性治疗而开发的口服降钙素基因相关肽(CGRP)受体拮抗剂,10月被FDA批准用于成人预防性治疗发作性偏头痛。
Opzelura是FDA批准的第一个外用Janus激酶抑制剂,9月被FDA批准用于短期和非持续性慢性治疗接受外用处方疗法未能充分控制病情或当这些疗法不可取、非免疫功能低下的轻度至中度特应性皮炎(AD)青少年(年龄≥12岁)和成人患者。
Lupkynis(voclosporin)是一种新型、潜在同类最佳的钙调神经磷酸酶抑制剂(CNI),1月被FDA批准联合背景免疫抑制治疗方案,用于治疗活动性狼疮性肾炎(LN)成人患者,成为FDA批准的第一个治疗LN的口服疗法。

 产业资讯
产业资讯
 一度医药
一度医药  2025-07-18
2025-07-18
 34
34

 产业资讯
产业资讯
 药渡Daily
药渡Daily  2025-07-18
2025-07-18
 36
36

 产业资讯
产业资讯
 医药魔方Invest
医药魔方Invest  2025-07-18
2025-07-18
 34
34