 产业资讯
产业资讯
 医药经济报
医药经济报  2023-09-12
2023-09-12
 5095
5095
荣昌生物泰它西普新适应症上市申请获受理
9月7日,荣昌生物注射用泰它西普的新适应症上市申请获CDE受理,用于治疗类风湿性关节炎(RA)。

类风湿关节炎(RA)是一种慢性自身免疫性疾病,以侵蚀性关节炎为主要特征。发病初期的关节表现为关节晨僵、肿胀、疼痛等,最后可发生关节畸形,并丧失关节正常的功能,严重影响患者生活质量。
中国RA的患病率在0.32%-0.36%之间,发病率较高。当前标准治疗以抗炎类、糖皮质激素、传统免疫抑制剂及TNF-α抑制剂等药物为主,对于上述疗法无效或不耐受的患者而言,存在尚未满足的临床需求。
泰它西普(RC18,商品名:泰爱)是荣昌生物自主研发的用于治疗自身免疫性疾病的新型融合蛋白,由人跨膜激活剂及钙调节剂和亲环蛋白配体相互作用因子(TACI)受体的胞外域以及人免疫球蛋白G(IgG)的可结晶片段(Fc)域构成。
泰它西普靶向两类对B淋巴细胞发育至关重要的细胞信号分子:B淋巴细胞刺激因子(BLyS)和增殖诱导配体(APRIL),得以有效降低B细胞介导的多种自身免疫性疾病。
荣昌生物宣布已经完成了泰它西普在中国治疗RA患者的Ⅲ期研究,获得了相关数据结果。
泰它西普已于2021年3月正式获得中国国家药品监督管理局(NMPA)在中国的附条件上市的批准,用于治疗系统性红斑狼疮(SLE),并于当年被纳入更新后的国家医保目录(NRDL)。
恒瑞医药引进创新药林普利塞新适应症上市申请获受理
9月7日,林普利塞新适应症上市申请获CDE受理,用于治疗复发和/或难治性外周T细胞淋巴瘤(R/R PTCL)患者。

PTCL是一类来源于胸腺后不同阶段T淋巴细胞的恶性肿瘤,亚洲国家更多见,约占所有淋巴瘤的21.4%,明显高于欧美国家(约10%)。PTCL患者治疗选择有限,现有治疗的疗效低,持续时间短,R/R PTCL患者治疗选择更为有限,目前尚无标准治疗方案,预后极差,3年总生存期(OS)<30%。因此,R/R PTCL治疗领域仍存在未被满足的临床需求,亟需高效且安全的治疗药物为R/R PTCL患者的治疗打开新局面。
林普利塞为恒瑞医药引进的1类新药,是由合作方璎黎药业自主研发的靶向PI3Kδ的高选择性小分子抑制剂。
此次申报新适应症上市,是基于一项单臂、多中心的II期注册性临床研究CTR20210333,旨在评估林普利塞治疗R/R PTCL的疗效和安全性。此研究的主要终点是由独立数据评估委员会(IRC)评估的总缓解率(ORR)。其初步数据显示,林普利塞治疗R/R PTCL疗效良好,安全性整体可控,有望成为更多R/R PTCL患者的治疗新选择。
默沙东九价人乳头瘤病毒疫苗新适应证上市获受理
9月5日,CDE官网显示,默沙东九价人乳头瘤病毒疫苗(酿酒酵母)(佳达修9)新适应证上市申请获受理,据了解,此次申报的新适应证主要是用于男性接种。
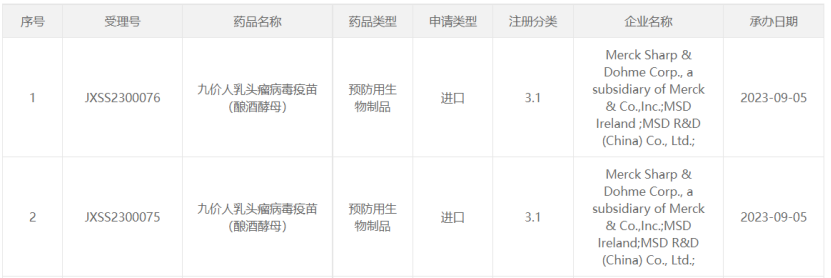
人乳头瘤病毒(HPV)是一项极为常见的引起生殖道病毒性感染的病毒,传播方式主要为性接触传播,而且该病毒还可以通过接触已感染的生殖器皮肤、黏膜或体液而传播。临床上,HPV持续感染不仅是女性宫颈癌、外阴癌和阴道癌的主要诱因,同时也可以造成尖锐湿疣、肛门癌以及头颈癌等男女共患疾病。
数据显示,在全球范围内,女性人群中HPV感染率峰值为24%,男性人群中生殖器HPV总体感染率高达45.2%。默沙东九价HPV疫苗男性适应证已在国外获批。
2018年4月,“佳达修9”首次在中国获批上市,用于16岁至26岁女性的预防接种,2022年8月获药监局批准扩龄,适用人群拓展至9岁-45岁适龄女性。
公开资料显示,2021年默沙东在中国启动了关于评价九价HPV疫苗在男性中的保护效力、免疫原性和安全性的三期临床试验。3项试验累计入组人数达到18690人之多,也覆盖9岁至45岁年龄层,具体包括:9岁到14岁男性的2剂疗法、9岁到19岁男性的3剂疗法;18岁至45岁男性;20岁至45岁男性。

 产业资讯
产业资讯
 药智网
药智网  2026-05-28
2026-05-28
 608
608

 产业资讯
产业资讯
 珍立拍
珍立拍  2026-05-28
2026-05-28
 666
666

 产业资讯
产业资讯
 药明康德
药明康德  2026-05-28
2026-05-28
 531
531
 热门资讯
热门资讯