 研发追踪
研发追踪
 UmabsDB
UmabsDB  2025-05-19
2025-05-19
 3396
3396
Umabs DB作为目前全球最全面的抗体药物专业数据库,收录全球近10000个从临床前到商业化阶段抗体药物,涉及靶点1600+,涉及疾病种类2400+,研发机构2900+,覆盖药物蛋白序列、专利和临床等多种专业信息。Umabs DB药物数据库已正式开放上线,可访问www.umabs.com注册享受7天免费试用。
2025年5月15日,专注与LAG3疗法开发的Immutep,更新了一项LAG-3融合蛋白eftilagimod alpha(efti),联合PD-1抗体Pembrolizumab用于一线非鳞状非小细胞肺癌治疗的,一项研究者发起的临床实验INSIGHT-003的初步积极结果,这也是其在继头颈鳞癌(中位OS达到17.6个月,股票大涨45%:Immutep更新LAG-3联合K药头颈鳞癌数据)后的再次突破。

截至 2025 年 5 月 6 日,51例可评估患者显示,联合疗法取得了60.8% 的客观反应率和 90.2% 的疾病控制率。值得注意的是,该研究中,~92% 的可评估患者PD-L1 TPS <50%,这其中PD-L1 TPS 1-49% 的患者为49%,TPS<1%的患者为43%,但仍然保持较高的客观响应率,并显著高于Pembrolizumab+化疗的历史数据。
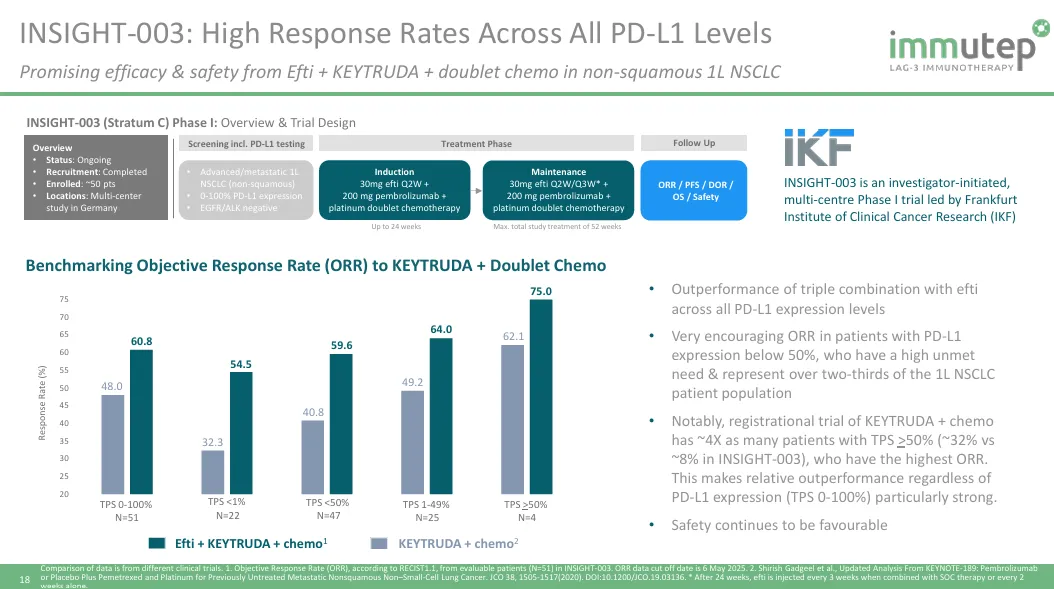
初步的PFS和OS的数据显示,eftilagimod alpha(efti)+Pembrolizumab的联合疗法分别达到了12.7个月和32.9个月,均优于Pembrolizumab+化疗的历史数据。
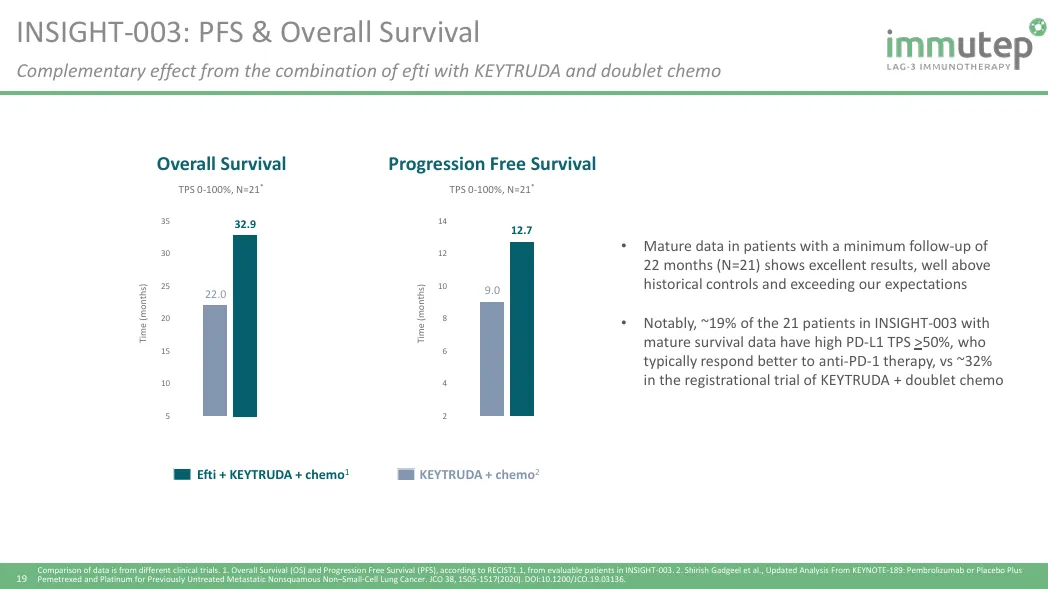
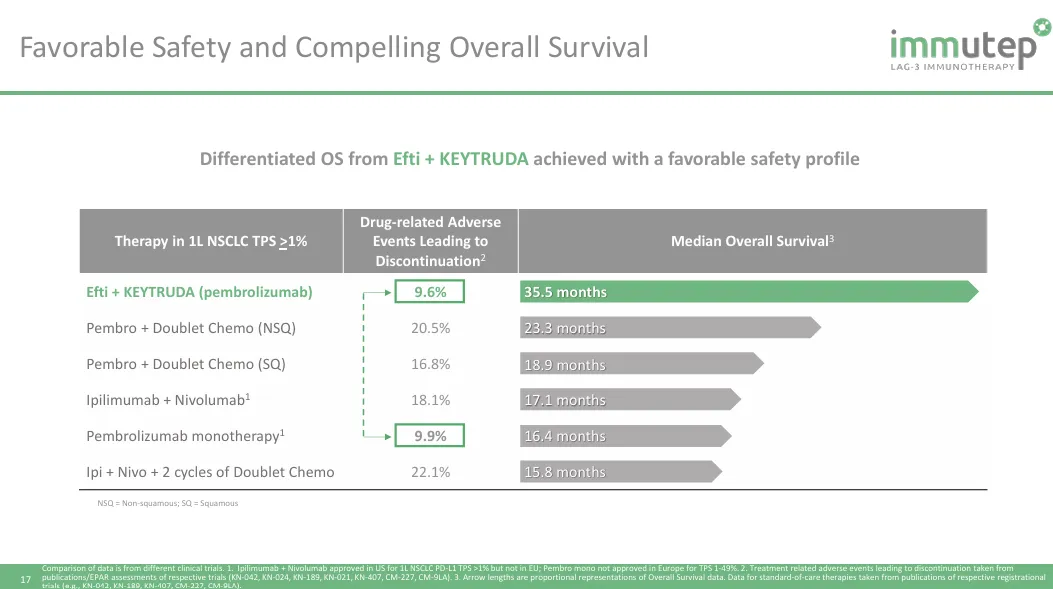
此前的2023年ESMO会议期间,Immutep也报道过eftilagimod alpha(efti)+Pembrolizumab用于一线非小细胞肺癌治疗的二期临床ACTI-002的数据。联合疗法的总体客观响应率达到40.4%,同样对于PD-L1的表达量依赖性不高,TPS<1%客观响应率略低一些,但仍然比较可观。PFS和OS数据,相对于Pembrolizumab的单药疗法,同样提升显著,特别是中位OS翻倍达到35.5个月。
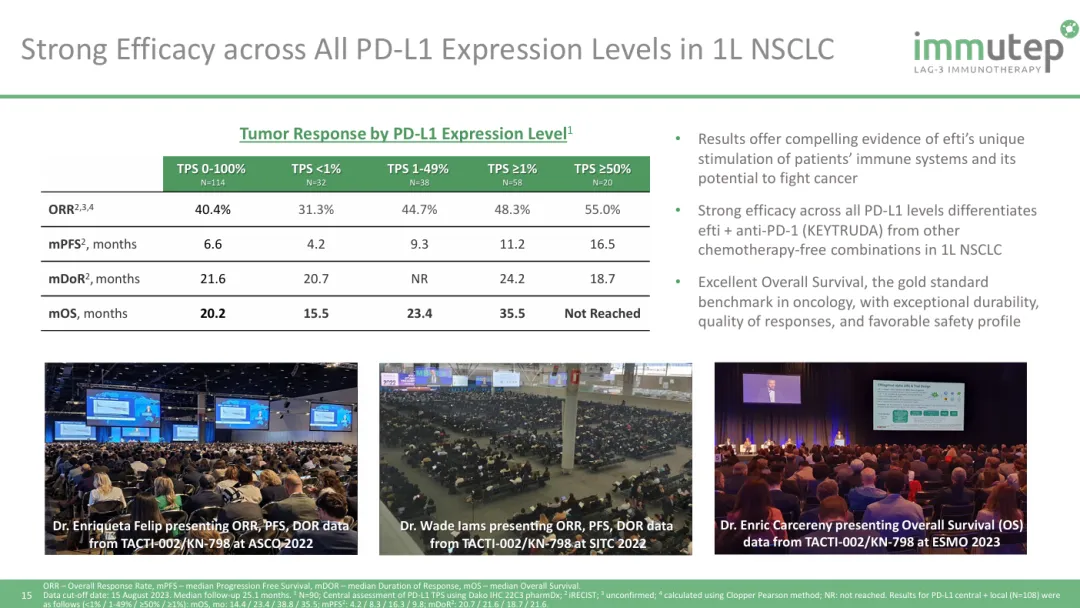
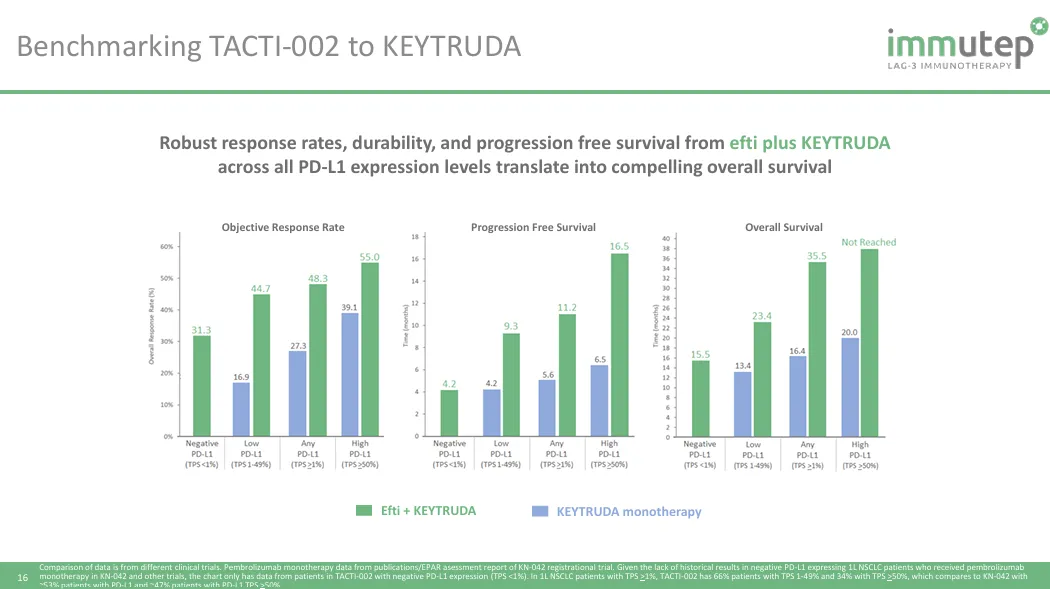
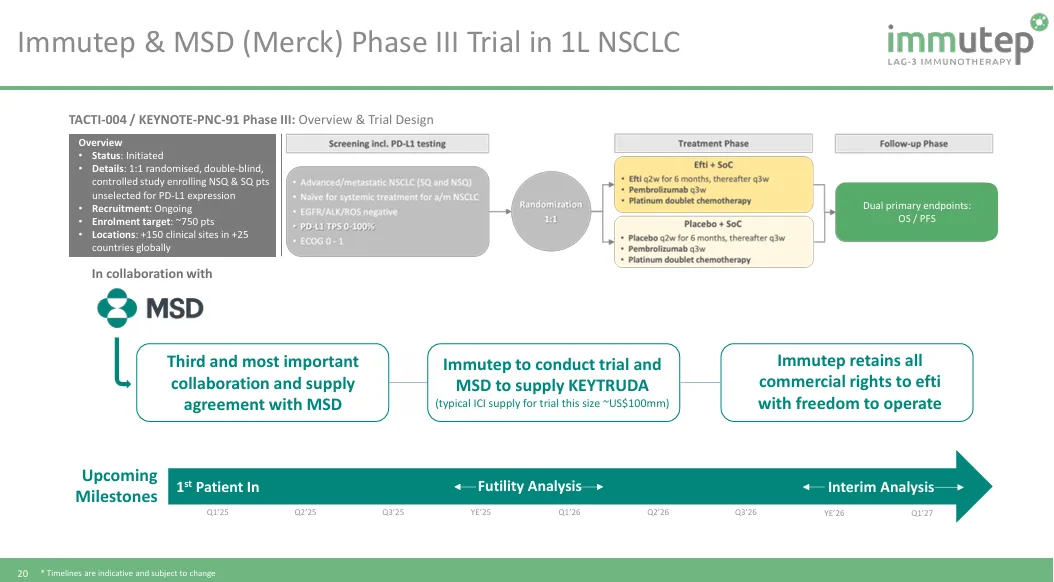
基于以上初步积极临床数据,Immutep和默沙东已经于今年初启动一项注册性三期临床试验TACTI-004/KEYNOTE-PNC-91,和Pembrolizumab+化疗进行头对头比对,并不对PD-L1的表达量进行限制,预计入组750例患者,PFS和OS作为双主要临床试验终点。
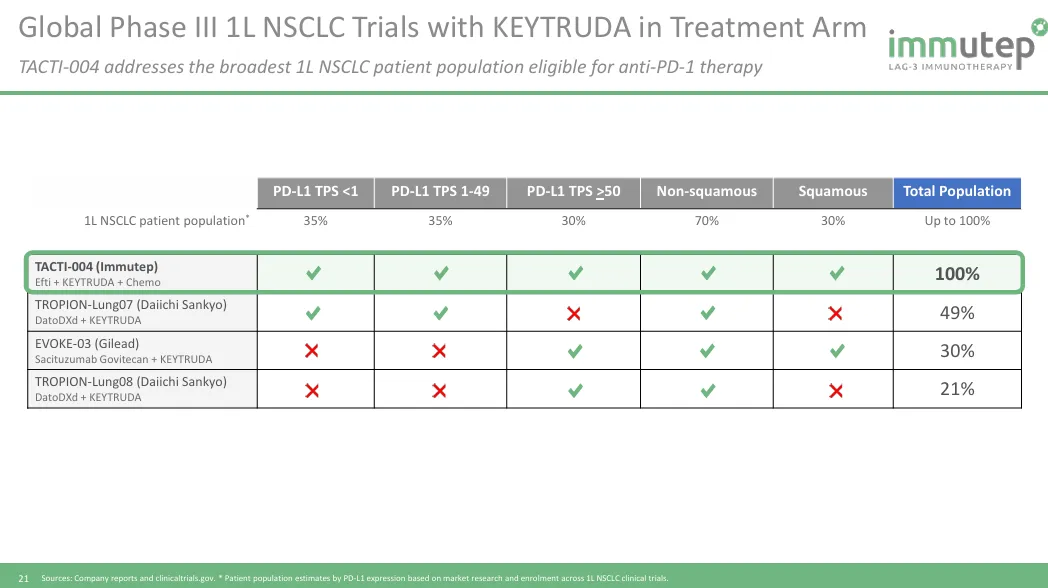
基于该临床不对PD-L1进行限制,其也将具有全面取代Pembrolizumab+化疗在一线非小细胞肺癌统治地位的潜力,比当前多个ADC药物的覆盖人群都要广。
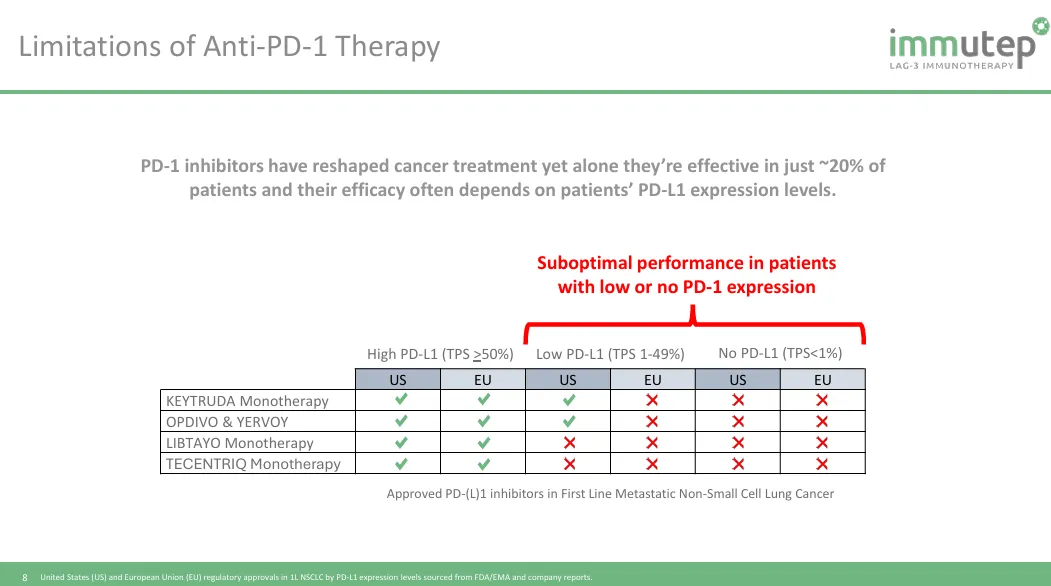
里程碑式的PD-1/PD-L1抗体药物开发十多年以来,已经在PD-L1领域建立相对强势的治疗地位,但在多个肿瘤领域的PD-L1低表达患者仍然疗效不佳,CTLA-4和LAG-3成为唯一两个被证明协同作用的免疫检查点,扩展部分肿瘤的低PD-L1治疗应用,未来联合疗法、双抗和ADC等新型疗法仍需要继续提升。
原文链接:

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 555
555

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 468
468

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 495
495
 热门资讯
热门资讯