 研发追踪
研发追踪
 新药猎人日记
新药猎人日记  2025-07-14
2025-07-14
 2208
2208
今天,Apogee Therapeutics宣布其在研药物 APG777 在治疗中重度特应性皮炎的 Phase 2 APEX 试验 Part A 部分中取得了令人瞩目的成果,展现了在抗白细胞介素 - 13(IL-13)生物制剂中的卓越潜力。
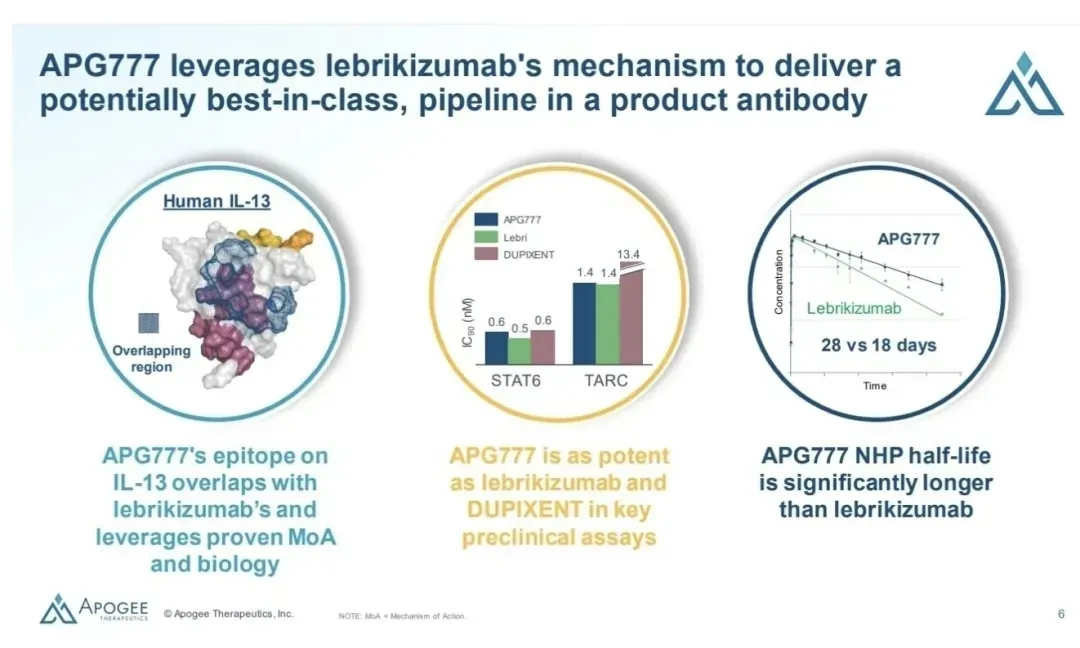
APG777 是 Apogee Therapeutics 公司研发的一种新型抗 IL-13 生物制剂,旨在通过靶向 IL-13 这一关键炎症介质,调节免疫反应,从而减轻特应性皮炎患者的症状。
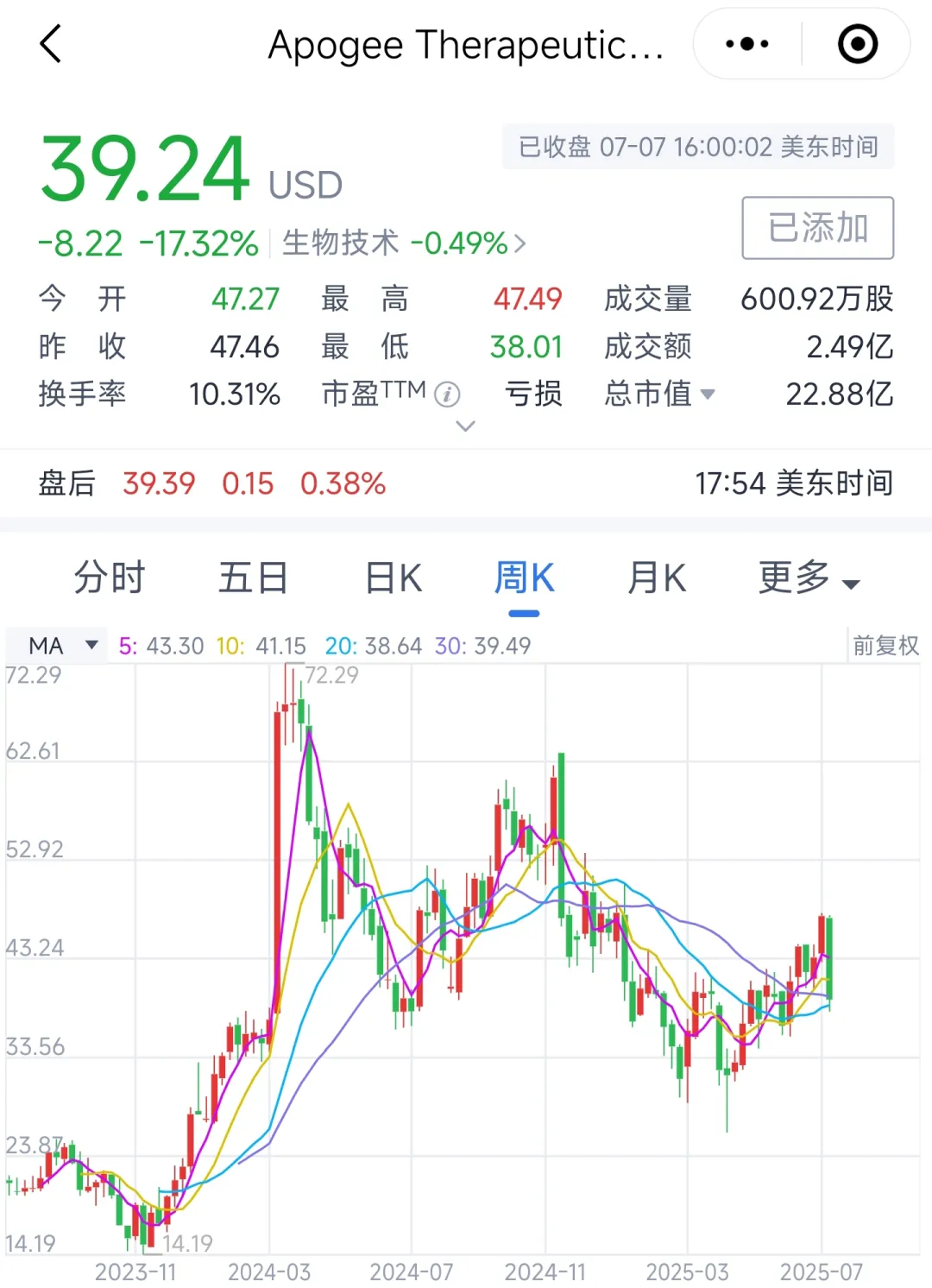
Apogee公布长效IL-13以来股价可谓一路飙升。不过昨天发布一起数据后骨架下跌17%。我们来一起看一下到底发生了什么?
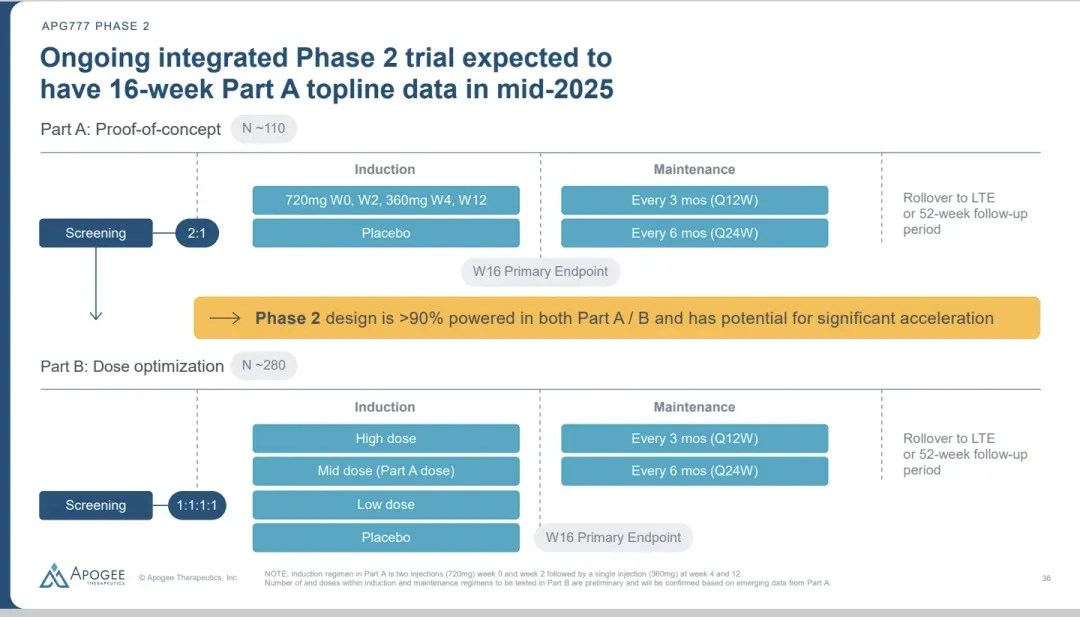
Apogee Therapeutics 公司公布的数据,APG777 在 Phase 2 APEX 试验 Part A
中成功达到了所有主要和关键次要终点。A部分(此次结果)采用了720mg(第一周和第二周给药)和360mg(第四周和第十二周),然后后续采用每3个月或每6个月一针的维持给药。B部分继续采用A部分的剂量,并额外加一个高剂量和低剂量。B部分16周数据将在明年读出。
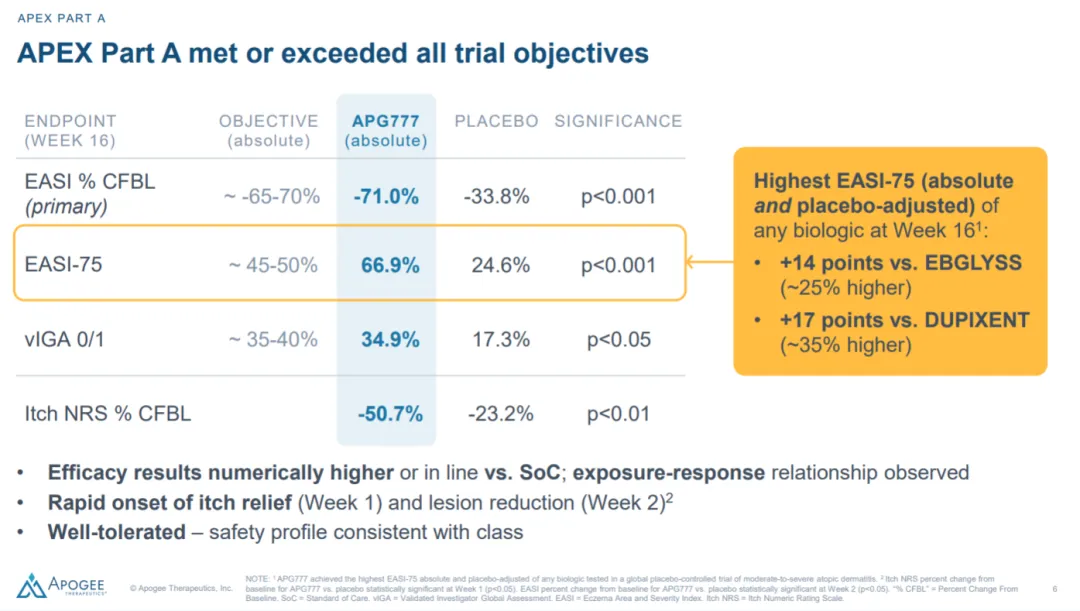
在治疗的第 16 周,患者平均的湿疹面积和严重程度指数(EASI)降低了 71%,同时有 66.9% 的患者达到了
EASI-75,即湿疹面积和严重程度指数较基线降低至少 75%。这一显著的疗效数据表明 APG777 在抗 IL-13
生物制剂中具有最佳的治疗潜力,有望为中重度特应性皮炎患者提供一种更有效的治疗选择。
APG777相比礼来/Almirall公司的IL-13抗体Lebrikizumab以及赛诺菲的Dupilumab也毫不逊色。
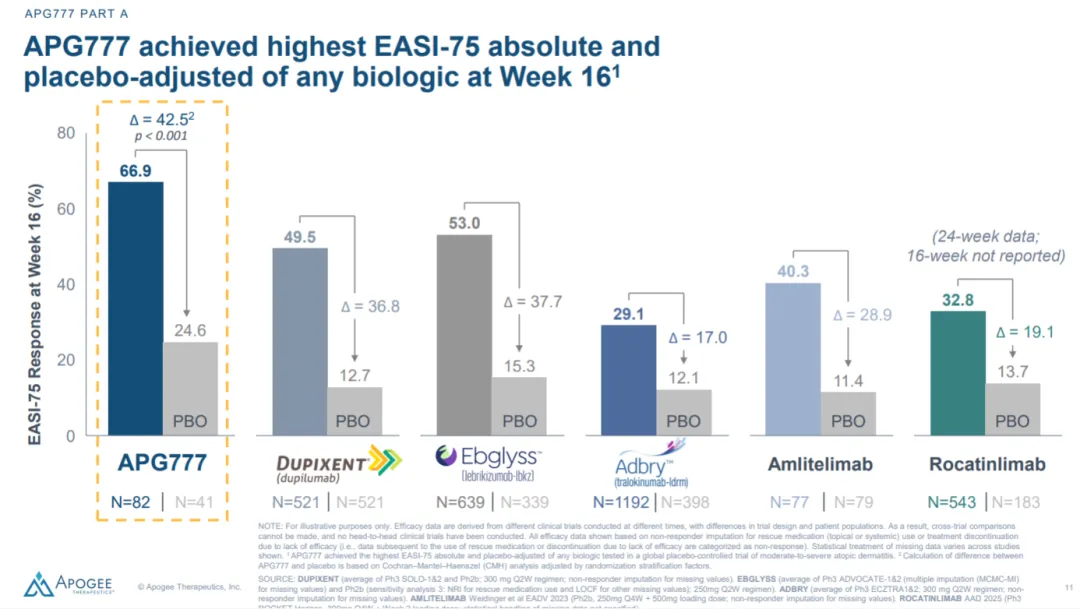
但是!这次股价大跌的终点来了!次要终点IGA0/1的数据对比,为掩盖数据的不好,没有秀出扣减placebo后对比数据。绝对值和Dupilumab以及Lebrikizumab相当,但Placebo扣减后数据并不如二者。
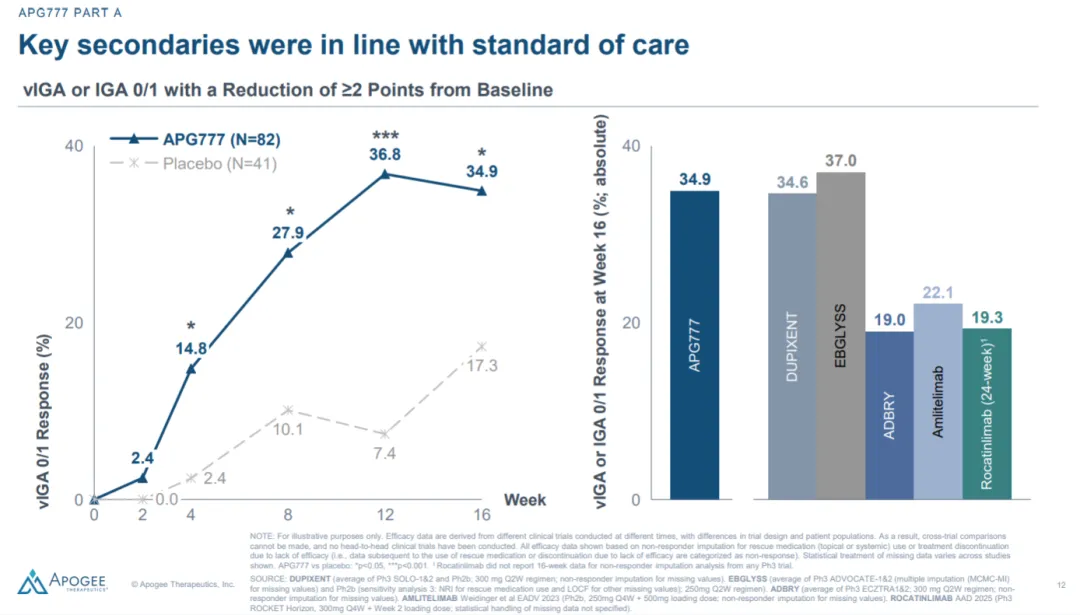
小编检索数据后做了个竞品的对比,APG777的IGA0/1的数据只有17.6%,仅仅和Leo的IL-13抗体Tralokinumab相当,远逊于Dupilumab和Lebrikizumab。
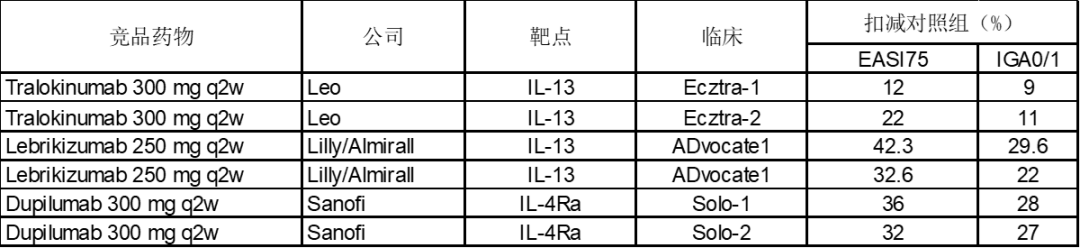
瘙痒相关数据仍然没有秀扣减placebo后对比数据,扣减placebo后NRS评分为-27.5,并没有比dupilumab和Lebrikizumab优秀。小伙伴可以自行检索数据。
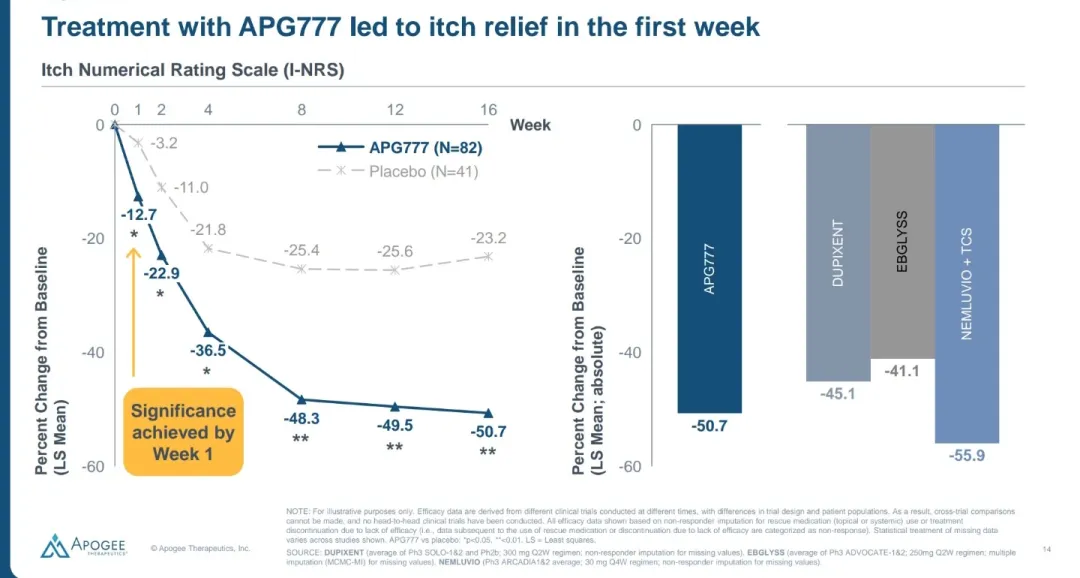
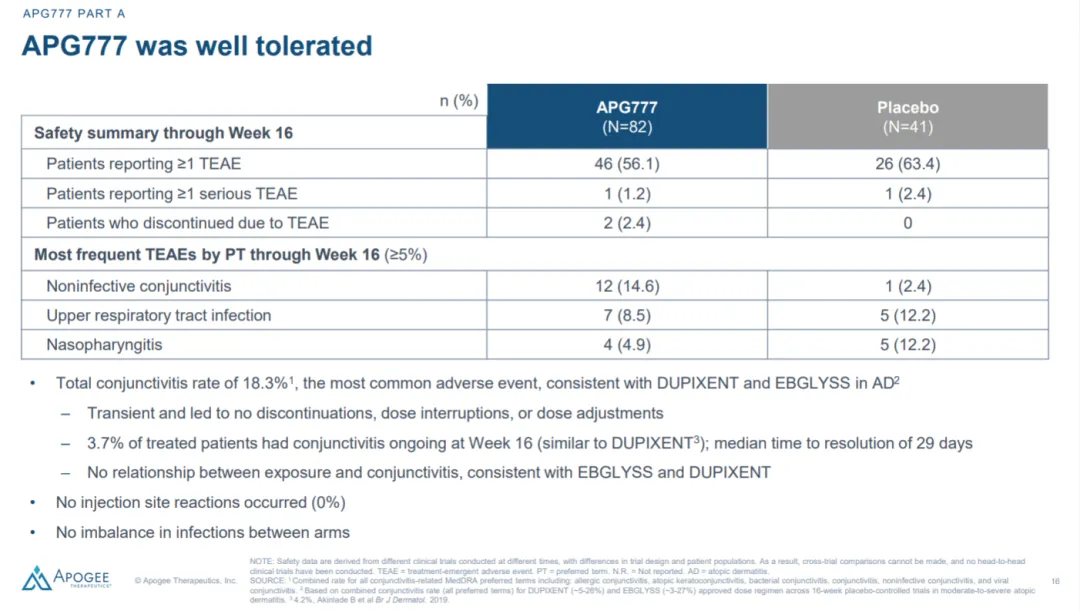
AGP777耐受性良好,但结膜炎的比例要高很多(高达14.6%),比对照组高12个百分点!后期临床需特别关注。
随着 Phase 2 APEX 试验的持续推进,Apogee Therapeutics 公司将继续收集更多关于 APG777
的数据,以进一步评估其安全性和有效性,预计明年一季度52周数据读出。
明年中二期B部分16周数据也将读出,然而小编并不看好,B部分除了A部分一个剂量,还有一个高剂量和低剂量。高剂量可能带来药效的提升,上面我们关注的结膜炎比例也很可能也会大幅增加,低剂量小编预计Apogee估计会放弃了。

结束语:
APG777 的研发有望改变特应性皮炎的治疗格局,为患者提供一种更安全、更有效且患者依从性更好的治疗方案。Apogee此次带来的数据仅仅在EASI75数据上可以“击败”赛诺菲的Dupilumab和礼来的Lebrikizumab,然而在IGA0/1和瘙痒指标上,Apogee试图掩盖药效差,没有展示对照组数据。安全性方面总体比较耐受,高达14.6%的结膜炎,比Dupilumab还要高,这个在后期B部分以及52周的临床需多家关注。虽然管理层声称药效非常的这些也为什么当天股价大跌,市场不买账的原因。
原文:

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 556
556

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 470
470

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 496
496
 热门资讯
热门资讯