 研发追踪
研发追踪
 药研网
药研网  2025-08-23
2025-08-23
 1998
1998
8月22日,中国国家药监局药品审评中心(CDE)官网显示,强生提交的尼拉帕利阿比特龙片新适应症上市申请已正式获得受理。结合强生近期在全球的注册申报动态及相关临床证据推测,此次国内申报的适应症很可能与2025年7月其在欧洲提交的扩展申请一致:联合泼尼松或泼尼松龙用于治疗激素依赖性前列腺癌患者。
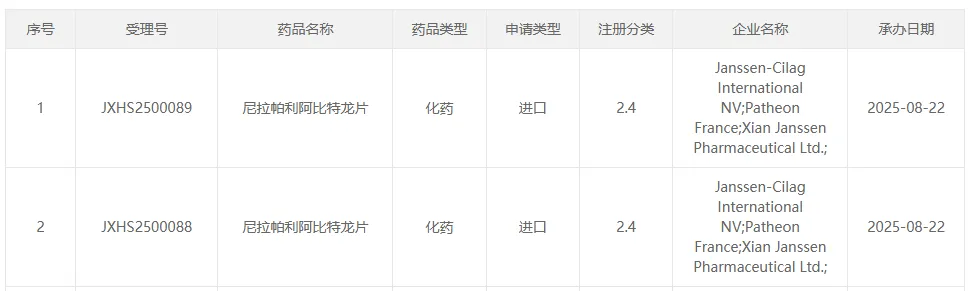
图源:CDE 官网

图源: 强生官网
该申请主要依据III期AMPLITUDE研究的临床数据支持。该研究是一项III期、随机、安慰剂对照、双盲研究,其PARP抑制剂niraparib联合醋酸阿比特龙和泼尼松(AAP)在携带同源重组修复(HRR)基因突变(包括BRCA)的转移性去势敏感性前列腺癌(mCSPC)患者中的疗效。研究对象为696例携带HRR基因突变的mCSPC患者。研究的主要终点为影像学无进展生存期。
分析显示,试验达成rPFS主要终点。在BRCA突变患者(n=191)中,niraparib联合治疗展现出显著的获益,患者的中位rPFS尚未达到,而对照组为26个月,疾病影像学进展或死亡风险降低了48%(HR=0.52;95% CI:0.37-0.72,p<0.0001)。在所有HRR突变患者中,niraparib联合治疗组患者同样未达到中位rPFS,而对照组患者的中位rPFS则为29.5个月,疾病进展或死亡风险降低37%(HR=0.63;95% CI:0.49-0.80,p=0.0001)。
安全性方面,3/4级不良事件(AE)在niraparib联合治疗组更为常见(75%对比59%),其中贫血与高血压为最常见不良反应;但因不良事件导致的停药率仍较低(14.7%对比10.3%)。截至目前,niraparib联合醋酸阿比特龙与泼尼松的安全性特征与既往研究一致。
尼拉帕利阿比特龙是强生推出的复方制剂,于2023年在欧盟和美国获批,用于联合泼尼松或泼尼松龙治疗携带BRCA1/2突变的转移性去势抵抗性前列腺癌(mCRPC)成人患者的一线治疗。2024年10月,该药在国内首次获批,成为国内首个且唯一获批的双效复方制剂。
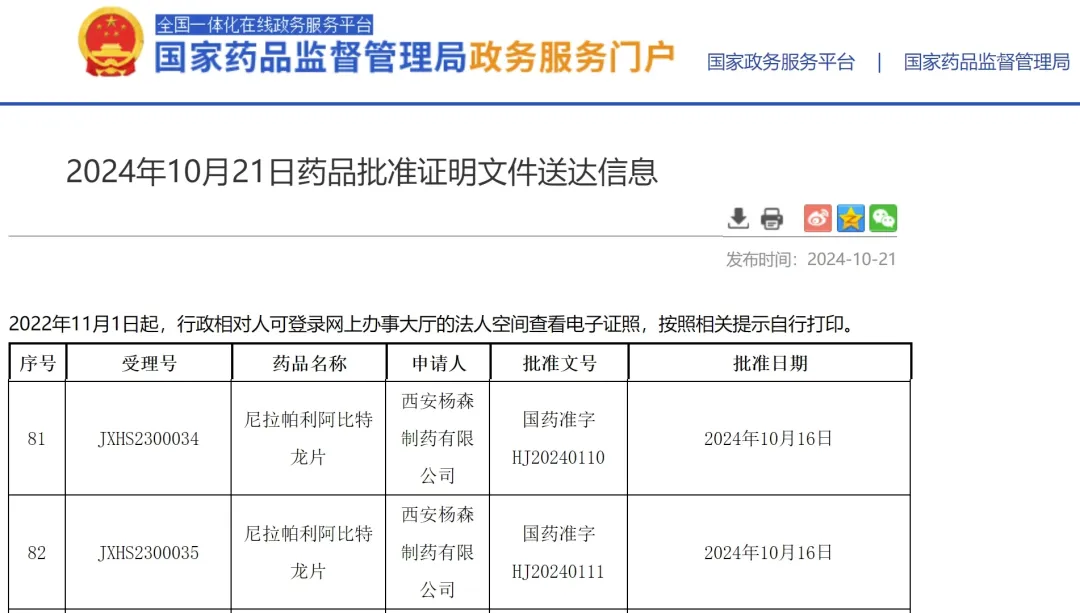
此次新适应症申请的受理,标志着尼拉帕利阿比特龙在前列腺癌治疗领域的适应症进一步扩展,为国内患者提供了更多治疗选择。

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 563
563

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 476
476

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 501
501
 热门资讯
热门资讯