 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2025-08-30
2025-08-30
 2181
2181
根据 Insight 数据库,截至 8 月 28 日,有 20 款新药在本月向 NMPA 递交了上市申请(含新适应症),包括 8 个首次上市申请和 12 个新适应症申请。
从注册分类来看,20 款药中,国产药有 12 款,进口药有 8 款。药物类型上,化药有 13 款,生物药有 7 款。本文将节选其中几款首次报产的新药信息做介绍,仅供参阅。
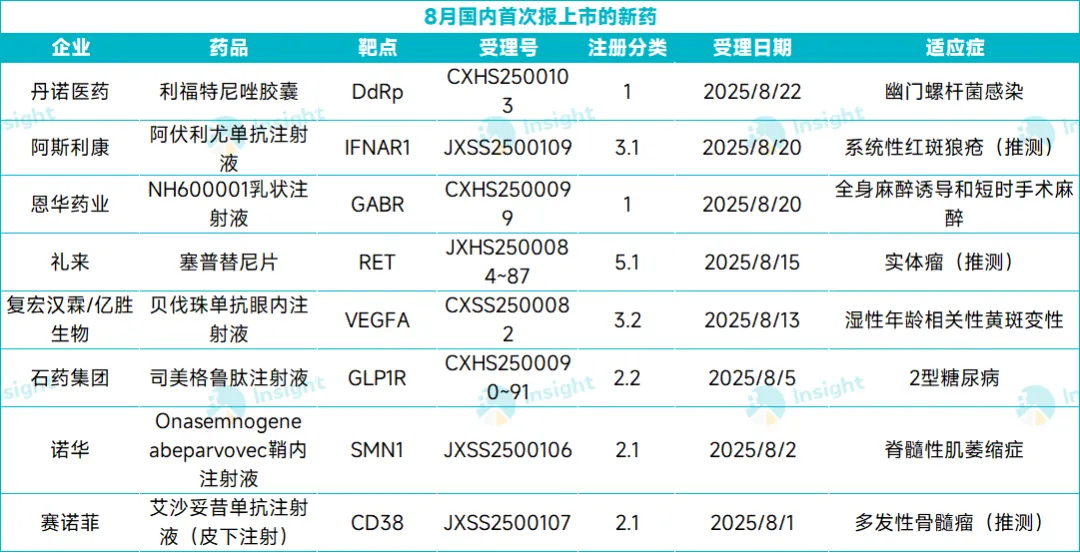
数据来源:CDE、Insight 数据库,统计范围 2025.8.1-8.28
首个 SMA 基因疗法
8 月 2 日,诺华 Onasemnogene abeparvovec 鞘内注射液(OAV101 注射液,Zolgensma)申报上市。该申请已被 CDE 纳入优先审评,用于治疗 6 月龄及以上 5q 型脊髓性肌萎缩症(SMA)患者。

截图来源:CDE 官网
Zolgensma 是诺华在 2018 年通过 87 亿美元收购 AveXis 公司获得的一种基于腺相关病毒(AAV)载体的基因治疗药物。2019 年 5 月,该药首次获 FDA 获批上市,用于治疗两岁以下 I 型 SMA 患者,2024 年销售额为 12.14 亿美元。
22 年 4 月,Zolgensma 首次在国内启动临床。这是一项随机、假操作对照、双盲、III 期临床试验,属于全球 III 期临床 STEER 研究(NCT05089656)的中国部分,针对 2 -18 岁初治 2 型 SMA 患者,拟在中国入组 20 人,国际入组 125 人。
24 年 12 月,诺华宣布 STEER 研究达到主要终点。研究结果显示,相较于对照组,接受鞘内注射 Zolgensma 治疗的 SMA 患者的 Hammersmith 运动功能量表扩展版(HFMSE)总分较基线有所增加,这表明 SMA 患者的运动功能得到改善。根据诺华新闻稿,这是首个在两岁及以上未接受治疗的 SMA 患者中具有临床获益的试验性基因疗法。
Insight 数据库显示,目前全球范围内,获批的 SMA 新药仅有 3 款,分别是 PTC Therapeutics 的利司扑兰、Ionis Pharmaceuticals 的诺西那生和诺华的 Zolgensma。其中,只有诺华的为基因治疗药物。
石药集团「司美格鲁肽」
申报糖尿病适应症
8 月 5 日,石药集团司美格鲁肽注射液国内报上市,用于成人 2 型糖尿病患者的血糖控制。石药集团的产品是按照化学合成法制备的司美格鲁肽制剂,属于化药 2.2 类新药。
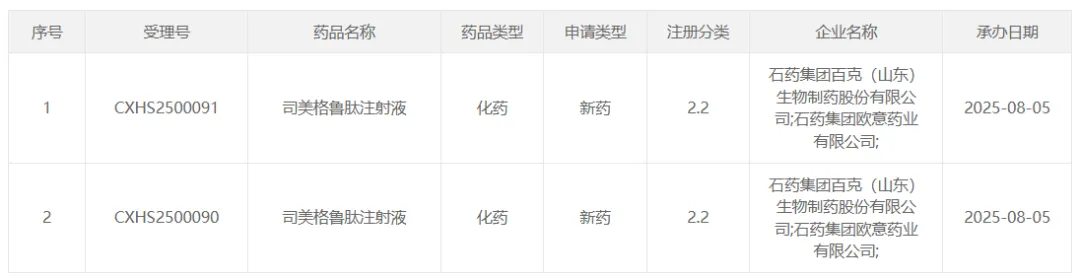
截图来源:CDE 官网
本次上市申请是基于一项关键性 Ⅲ 期临床试验结果。这项临床试验数据显示,在经二甲双胍治疗血糖控制不佳的 2 型糖尿病患者中,与诺和诺德的司美格鲁肽原研药相比,石药集团的司美格鲁肽产品展现出高度一致的疗效,且其胃肠道反应发生率略低。
Insight 数据库显示,目前国内已有 7 款国产司美格鲁肽申报上市,分别来自九源基因、丽珠集团、齐鲁制药、联邦制药、中美华东、石药集团、惠升生物,首发适应症都是 2 型糖尿病。
从注册分类来看,齐鲁制药和石药集团的司美格鲁肽是按照化药改良新药 2.2 类申报的,其它几款产品都是按照生物类似药 3.3 类申报。
复宏汉霖/亿胜生物
「贝伐珠单抗眼科制剂」
8 月 13 日,复宏汉霖和亿胜生物联合递交了贝伐珠单抗眼内注射液(HLX04-O)的上市申请,用于治疗湿性年龄相关性黄斑变性(wAMD) 。

截图来源:CDE 官网
HLX04-O 是复宏汉霖利用基因工程技术构建的一款重组抗 VEGF 人源化单克隆抗体注射液。亿胜生物已和复宏汉霖达成协议,在全球范围内共同开发 HLX04-O 用于治疗湿性年龄相关性黄斑变性等眼科疾病。
本上市申请是基于一项多中心、随机、双盲、阳性对照的非劣效 III 期研究(NCT05003245),该试验比较了玻璃体内注射(IVT)HLX04-O 与雷珠单抗治疗 wAMD 的效果和安全性。
2025 年 4 月,复宏汉霖宣布这项项 III 期临床研究达到主要研究终点。研究数据显示,HLX04-O 组第 48 周最佳矫正视力(BCVA)较基线改善的平均字母数变化非劣于雷珠单抗组。此外,HLX04-O 和雷珠单抗对 wAMD 患者人群整体、眼部、非眼部的安全性特征均相似,且安全性良好。
根据 Insight 数据库,国内尚无贝伐珠单抗获批治疗眼科疾病,也无贝伐珠单抗的眼科制剂获批。今年 6 月,兆科眼科和东曜药业联合提交了贝伐珠单抗眼科制剂 TAB014 的上市申请,用于治疗 wAMD 。复宏汉霖/亿胜生物的 HLX04-O 是第 2 款报产的此类药物。
恩华药业「NH600001」
麻醉 1 类新药
8 月 20 日,恩华药业 1 类新药 NH600001 乳状注射液申报上市,适应症为全身麻醉诱导和短时手术麻醉。 NH600001 是依托咪酯创新迭代的升级产品,目前国内尚无同类型产品上市。

截图来源:CDE 官网
临床研究显示,NH600001 镇静/麻醉疗效确切,有效剂量低于依托咪酯,起效快、苏醒迅速,在保留依托咪酯在血流动力学稳定性与对呼吸影响小等优势的基础上,还显著降低了肌阵挛发生率,并基本消除了对肾上腺皮质功能的抑制风险。
恩华药业预计 NH600001 将在 2026 年获批上市,上市后将与恩华药业的 TRV130 产品(富马酸奥赛利定注射液)形成「镇痛-镇静」产品协同闭环,进一步丰富公司在中枢神经领域的产品管线。
阿斯利康「阿伏利尤单抗」
8 月 20 日,阿斯利康阿伏利尤单抗注射液国内申报上市,推测适应症为用于治疗系统性红斑狼疮(SLE)。

截图来源:CDE 官网
阿伏利尤单抗是一款靶向 Ⅰ 型干扰素受体1(IFNAR1)的单克隆抗体药物。Ⅰ 型干扰素通路是驱动 SLE 发生发展的重要机制。阿伏利尤单抗可通过与 Ⅰ 型干扰素受体靶向结合,同时阻断多种亚型 Ⅰ 型干扰素的作用,从而实现对 SLE 的治疗效果。
阿伏利尤单抗已在美国、日本、欧盟获批上市,用于治疗中度至重度 SLE 成人患者。24 年,该药的全球销售额为 4.74 亿美元,同比增长 69.29%。
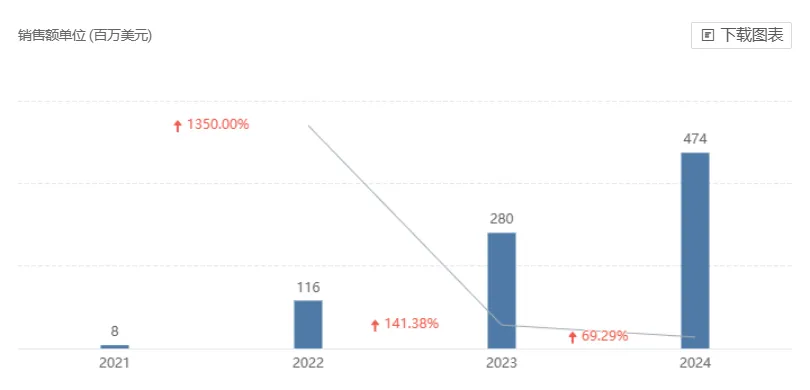
截图来源:Insight 数据库
丹诺医药「利福特尼唑」
幽门螺杆菌感染 1 类新药
8 月 22 日,丹诺医药 1 类新药利福特尼唑胶囊申报上市,用于治疗幽门螺杆菌感染。

截图来源:CDE 官网
根据丹诺医药新闻稿,利福特尼唑(TNP-2198)是全球首个专门针对幽门螺杆菌开发的新分子实体,具有多靶点协同作用机制,有望克服传统抗生素的耐药问题,为幽门螺杆菌感染患者提供一个新的治疗方案。
在中国完成的多中心、随机、双盲、铋剂四联对照的 III 期临床试验中,与目前使用的铋剂四联疗法相比,以利福特尼唑为基础的三联方案已展现出了多方面的优势。
丹诺医药专注于解决细菌感染及细菌代谢相关疾病领域的未被满足临床需求。除了利福特尼唑,该公司还有两款核心产品,包括:利福喹酮 (TNP-2092) 注射剂,一款潜在首创三靶点治疗植入体相关细菌感染的候选药物;TNP-2092 口服制剂,全球首个用于治疗肠道菌群代谢相关疾病的多靶点候选药物。

 研发追踪
研发追踪
 药说新药
药说新药  2026-06-08
2026-06-08
 563
563

 研发追踪
研发追踪
 药番茄Pharmato
药番茄Pharmato  2026-06-08
2026-06-08
 476
476

 研发追踪
研发追踪
 十亿分子
十亿分子  2026-06-08
2026-06-08
 501
501
 热门资讯
热门资讯