 会员动态
会员动态
 正大天晴药业集团
正大天晴药业集团  2024-11-11
2024-11-11
 4726
4726
晚期非小细胞肺癌患者迎来又一重磅靶向药物。11月8日,国家药监局官网显示,正大天晴联合开发的KRAS G12C抑制剂格索雷塞片(商品名:安方宁)获批准上市,适用于治疗至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因(KRAS)G12C 突变型的晚期非小细胞肺癌(NSCLC)成人患者。这是正大天晴今年获批的第四款1类创新药,也是公司在肺癌领域取得的又一突破。

攻克“不可成药”靶点,格索雷塞重塑KRAS G12C突变治疗格局
肺癌是全球第一大癌种。国家癌症中心发布的数据显示,2022年中国肺癌新发病例达106万人,是我国发病率和死亡率最高的恶性肿瘤。其中,非小细胞肺癌(NSCLC)约占所有肺癌的85%[1]。
KRAS突变是非小细胞肺癌中除EGFR之外最常见的驱动基因突变,G12C又是KRAS突变中发生率最高的亚型[2,3]。该人群在现有非靶向治疗方案中的获益有限,存在明确未被满足的临床需求。
受KRAS基因结合点不明显、蛋白结构近似球形等因素影响,KRAS一度被认为是最难攻克的“不可成药”靶点,是肺癌治疗中的“老大难”。
格索雷塞片是国内首个自主研发并进入临床试验阶段的KRAS G12C抑制剂,也是首个被CDE(国家药监局药品审评中心)纳入突破性治疗品种的国产KRAS G12C抑制剂,并且在今年1月被CDE纳入优先审评审批程序。此次格索雷塞获批上市,将进一步提升国内肿瘤精准靶向治疗水平,重塑KRAS G12C突变治疗格局。
2023年8月,正大天晴与益方生物签订许可与合作协议,获得KRAS G12C靶向药物D-1553产品在中国大陆地区开发、注册、生产和商业化的独家许可权。
研发数据亮眼:中位ORR 52%、中位OS 14.1个月
格索雷塞采用一种创新的分子结构设计——采用双甲基取代哌嗪,能量更低且构象更稳定。其和血浆蛋白结合率低,提高血浆和脑组织中游离药物浓度和总暴露量,在多种KRAS G12C突变的体外及动物模型中展现出抗肿瘤活性。
格索雷塞能选择性地与KRAS G12C的SWITCH II蛋白中的二磷酸鸟苷结合,从而抑制KRAS的致癌信号传导,抑制肿瘤细胞增殖,从而实现抗肿瘤作用,是一款具有创新结构特点的KRAS G12C抑制剂。
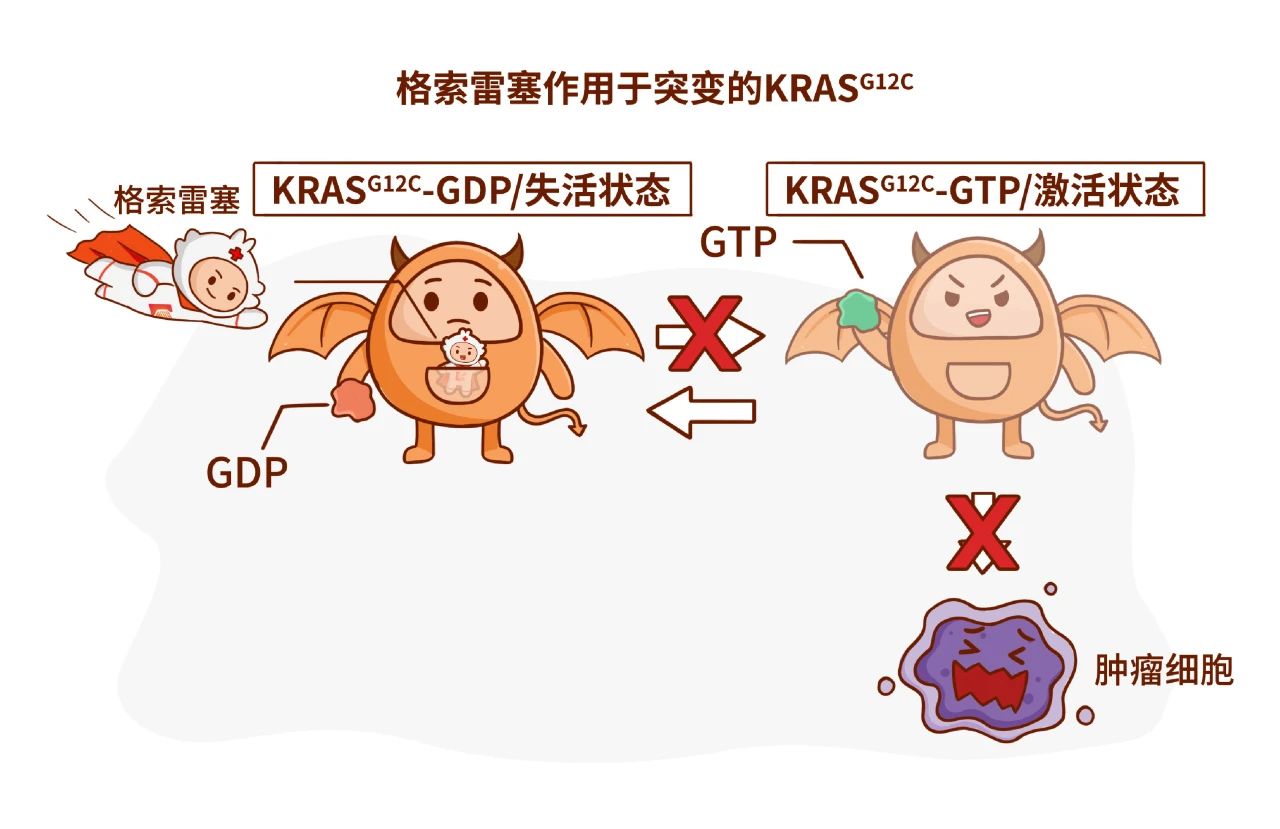
今年9月,格索雷塞在2024世界肺癌大会(WCLC)上公布了治疗KRAS G12C突变的非小细胞肺癌Ⅱ期临床研究数据:客观缓解率(ORR)为52%,疾病控制率(DCR)为88.6%,中位缓解持续时间(DOR)为12.5个月,中位无进展生存期(PFS)为9.1个月,中位总生存期(OS)为14.1个月[4]。上述数据显示,格索雷塞在携带KRAS G12C突变的NSCLC患者中持续表现出较高的肿瘤缓解率和较长的缓解持续时间。
深挖临床应用潜力,新适应症加速推进中
除了这次获批的适应症,格索雷塞单药和联合用药在非小细胞肺癌一线治疗以及结直肠癌等其他实体肿瘤中的国际多中心临床研究也正在进行中。
2024年6月,格索雷塞另外两个适应症被CDE纳入突破性治疗药物程序,分别为:(1)用于治疗经一线治疗失败的伴KRAS G12C突变局部晚期或转移性胰腺导管腺癌;(2)联合西妥昔单抗注射液用于经二线标准治疗(包括奥沙利铂、伊立替康、5-氟尿嘧啶和抗VEGF单抗)失败的、KRAS G12C突变阳性的、手术无法切除的局部晚期或转移性结直肠癌。
今年以来,正大天晴迎来创新产品收获期,上半年已有安奈克替尼、依奉阿克、贝莫苏拜单抗三款抗肿瘤1类新药获批上市,同期国内企业第一。肺癌领域是正大天晴的发力重点之一,随着格索雷塞获批,公司在肺癌领域创新药数量已达6个。
参考文献:
[1] 揭光灵,杨莹,虞永峰,等. 非小细胞肺癌治疗年度进展2023[J]. 中华医学杂志,2024,104(36):3446-3454.
[2] 农靖颖, 李小雪, 姚舒洋, 等. KRAS突变非小细胞肺癌的生物学和治疗研究进展 [J] . 肿瘤研究与临床, 2021, 33(1): 69-73.
[3] Tang D,et al. Oncogenic KRAS blockade therapy:renewed enthusiasm and persistent challenges[J]. Mol Cancer,2021,20(1): 128.
[4] Li Z, et al. Garsorasib in KRAS G12C-Mutated Non-Small-Cell Lung Cancer: Updated Results from a Phase 2 Study. 2024 WCLC Abstract OA14.03.

 会员动态
会员动态
 药研网
药研网  2026-05-12
2026-05-12
 1195
1195

 会员动态
会员动态
 InxMed应世生物
InxMed应世生物  2026-05-08
2026-05-08
 1271
1271

 会员动态
会员动态
 维健医药
维健医药  2026-04-27
2026-04-27
 1618
1618
 热门资讯
热门资讯