 产业资讯
产业资讯
 医药观澜
医药观澜  2025-04-11
2025-04-11
 2915
2915
4月9日,中国国家药监局药品审评中心(CDE)官网最新公示,有5款新药拟纳入突破性治疗品种,分别来自鞍石生物、康方生物、翰森制药、三生制药,针对的适应症为不同类型的非小细胞肺癌(NSCLC)。
鞍石生物:PLB1004胶囊
作用机制:EGFR-TKI
适应症:治疗既往接受EGFR-TKI治疗失败后,具有EGFR突变、MET扩增和/或过表达的局部晚期或转移性NSCLC患者

截图来源:CDE官网
根据鞍石生物公开资料,安达替尼(PLB1004)是其在研的新型小分子酪氨酸激酶不可逆抑制剂(EGFR-TKI),具有高选择性,可以透过血脑屏障。非临床药效实验表明,该化合物对EGFR 20号外显子插入突变、HER2 20号外显子插入突变、EGFR敏感突变、EGFR耐药突变和EGFR罕见突变均有效。
在2024年世界肺癌大会(WCLC)上,研究人员公布了一项1/2期临床研究结果,该研究评估了PLB1004+c-MET抑制剂vebreltinib,在EGFR突变阳性、MET扩增或过表达的EGFR-TKI后NSCLC患者中的疗效和安全性。这也正是该产品本次拟纳入突破性治疗品种的适应症。
44例患者在1b期接受了vebreltinib 100mg+PLB1004 160mg、vebreltinib 150mg+PLB1004 160mg、vebreltinib 200mg+PLB1004 80mg或vebreltinib 150mg+PLB1004 80mg,并纳入了安全性分析。44例患者中,36.4%的患者发生脑转移,86.4%的患者接受了第三代EGFR-TKI治疗。
研究结果显示,所有vebreltinib和PLB1004剂量水平的测试中都发生了客观缓解,在19/32(59.4%)可评估反应的患者中观察到部分缓解(PR)。四个剂量组可评价疗效的患者中,分别有7/12(58.3%)、6/13(46.2%)、2/3(66.7%)、4/4(100%)达到PR。此外,在脑转移患者中,ORR为75.0%(9/12)。先前接受过第三代EGFR-TKI的患者的ORR为58.6% (17/29)。
研究人员认为,vebreltinib+PLB1004在MET扩增或过表达的EGFRm NSCLC患者中显示出有希望的抗肿瘤活性和可管理的安全性,这些患者在先前的EGFR-TKI治疗后经历了疾病进展,特别是那些患有脑转移并接受第三代EGFR-TKI治疗的患者。
康方生物:AK109联合AK104
作用机制:VEGFR-2单抗联合PD-1/CTLA-4双抗
适应症:治疗经含PD-(L)1抑制剂治疗后进展的晚期鳞状NSCLC

截图来源:CDE官网
普络西(AK109)是一款全人源VEGFR-2(抗血管内皮生长因子受体-2)单克隆抗体;卡度尼利(AK104)为一款PD-1/CTLA-4双特异性抗体,已经在中国获批治疗宫颈癌、胃癌等适应症。
根据康方生物公开资料介绍,卡度尼利联合普络西具有显著的抗肿瘤活性和可控的安全性特征,有可能通过协同增效来克服免疫检查点抑制剂耐药。卡度尼利联合普络西用于治疗晚期胃腺癌或胃食管结合部腺癌的注册性3期临床研究已经启动,并于2024年7月完成了首例患者入组。
翰森制药:注射用HS-20093
作用机制:B7-H3靶向ADC
适应症:既往经过含铂化疗后进展或复发的驱动基因阴性的局部晚期或转移性非鳞状NSCLC

截图来源:CDE官网
HS-20093是一种B7-H3靶向抗体偶联药物(ADC),由全人源抗B7-H3单抗与拓扑异构酶抑制剂(TOPOi)有效载荷共价连接而成,正于中国开展用于治疗肺癌、肉瘤、头颈癌以及其他实体瘤的多项临床研究,其中针对小细胞肺癌适应症已经进入3期临床阶段。2023年12月,翰森制药与葛兰素史克(GSK)订立独家许可协议,授予后者全球独占许可(不含大中华区),以开发、生产及商业化该产品。
此前,HS-20093已经获美国FDA授予突破性疗法认定,用于治疗广泛期小细胞肺癌、骨肉瘤;被中国NMPA纳入突破性治疗品种,用于治疗广泛期小细胞肺癌、骨肉瘤;被欧洲EMA授予优先药物认定,用于治疗广泛期小细胞肺癌。
三生制药:SSGJ-707注射液
作用机制:VEGF/PD-1双抗
适应症:一线治疗PD-L1表达阳性的局部晚期或转移性NSCLC
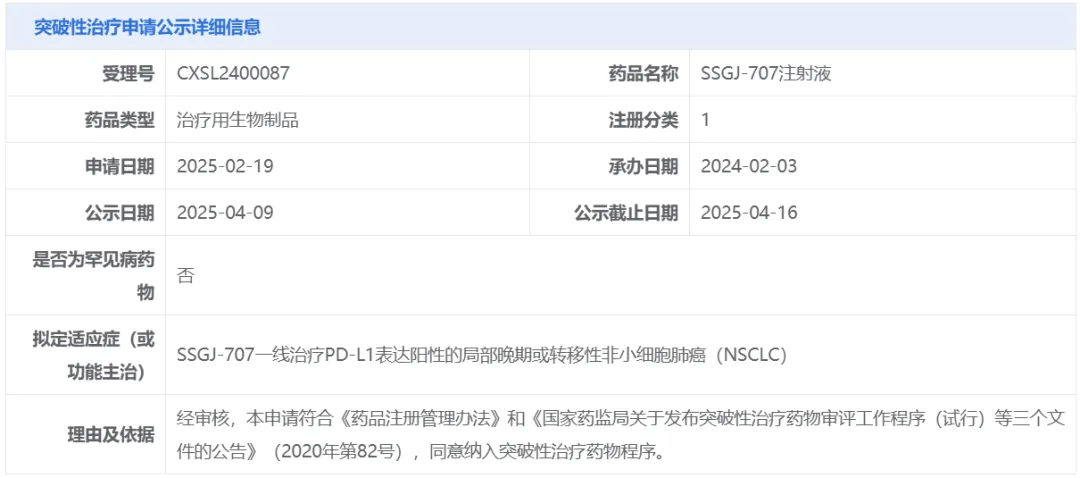
截图来源:CDE官网
SSGJ-707是一款VEGF/PD-1双抗,研究人员正在推进该产品在包括单药一线治疗PD-L1阳性的NSCLC、联合化疗一线治疗NSCLC、转移性结直肠癌(mCRC)、以及包括子宫内膜癌、卵巢癌等在内的晚期妇科肿瘤等2期临床研究。
根据三生制药此前新闻稿,在2025年JPM大会上披露的2期临床阶段性分析数据显示,SSGJ-707在非小细胞肺癌和转移性结直肠癌患者的治疗上展现出优异的客观缓解率(ORR)和疾病控制率(DCR),尤其在NSCLC适应症上,无论单药还是与化疗联用,该产品均展示了显著的抗肿瘤活性和良好的安全性。其中,针对一线治疗PD-L1表达阳性的局部晚期或转移性NSCLC适应症的2期中期数据显示,SSGJ-707具有良好的耐受性和良好的安全性,ORR为70.8%,DCR为100%。

 产业资讯
产业资讯
 识林
识林  2026-05-23
2026-05-23
 505
505

 产业资讯
产业资讯
 米内网
米内网  2026-05-23
2026-05-23
 415
415

 产业资讯
产业资讯
 药通社
药通社  2026-05-23
2026-05-23
 428
428
 热门资讯
热门资讯