 产业资讯
产业资讯
 Insight数据库
Insight数据库  2025-06-18
2025-06-18
 2475
2475
6 月 17 日,CDE 官网显示,默沙东的 Clesrovimab (MK-1654) 注射液上市申请拟纳入优先审评,适应症为用于即将进入或出生在第一个呼吸道合胞病毒(RSV)流行季的新生儿和婴儿预防 RSV 所致的下呼吸道感染。
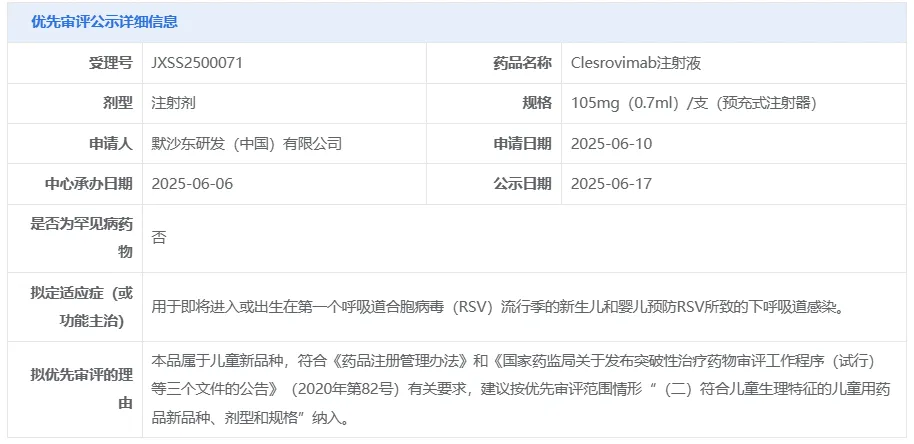
截图来源:CDE 官网
RSV 是一种传染性病毒,可引起广泛的季节性感染。Clesrovimab 是一款预防性长效单克隆抗体,可通过与 RSV 的融合糖蛋白结合来诱导对 RSV 的被动免疫,从而预防 RSV 感染,旨在为婴儿提供直接、快速和持久的保护。
6 月 9 日,Clesrovimab 刚获得美国 FDA 批准上市,是首个也是唯一一个针对婴儿的单剂量 RSV 单抗,无论患者体重如何。
FDA 的批准是基于关键 IIb/III 期 CLEVER 研究(MK-1654-004 )和 III 期 SMART 研究(MK-1654-007)结果。
CLEVER 研究是一项随机、双盲、安慰剂对照的 IIb/III 期临床试验,评估了对早产儿和足月儿(出生至 1 岁)注射单剂量 Clesrovimab 的疗效。该试验达到了主要终点和关键次要终点。
与安慰剂相比,给药后第 150 天(5 个月),Clesrovimab 组将需要就医的 RSV 相关下呼吸道感染(MALRI)发生率降低了 60.5%(95% CI:44.2, 72.0,p<0.001),将 RSV 相关住院率降低了 84.3%(95% CI:66.7, 92.6,p<0.001) 。
对于进入 RSV 首个流行季的婴儿,Clesrovimab 的安全性与安慰剂大致相当。最常见的不良反应包括给药后 5 天内发生的注射部位红斑、给药后 5 天内发生的注射部位肿胀,以及给药后 14 天内发生的皮疹。
SMART 研究是一项随机、部分盲法、多中心的 III 期临床试验,旨在评估 Clesrovimab 头对头帕利珠单抗在重症 RSV 感染高风险婴儿中的安全性和有效性。
SMART 试验结果显示,Clesrovimab 和帕利珠单抗的 RSV 相关 MALRI 发生率和 RSV 相关住院率相当;安全性也与帕利珠单抗大致相当,并与 CLEVER 试验中 Clesrovimab 在婴儿中的安全性一致。
Insight 数据库显示,全球现共有三款 RSV 单抗获批上市,分别为阿斯利康/赛诺菲的尼塞维单抗、阿斯利康/苏庇医药的帕利珠单抗、默沙东的 Clesrovimab。
在国内,目前仅有阿斯利康/赛诺菲的尼塞维单抗获批。默沙东的 Clesrovimab 已报上市。此外,还有两款 RSV 单抗已进入 Ⅲ 期临床,分别来自泰诺麦博(TNM001)、瑞阳生物(RB0026)。

截图来源:Insight 数据库

 产业资讯
产业资讯
 珍立拍
珍立拍  2026-05-19
2026-05-19
 429
429

 产业资讯
产业资讯
 深究科学
深究科学  2026-05-19
2026-05-19
 429
429

 产业资讯
产业资讯
 中国医药报
中国医药报  2026-05-19
2026-05-19
 556
556
 热门资讯
热门资讯