 产业资讯
产业资讯
 药智局
药智局  2026-03-10
2026-03-10
 1303
1303
近日,知名行业媒体BioPharmaTrend发布2026年AI原生(AI-Native)生物科技企业名单。
所谓AI原生,即从创立之初就以AI为底层核心,这类Biotech不是在传统研发流程上叠加AI工具,而是用AI重构整个药物研发全流程。
名单介绍了几家新成立的公司,它们将AI深度应用于RNA 设计、生物分子建模、调控DNA 工程、实验室自动化等多个领域。
这些项目集中反映出AI制药的前沿风向,有望揭示行业未来最具价值的增长赛道。
智药局结合公开信息,对上述公司进行了整理,以供业内参考。
Blank Bio
面向疗法开发与临床试验的RNA基础大模型
Blank Bio是一家由YC(Y Combinator)投资的科技生物公司,2025年在加州旧金山成立,由Philip Fradkin、Jonny Hsu与Ian Shi 联合创立。
公司致力于打造新一代RNA基础大模型,为RNA疗法、生物标志物与诊断技术提供覆盖全研发流程的支持。
模型可对不同RNA分子变体、突变及其在细胞中的表达水平进行分析,预测其稳定性与蛋白表达量,在计算机中高效模拟多项湿实验。
基于这些预测,系统能够优化mRNA 序列以提升效果,分析血液样本中的游离 RNA,在特定RNA变体层面识别生物标志物,并发现全新的RNA药物靶点,同时支持RNA靶向疗法的设计。
公司表示,这类模型还可实现更精准的患者分层,助力设计更高效的临床试验。
目前Blank Bio的开源模型已被制药巨头如赛诺菲和葛兰素史克 (GSK) 使用,公司还与Arc Institute合作,将其RNA嵌入技术整合到下一代虚拟细胞模型中。
Boltz PBC
面向药物研发的开源生物分子基础大模型
Boltz PBC专注于研发用于药物发现的生物分子基础大模型。公司于 2026 年初正式公开亮相,完成由A16z领投的2800 万美元种子轮融资。
Boltz源自麻省理工学院计算机科学与人工智能实验室(MIT CSAIL),核心技术围绕 Boltz 系列模型展开,由Gabriele Corso、Jeremy Wohlwend、Saro Passaro (下图从左至右)共同创立。

该平台依托一系列能深度理解蛋白质及其他生物分子3D 结构的大型 AI 模型,将其转化为科研人员可直接用于分子设计与预测的实用工具。
2024年底发布的Boltz-1,是首个性能达到 AlphaFold3 水平且完全开源的模型,能够精确预测蛋白质、配体、核酸等生物分子复合物的 3D 结构。
后续发布的Boltz-2进一步超越了结构预测,引入了亲和力预测。它能够以比传统物理模拟快 1000 倍的速度预测药物分子与靶点结合的紧密程度,极大地加速了早期药物筛选。
公司还发布了BoltzGen,一个生成式AI 模型,专门用于从零开始设计能够结合特定生物靶点的蛋白质。
这些模型被整合进Boltz Lab平台,并提供了用于小分子和蛋白质设计的AI智能体,可自动完成结合分子生成、亲和力预测排序、合成可行性筛选等全流程工作。
Boltz已与辉瑞达成合作,基于辉瑞内部数据对基础大模型进行专项训练,打造专供辉瑞使用的定制版本,用于结构预测、小分子亲和力评估与生物药设计;而通用版模型则继续向全球科研社区开放使用。
Origin
用于更安全细胞与基因治疗的调控DNA设计
Origin是一家总部位于旧金山的初创公司,2025 年由 CEO Yash Rathod 与 CTO Malhar Bhide 联合创立,并入选 Y Combinator 2026 年冬季创业营。
公司致力于通过设计调控DNA“开关”(启动子与增强子),让细胞与基因治疗更加安全,精准控制治疗基因在体内的表达位置与强度。
传统的细胞和基因疗法(如CAR-T)虽然强大,但往往由于无法精确控制基因在何时、何地表达,容易产生毒性。Origin 的目标是通过编程让药物只在病变细胞中生效。
2025年10月,Origin 正式发布AI模型Axis,该模型既能预测现有调控序列的行为,也能从头设计全新序列。
根据公司披露的数据,其Axis 模型在预测调控元件活性方面,平均优于 Google DeepMind 的 AlphaGenome 模型约6.7%。
公司正在构建全球最大的合成调控序列专有数据库,涵盖多种细胞状态。主要应用于癌症、中枢神经系统(CNS)疾病等领域的基因疗法优化。
Manas AI
端到端药物研发,专注肿瘤与罕见病
Manas AI是一家成立于2025年的全栈式AI原生生物制药公司,联合创始人包括肿瘤学家、普利策奖获得者Siddhartha Mukherjee与领英联合创始人Reid Hoffman、前谷歌工程高管Ujjwal Singh。

图:Reid Hoffman(左)和Siddhartha Mukherjee(右)
公司公开亮相时完成2460万美元种子轮融资,由General Catalyst与Reid Hoffman联合领投,之后又宣布追加2600万美元种子轮融资。
Manas AI专注开发肿瘤与罕见病药物,早期公开信息显示,其首批项目聚焦乳腺癌、前列腺癌与淋巴瘤。
Manas称其核心模型为神经符号科学基础大模型,将物理定律与深度学习相结合,目标是大幅缩短研发周期、降低肿瘤与罕见病新药的开发成本。
公司平台覆盖药物研发全流程:从早期靶点发现、分子设计、实验室验证到临床试验,将AI 系统与生物学家、化学家、临床医生的专业判断结合,可用于抗体、小分子、RNA 药物及联合疗法等多种类型。
2026年初,Manas AI 与Schrödinger达成了深度战略合作。通过整合Schrödinger的物理模拟平台,Manas能够以传统方法 100 倍的速度进行大规模分子对接。
Strand AI
用于补齐缺失组学与临床数据的基础大模型
Strand AI成立于2025年,由Yue Dai (CEO) 和 Oded Falik (CTO) 创立,总部位于旧金山,专注于生命科学数据基础设施建设。
公司致力于打造面向生命科学的多模态患者数据集,重点应用于药物发现与临床开发场景。
Strand AI构建生物学基础模型,并从已测得的生物读数中预测“缺失”的生物数据,重构临床试验数据中缺失或未检测的组学信息,让原本数据不完整的患者样本仍可被使用。
对于样本量少、数据缺失严重的罕见病研究,该平台可合成缺失指标,让原本无法训练的模型成为可能。
Strand还开放了一款交互式工具,可展示AI基于DNA变异预测的跨组织、跨人群 RNA 表达情况,并支持数据浏览与下载。
Medra AI
面向药物研发的全自动AI 机器人实验室自动化平台
Medra是一家总部位于旧金山的初创公司,致力于为生命科学实验室打造所谓“物理AI科学家”,由斯坦福大学机器人专家、前纽约大学教授 Michelle Lee 于2021年创立。
Medra于2025年9月正式走出隐身模式,并在同年12月完成 5200 万美元A轮融资,由 Human Capital 领投,Lux Capital、Menlo Ventures、Fusion Fund 等参投,累计融资额达到约 6300 万美元。

Medra的核心目标,是打通计算机药物发现模型与湿实验验证之间的闭环,让 AI 系统能够在7×24
小时无人值守的全自动实验室中,自主开展实验并持续迭代优化。
Medra开发了一个通用的 AI 视觉控制层,可以让廉价、灵活的协作机器人手臂像人类实验员一样“看”并“操作”实验器材,并在几小时内完成部署。
Medra平台由两大核心模块组成:
物理 AI(Physical AI):通用型实验室机器人集群,可对接标准仪器、读取屏幕、操作按键、处理实验耗材,能自动化普通实验室中约 70% 的设备操作。
科学AI(Scientific AI):基于大语言模型与视觉模型构建的推理层,负责提出科学假设、设计实验方案、解读实验结果。
Resonate Bio
基于AI驱动的核磁共振平台,用于结构导向药物设计
Resonate Bio是一家位于维也纳的生物技术公司,2025 年由 Darryl B. McConnell、Gerald Platzer 与 Robert Konrat 从维也纳大学孵化成立。
传统的结构生物学技术(如X 射线晶体学)只能给蛋白质拍摄“照片”,即静态结构。然而,人体内约有一半的致病蛋白是高度柔性且处于动态变化的,这使得它们很难通过静态模型来设计药物。
Resonate Bio的开发了 AI-NMR 混合技术。通过结合核磁共振(NMR)实验数据和先进的 AI 算法,他们能够生成蛋白质与药物结合时的动态“电影”。
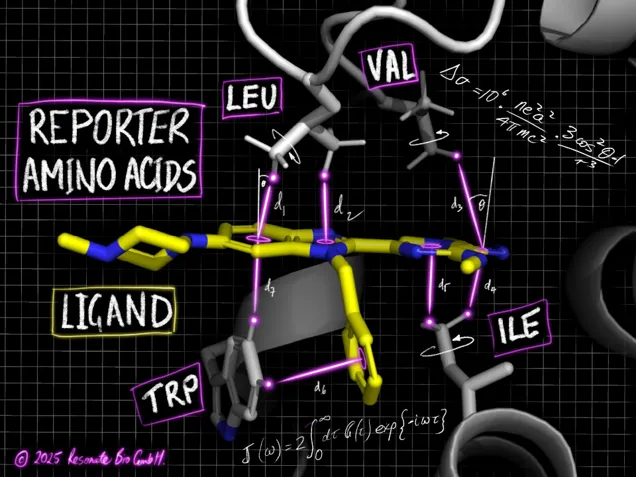
与传统单一静态结构不同,该系统可输出蛋白质配体构象集合及其相对丰度,被认为是结构导向药物设计(SBDD)的一次重大升级。
这类构象集合专为动态靶点的结构导向药物设计服务,可攻克传统晶体学、冷冻电镜难以触及的“不可成药” 靶点。
在实际应用中,AI模型从 NMR 数据中学习,以高通量方式推断大量化合物的潜在三维结合模式,为药物化学家在设计与优化小分子药物时提供更丰富的结构信息。

 产业资讯
产业资讯
 赛柏蓝器械
赛柏蓝器械  2026-04-27
2026-04-27
 80
80
 产业资讯
产业资讯
 药融圈
药融圈  2026-04-27
2026-04-27
 74
74

 产业资讯
产业资讯
 药融圈
药融圈  2026-04-27
2026-04-27
 74
74
 热门资讯
热门资讯