 产业资讯
产业资讯
 药时空
药时空  2026-04-22
2026-04-22
 98
98
4月20日,国家药监局药品审评中心(CDE)正式发布《关于公开征求 ICH〈M8:电子通用技术文档(eCTD)v4.0〉指导原则及问答文件中文翻译稿意见的通知》,公开征求意见为期 1 个月。这标志着我国药品电子注册申报体系即将迎来自 2017 年推行 eCTD 以来最重大的一次升级,全球统一的 eCTD v4.0 标准距离在国内正式落地只差最后一步。

作为一名从事药品注册工作多年的老兵,我全程见证了中国药品注册从纸质时代到电子时代的跨越。eCTD v4.0 绝不仅仅是格式的简单升级,而是一场从 “文件管理”到“元数据管理”的底层革命,将彻底重构全球药品注册的工作模式。下面,我将从注册从业者的视角,为大家深度解读这份决定未来 10 年药品注册格局的关键文件。
《M8:电子通用技术文档(eCTD)v4.0》
问答文件中文版
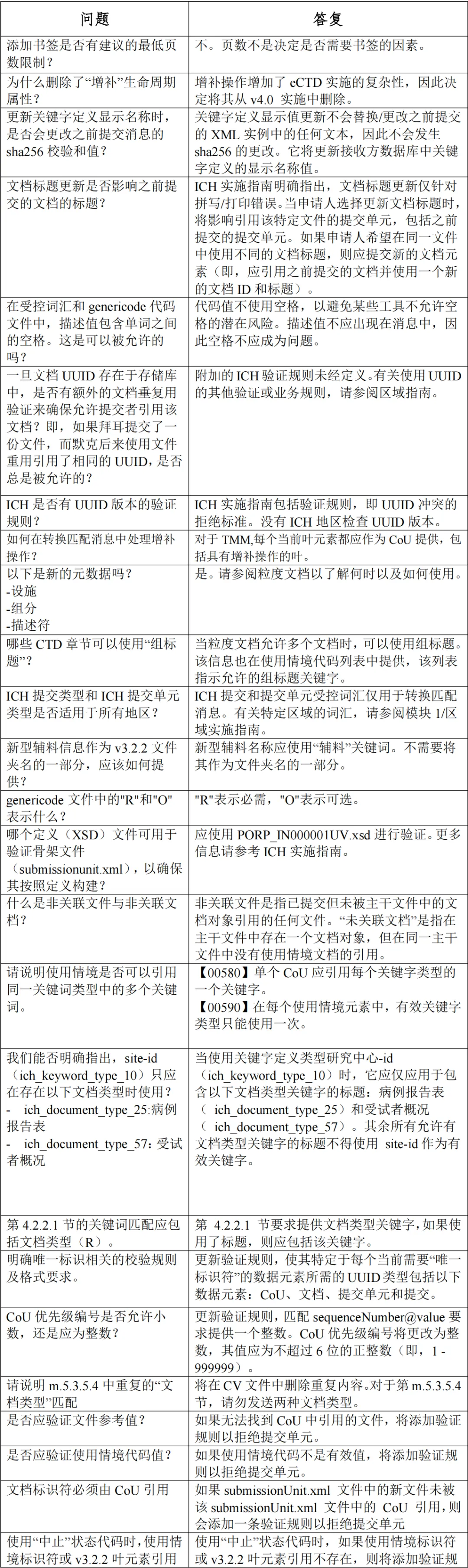

一、为什么 eCTD v4.0 是行业的必然趋势?
自 2003 年 ICH 发布 eCTD v3.0 以来,电子通用技术文档已成为全球药品注册的主流标准。我国自 2017 年开始逐步推行 eCTD v3.2.2,目前已实现化学药、生物制品、中药等全品类的电子申报。然而,随着全球药品研发和注册的日益全球化,v3.2.2 版本的局限性日益凸显:
文档复用效率极低:同一文档在不同适应症、不同国家申报时需要反复提交,不仅增加了企业的工作量,也浪费了监管机构的审查资源
生命周期管理混乱:基于叶节点的管理模式复杂易错,"增补" 操作定义模糊,容易导致版本冲突
研究文件组织困难:依赖 STF(研究标签文件)组织临床和非临床研究文件,格式不统一,可读性差
跨区域互操作性差:不同地区的 eCTD 实施存在差异,增加了全球同步申报的难度
为了解决这些问题,ICH 于 2015 年启动了 eCTD v4.0 的制定工作,并于 2024 年 5 月发布了最新的实施指南 v1.6和问答文件 v1.9。截至目前,美国 FDA、欧盟 EMA、日本 PMDA 等主要监管机构均已公布了 eCTD v4.0 的实施时间表,预计 2027-2028 年将全面强制实施。
二、eCTD v4.0 的五大核心变革:注册人必须掌握
eCTD v4.0 基于 HL7 RPS(受监管产品提交)标准构建,与 v3.2.2 相比发生了根本性的变化。以下五大变革将直接影响每一位注册从业者的日常工作:
1. 单一 XML 报文:告别 "三文件时代"
这是最直观的变化。在 eCTD v3.2.2 中,每个提交序列需要生成index.xml、region.xml 和 stf.xml三个独立的 XML 文件。而在 v4.0 中,所有信息都整合到一个名为 submissionunit.xml 的主干文件中,大大简化了报文结构,降低了出错概率。
2. 革命性的文档复用机制:一次提交,终身复用
这是 eCTD v4.0 最核心的优势。v4.0 为每一个文档分配一个全球唯一的 UUID(通用唯一标识符)。一旦文档被监管机构接收并存储,后续在任何适应症、任何国家的申报中,都可以通过引用这个 UUID 来复用该文档,无需再次提交实体文件。
注册人解读:这意味着我们再也不用把同一个 "原料药质量标准" 复制粘贴到 10 个不同的申报资料包里了。对于拥有多个产品线的大型药企来说,这将节省海量的时间和精力。同时,文档的任何更新都会自动同步到所有引用它的地方,彻底解决了版本不一致的问题。
3. 基于“使用情境(CoU)”的生命周期管理
v4.0 引入了使用情境(Context of Use, CoU)的核心概念,取代了 v3.2.2 中的叶节点。一个使用情境代表 “一个文档在 CTD 目录中的一个特定位置”。
每个使用情境都有自己的生命周期状态(活跃/中止)
替换文档时,只需创建一个新的使用情境,并将旧的使用情境标记为 "作废"
彻底删除了容易引起混淆的“增补”操作,只保留“新增”、“替换”和“删除”三种基本操作
4. 情境组取代 STF:研究文件组织更清晰
在 v3.2.2 中,我们需要通过复杂的 STF 文件来组织临床和非临床研究的多个文档。而在 v4.0 中,STF 文件被彻底废除,取而代之的是情境组(Context Group)机制。
通过“使用情境代码 + 关键词代码”的组合,可以将多个相关文档自动分组到同一个研究项下。例如,所有与“Study-001”相关的文档,只要都加上 “studyID_$Study-001” 这个关键词,就会自动显示在 CTD 目录的同一个位置。
5. 标准化的关键词体系:实现智能检索
v4.0 建立了一套完整的标准化关键词体系,涵盖了原料药、制剂、生产商、适应症、剂型、研究 ID 等所有关键信息。所有关键词都通过受控词汇表进行管理,确保了术语的一致性。
注册人解读:这不仅方便了监管机构的检索和审查,也为企业内部的注册数据管理和分析提供了基础。未来,我们可以通过关键词快速筛选出所有“针对非小细胞肺癌”、“使用 XX 生产商原料药”的申报项目,实现真正的数字化管理。
三、对国内药企的三大挑战
eCTD v4.0 的实施是一把双刃剑,既带来了效率的提升,也对药企的注册体系提出了更高的要求:
1.系统和工具的全面升级
现有的所有 eCTD 编辑和验证工具都将无法支持 v4.0 格式。药企需要提前评估和采购新的 eCTD v4.0 软件,并完成与内部文档管理系统(DMS)、电子实验记录本(ELN)等系统的集成。
2.人员能力的重构
注册人员需要从 "文档排版员" 转变为 "元数据管理员"。我们不仅要懂 CTD 结构,还要懂 XML 语法、UUID 管理、使用情境设计、关键词配置等全新的知识。
3.内部流程的再造
文档复用机制要求企业建立统一的、中心化的注册文档库。所有文档的创建、审核、版本控制都必须遵循标准化的流程,确保每个文档的质量和唯一性。
四、国内实施展望与药企行动建议
结合 CDE 本次征求意见的进度和国际上的实施经验,我们对 eCTD v4.0 在国内的实施做出以下预测:
2026 年下半年:正式发布 eCTD v4.0 指导原则和实施通知
2027 年上半年:开始接受 eCTD v4.0 格式的申报,与 v3.2.2 并行
2028 年 1 月 1 日:全面强制实施 eCTD v4.0,不再接受 v3.2.2 格式
在此,我给国内药企提出以下几点行动建议:
1.立即启动学习和培训:组织注册、QA、IT 等相关部门人员系统学习 eCTD v4.0 的规范,重点掌握文档复用、使用情境和关键词体系
2.评估现有系统兼容性:与 eCTD 软件供应商沟通,了解其 v4.0 版本的开发进度和升级方案
3.建立中心化文档库:按照 v4.0 的要求梳理和规范现有注册文档,为未来的文档复用做好准备
4.选择试点项目:在正式实施前,选择 1-2 个简单的补充申请项目进行 v4.0 格式的模拟申报,积累经验
eCTD v4.0 与 v3.2.2 核心差异对照表
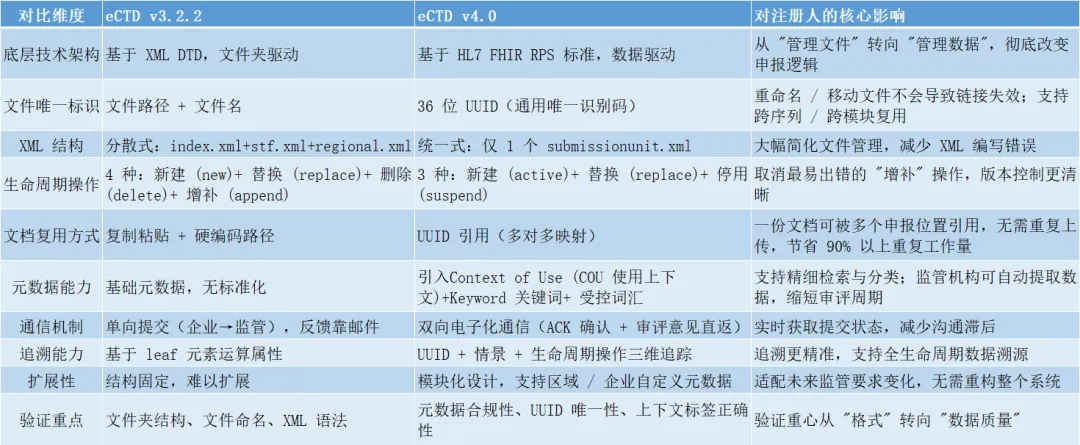
写在最后
eCTD v4.0 的实施是中国药品监管与国际接轨的又一重要里程碑。它不仅将提高药品注册的效率和透明度,也将推动中国药企更好地参与全球医药市场的竞争。
作为注册人,我们既是这场变革的见证者,也是参与者。虽然转型的过程会有阵痛,但长远来看,它将把我们从繁琐的重复劳动中解放出来,让我们有更多精力专注于注册策略的制定和与监管机构的沟通。
CDE 本次公开征求意见,也是为了充分听取行业的声音,确保 eCTD v4.0 在国内的顺利落地。建议大家结合自身的工作实践,积极反馈意见和建议,共同推动中国药品注册事业的发展。
注册人最容易踩坑的 10 个问题
1. 混淆 "文件" 与 "数据",仍用 v3.2.2 思维做 v4.0 申报
坑点:继续按文件夹结构组织文件,手动管理路径和链接,完全浪费 v4.0 的优势
避坑:提前建立企业级元数据库 (MDR),将所有申报文档按 UUID 统一管理,实现数据自动化流转
2. UUID 生成不规范,出现重复或冲突
坑点:手动生成 UUID,或使用非标准算法生成,导致全局唯一标识符冲突
避坑:使用 eCTD 软件自动生成 UUID;建立 UUID 管理系统,确保每个文档的 UUID 在企业内唯一且永久不变
3. 上下文标签 (COU) 使用错误
坑点:标签与文档内容不匹配,或使用非标准化标签,导致监管系统无法正确解析
避坑:严格遵循 ICH 和 NMPA 发布的 COU 受控词汇表;提交前用官方验证工具检查标签正确性
4. 生命周期操作错误,误用 "新建" 代替 "替换"
坑点:将更新后的文档以 "新建" 方式提交,导致历史版本混乱,审评人员无法看到完整变更轨迹
避坑:牢记:同一文档的更新必须用 "替换" 操作;只有全新的文档才用 "新建";删除文档用 "停用"
5. 元数据与文档内容不一致
坑点:文档内容修改后,未同步更新元数据标签,导致数据与内容脱节
避坑:建立元数据与文档内容的联动机制;每次修改文档后,自动触发元数据检查和更新
6. 跨序列复用文档时未验证引用有效性
坑点:引用了已被删除或替换的文档 UUID,导致申报资料出现 "死链接"
避坑:提交前运行全量引用检查;建立文档引用关系图谱,实时监控引用状态
7. PDF 文件不符合 v4.0 特殊要求
坑点:PDF 版本过高 / 过低、字体未嵌入、包含附件、有密码保护等,导致验证失败
避坑:使用专业的 PDF 合规工具批量处理;严格遵循 NMPA eCTD 验证标准中关于 PDF 的 24 条要求
8. 电子签名与证书问题
坑点:证书过期、证书链不完整、签名与证书不匹配,导致签名验证失败
避坑:提前检查证书有效期,确保覆盖整个项目周期;提交时包含完整的证书链;使用官方认可的数字证书
9. 忽视受控词汇的使用
坑点:使用自定义词汇代替 ICH/NMPA 规定的受控词汇,导致语义不一致,影响审评效率
避坑:建立企业内部受控词汇库,与官方词汇库同步更新;所有元数据标签必须使用受控词汇
10. 系统升级不彻底,新旧系统数据不兼容
坑点:仅升级 eCTD 提交软件,未打通内部 ERP、LIMS、EDC 等系统,导致数据孤岛
避坑:制定完整的系统升级和数据迁移计划;优先打通核心业务系统与 eCTD 系统的数据接口

 产业资讯
产业资讯
 E药经理人
E药经理人  2026-04-24
2026-04-24
 16
16

 产业资讯
产业资讯
 动脉网
动脉网  2026-04-24
2026-04-24
 17
17

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-04-24
2026-04-24
 15
15
 热门资讯
热门资讯