 产业资讯
产业资讯
 UmabsDB
UmabsDB  2026-04-24
2026-04-24
 4
4
多数人对复宏汉霖的认知,仍停留在PD-1百家争鸣的阶段:斯鲁利单抗Serplulimab、商业化能力以及其逐步推进的国际化路径。但在2026年AACR上,公司释放出的信号已经发生了明显变化。这一次公布的7项管线,并非简单意义上的“多靶点铺开”,而是围绕两条清晰的技术主线展开:一条是抗体偶联药物(ADC)的工程化升级,另一条是T细胞衔接器(TCE)的机制升级。在这两条主线之下,还隐含着一条更深层的创新方向,即对肿瘤免疫抑制底层机制的重新定义,尤其是围绕唾液酸-Siglec轴的探索。
这种从“分子开发”到“机制重构”的转变,使复宏汉霖开始具备从跟随型开发者迈向FIC/BIC竞争区间的潜力,其意义已经不再局限于单一产品,而在于平台能力的建立与外延。
一、TCE进入2.0阶段:从“激活T细胞”到“维持T细胞功能”
当前TCE的临床成功仍然高度集中在血液瘤领域,其核心靶点主要围绕CD20、BCMA、CD19及GPRC5D等抗原展开。而在实体瘤中,这一模式的效果始终受限,其根本原因并不在于T细胞是否能够被激活,而在于激活后的T细胞是否能够在高度抑制性的肿瘤微环境中持续发挥作用。换言之,第一代TCE解决的是“启动”,但尚未解决“持续”。
复宏汉霖的TCE平台正是围绕这一核心瓶颈展开,其关键设计在于引入CD28共刺激信号,从而在传统CD3介导的第一信号基础上,提供第二信号支持。这一策略并非简单叠加,而是针对实体瘤免疫抑制环境的一种结构性修复,试图在抗体体系中模拟CAR-T中已被验证的双信号激活机制。
以HLX3902为例,这一靶向STEAP1×CD3×CD28的三特异性抗体,在临床前数据中展现出的优势并不只是体现在杀伤强度上,而更多体现在功能的持续性上。在低效靶比条件下仍保持显著活性,并在极低剂量下表现出优于同类分子的抗肿瘤效果,同时能够显著促进T细胞的增殖、记忆形成及持续杀伤能力。这些特征指向一个更本质的问题:即TCE的竞争已经从“谁更强”转向“谁更持久”。
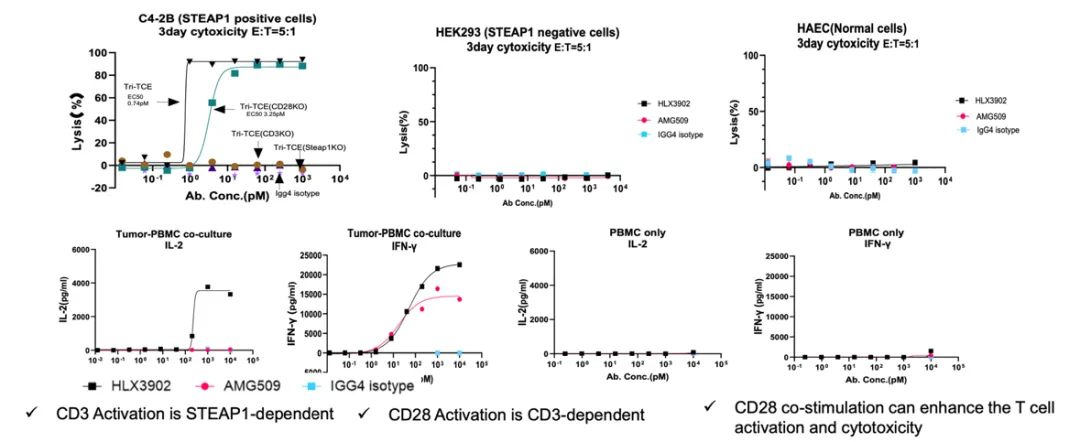
进一步来看,HLX3901作为DLL3双表位、CD3与CD28四特异性抗体,则在这一基础上向“条件性激活”迈进。通过双表位设计提升肿瘤选择性,同时结合CD28共刺激增强T细胞功能,该分子在低靶抗原密度环境中仍能保持有效杀伤能力。在与Tarlatamab等同类产品的对比中,其表现出更持久的抗肿瘤活性以及潜在更优的安全窗口,提示其在实体瘤领域具备进一步探索的空间。
从更宏观的角度来看,TCE赛道的竞争逻辑正在发生变化。过去的核心问题是能否有效激活T细胞,而现在的关键在于如何在肿瘤微环境中维持T细胞功能。复宏汉霖通过引入CD28信号,本质上是在尝试将CAR-T中的关键机制迁移至可规模化生产的抗体药物体系中,这一方向如果在临床中得到验证,将可能重新定义TCE在实体瘤中的应用边界。
二、ADC进入“可调毒性时代”:从payload强度到系统优化
ADC领域同样正在经历范式变化。过去行业普遍追求更高毒性的payload,但临床实践逐渐表明,高毒性往往限制给药剂量,从而削弱抗体本身的作用。ADC开发的核心矛盾,已经从“如何增强杀伤”转向“如何在毒性与暴露之间取得最优平衡”。 Hanjugator™平台正是在这一背景下提出,其核心不在于单一参数的提升,而在于通过模块化设计实现payload强度的可调节,并结合高亲水性连接子与优化DAR,使抗体功能与毒素作用形成协同。
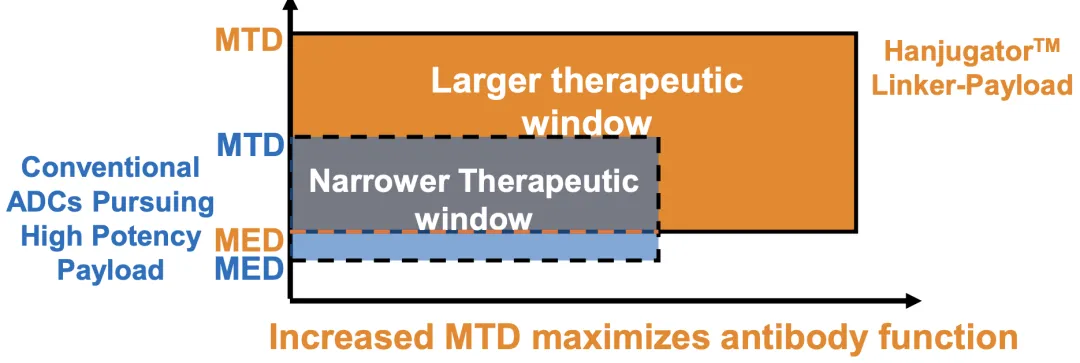
在这一体系中,HLX48(EGFR/c-MET双抗ADC)是最具代表性的核心资产之一。EGFR与c-MET的组合,本身即对应明确的生物学逻辑:二者在多种实体瘤中共表达,并在EGFR-TKI耐药过程中通过c-MET旁路激活形成关键驱动机制。因此,该靶点组合不仅具备广泛覆盖能力,也具备明确的耐药切入点。
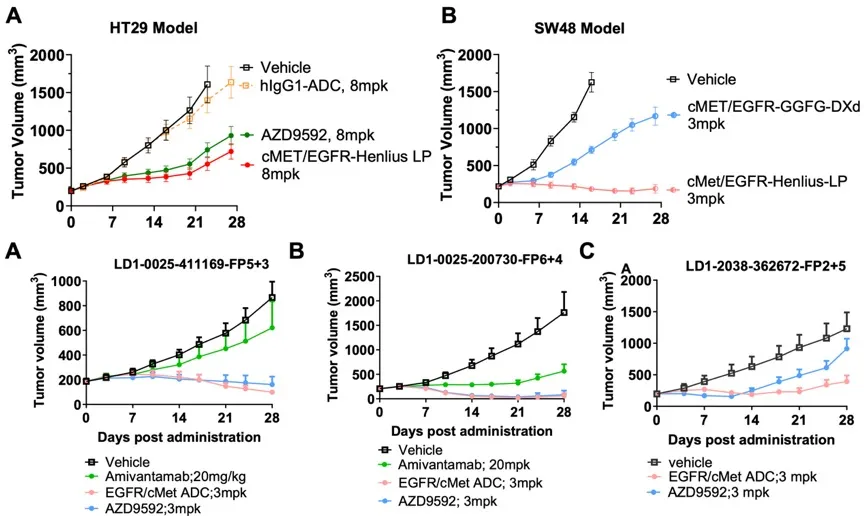
在竞争格局上,HLX48直接对标AZD9592等同类分子,但其设计路径呈现出明显差异。HLX48选择采用中等毒性payload,并通过高亲水性连接子与DAR约为4的设计,支持更高的临床给药剂量,从而实现更充分的受体占有率与药物暴露。这一策略并非追求单次杀伤能力,而是通过整体暴露水平提升抗肿瘤效果。
从临床前数据来看,HLX48在多种模型中展现出显著抗肿瘤活性,并在HT29结直肠癌等CDX和PDX模型中优于AZD9592。同时,在食蟹猴中高剂量给药下仍保持良好耐受性,验证了其中等毒性设计策略的可行性。这一点对于EGFR/c-MET这一类需要较高剂量覆盖的靶点尤为关键。
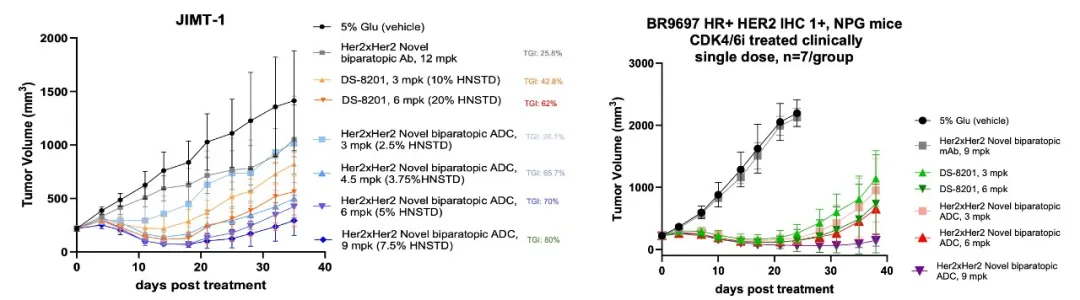
相比之下,HLX49(HER2双表位ADC)则代表另一种路径,即通过多表位设计提升内吞效率并扩大患者覆盖范围。在对标Trastuzumab
deruxtecan的过程中,其在HER2低表达及超低表达人群中展现出更广谱的抗肿瘤活性。
而HLX402(ADAM9 ADC)与HLX85(ALPP/ALPPL2
ADC)则体现了平台在不同维度的延展能力:前者通过重新设计连接子与payload解决历史毒性问题,后者则通过显著增强旁观者效应应对肿瘤异质性与耐药挑战。

整体来看,复宏汉霖的ADC策略已经从“单分子优化”转向“系统工程优化”,而HLX48作为其中最具竞争力的代表,承担着进入BIC竞争区间的关键角色。
三、从“功能叠加”到“机制协同”:IO与ADC的融合路径
在当前管线中,HLX43(PD-L1 ADC)体现了IO与ADC融合的经典路径。该分子通过将免疫检查点阻断与细胞毒杀伤结合,同时诱导免疫原性细胞死亡并增强T细胞浸润,从而在免疫激活与直接杀伤之间形成协同。这一方向在行业中已有初步验证,其价值在于通过单一分子实现多机制叠加,从而在一定程度上替代联合疗法。但其本质仍属于“功能整合”,而非机制层级的跃迁。
此外,复宏汉霖亦在探索一些更前沿的免疫调节方向,例如HLX316等分子,通过调节肿瘤微环境中的免疫抑制因素,进一步增强免疫效应。这类策略目前仍处于早期阶段,其临床价值有待后续数据验证,但在组合疗法体系中,可能为增强免疫应答提供补充路径。
四、从免疫检查点到“糖免疫检查点”:机制层级的跃迁
在所有管线中,真正体现差异化潜力的,是对免疫抑制底层机制的探索。HLX43作为PD-L1 ADC,延续了“免疫检查点阻断+细胞毒杀伤”的经典组合逻辑,其价值在于将IO与ADC机制整合,从而在免疫激活与直接杀伤之间形成协同。
但更具创新性的,是HLX316这一B7-H3靶向唾液酸酶融合蛋白。该分子的切入点并非传统的免疫检查点,而是肿瘤细胞表面的异常唾液酸化修饰。这一修饰通过与免疫细胞上的Siglec受体结合,从而抑制免疫反应。HLX316通过局部去唾液酸化,解除这一“糖免疫检查点”,从而恢复免疫细胞功能。
从数据来看,该分子在靶向条件下的去唾液酸化活性较非靶向形式提升超过1000倍,并在多种模型中表现出优于B7-H3抗体、非靶向酶及PD-1抗体的疗效。这一结果的意义在于,其作用层级可能位于传统PD-1通路之上,直接作用于免疫抑制的上游机制。如果传统IO针对的是信号通路层面的抑制,那么HLX316则切入了更底层的生化与物理屏障,其影响不仅体现在免疫信号,还可能涉及免疫突触形成与细胞间相互作用。这种从“checkpoint”向“immune substrate”的转变,代表了免疫治疗范式的一次潜在跃迁。
五、“组合能力”的价值:从单品到体系
如果单独看每一个分子,这些项目可以被理解为具有差异化潜力的候选药物。但当它们被放在同一体系中时,其意义发生了质的变化。复宏汉霖当前的管线,已经初步形成一个功能闭环:TCE用于激活T细胞,ADC用于直接杀伤肿瘤,而IO类分子则在免疫调节中提供支持。这种“激活—杀伤—调节”的组合逻辑,使不同技术平台之间具备天然的协同关系。
这一模式在行业中已有成功先例,例如Atezolizumab与Bevacizumab的联合。但复宏汉霖的差异在于,其核心组合资产主要来源于内部平台,而非依赖外部引进。这意味着其在联合策略设计与临床开发路径上拥有更高的自主性。
从BD与投资视角来看,这种变化具有重要意义。Biotech的价值正在从单一产品授权,转向平台与组合疗法的
结语:从产品驱动到”平台驱动”的关键一步
如果用一句话总结复宏汉霖在此次AACR上的变化,那就是其正在从一家以单一抗体产品为核心的公司,转向具备体系化创新能力的平台型的Pharma。真正值得关注的,并不是某一个分子的短期成败,而是其是否已经建立起一个可以持续产生差异化组合的能力结构。从CD28共刺激TCE,到以HLX48为代表的系统优化型ADC,再到IO融合与微环境调节的探索,这家公司正在逐步构建一个多层次的抗肿瘤治疗体系。而这一体系能否在临床中转化为真实的竞争优势,将决定其在下一阶段全球创新药格局中的位置。

 产业资讯
产业资讯
 E药经理人
E药经理人  2026-04-24
2026-04-24
 3
3

 产业资讯
产业资讯
 动脉网
动脉网  2026-04-24
2026-04-24
 3
3

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-04-24
2026-04-24
 3
3
 热门资讯
热门资讯