 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2025-12-08
2025-12-08
 2346
2346
当地时间 12 月 3 日,礼来宣布,美国 FDA 已批准 Jaypirca(Pirtobrutinib,匹妥布替尼,100mg 和 50mg 片剂)用于治疗既往接受过共价 BTK 抑制剂治疗的复发或难治性慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)成人患者。
同时,FDA 已将原定于 2023 年 12 月获得的用于治疗后期 CLL/SLL 的加速批准转为常规批准。

来源:礼来官网
此次批准基于 BRUIN CLL-321 研究的结果。这是一项随机、开放标签的 III 期研究,共入组 238 名受试者,随机分组接受匹妥布替尼和研究者选择的 IdelaR(艾代拉利司+利妥昔单抗) 或 BR(苯达莫司汀+利妥昔单抗)治疗。主要终点是 IRC 评估的 PFS。结果显示,PFS 风险比(HR)为 0.54,匹妥布替尼组的中位 PFS 为 14 个月,对照组为 8.7 个月。

来源:丁香园 Insight 数据库
匹妥布替尼是一款高选择性、非共价(可逆)BTK 抑制剂,最初由 Redx Pharma 研发,2017 年 7 月被 Loxo Oncology 买入。2019 年 1 月,礼来 80 亿美元收购 Loxo Oncology,获得了该产品。2024 年 12 月,信达生物引进了匹妥布替尼在中国大陆的进口、销售、推广和分销权益。
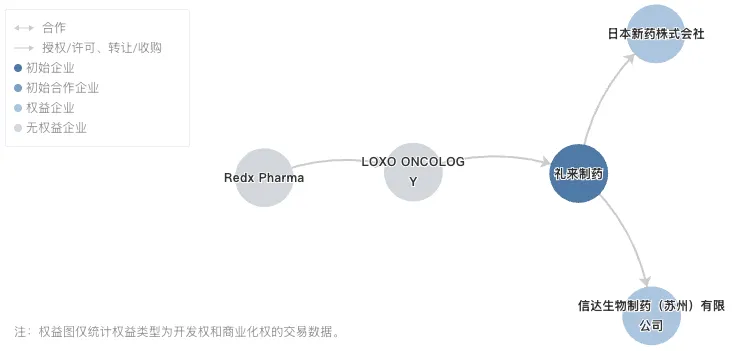
来源:丁香园 Insight 数据库
2023 年 1 月,匹妥布替尼率先在美国获批上市,目前已斩获多项适应症,分别为复发或难治性套细胞淋巴瘤(MCL)三线治疗、复发或难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)二线和三线治疗。
2024 年,匹妥布替尼收入 3.37 亿美元,今年前三季度收入了 3.58 亿美元。此次适应症拓展,将进一步促进该产品销售额的增长。
出处:

 研发追踪
研发追踪
 药渡
药渡  2026-05-27
2026-05-27
 523
523

 研发追踪
研发追踪
 医药笔记
医药笔记  2026-05-26
2026-05-26
 460
460

 研发追踪
研发追踪
 佰傲谷BioValley
佰傲谷BioValley  2026-05-26
2026-05-26
 476
476
 热门资讯
热门资讯