 国际交流
国际交流
 中国医药创新促进会
中国医药创新促进会  2025-12-12
2025-12-12
 5296
5296
2025年11月15-19日,ICH大会在新加坡顺利召开。本次大会上,尼日利亚食品药品监督管理局(NAFDAC)与南非卫生产品监管局(SAHPRA)正式成为ICH成员;多米尼加共和国药品监管总局(DIGEMAPS)与菲律宾食品药品监督管理局(Philippine FDA)新增为ICH观察员。目前,ICH共有25个成员和41个观察员。
此次大会期间,MedDRA指导委员会(MedDRA Steering Committee)和12个议题工作组召开了工作会议,共同推动指导原则的国际协调。中国医药创新促进会(以下称“我会”)五位工作组组长受邀现场参会,代表国际药品制造商协会联合会(以下称“IFPMA”)各工作组参与相关指导原则的修订讨论,具体如下:
MedDRA指导委员会
组长:郭晓军,和黄医药药物安全与警戒副总裁
MedDRA指导委员会的主要职能是管理、支持和促进监管活动医学词典(以下称“MedDRA”)的维护、开发和传播。MedDRA每年更新两次,最新版本28.1支持27种语言,包括新增的挪威语、斯洛伐克语和斯洛文尼亚语。为了更好的支持用户培训,今年初MSSO(Maintenance and Support Services Organization)推出了MedDRA学习管理系统(LMS),MedDRA用户可以通过在线学习获得证书和徽章。此外,在MedDRA.org网站上发布了新的培训视频《使用MedDRA编码生产和质量体系问题》。
Q6(R1):质量标准指导原则的修订
组长:安振明,齐鲁制药生物技术开发研究院执行院长
ICH Q6专家工作组在新加坡会议前完成了草案全文的撰写并在工作组内部进行了一轮审阅,此次会议针对审阅中征集到的主要问题进行了针对性的讨论,达成一致或明确调整方向;此外,工作组对全文的结构进行了讨论和优化,在进一步提升逻辑清晰度的同时,为生物药、化药及其他新型药物形式提供更多指导。会后,Q6专家组将按照新加坡会议的讨论和决定,对指南草稿进行调整、补充和修改,于2026年3月和4月进行成员机构审阅(Constituency Review)。
会议期间,Q6专家组还与S13、Q1专家组进行了交流讨论,以期提升各指南间的一致性。
S13:寡核苷酸治疗产品的非临床安全性研究
组长:弓雪莲,上海京新生物非临床评估部药代毒理总监
S13专家组于2024年11月完成了概念性文件的撰写和递交,2025年6月完成了指导原则大纲编写。本次会议旨在落实指导原则主体部分的协调和撰写。会议期间与ICH E14/S7B和Q6指导原则专家组进行了良好互动和交流,为不同领域指导原则的协调统一与优化完善奠定了坚实基础。
M11:临床电子结构化协调方案(CeSHarP)
组长:李文斌,首都医科大学附属北京天坛医院肿瘤综合治疗中心主任
本次会议聚焦M11指导原则的落地推进,围绕最终交付物的定稿与签批、培训体系建设、变更管理机制确立等核心议题展开深入研讨。会议最终达成多项关键成果:完成CeSHarP协议交付物正式签批,确定8个核心培训模块的交付方案,起草了2026年对于培训模块审批应用的计划。
M18:确定生物类似药开发计划中有效性比对研究价值的框架
组长:窦昌林,博安生物首席运营官、研发总裁、执行董事
M18专家工作组在本次会议上讨论完成了“确定生物类似药开发计划中有效性比对研究价值的框架(Framework for Determining the Utility of Comparative Efficacy Studies in Biosimilar Development Programs)”文件并提交大会审批。M18专家工作组目前已经启动了后续指导原则文件结构和内容的初步讨论,并制定了工作计划,将在2026年5月的巴西里约热内卢ICH大会上报告阶段性成果。

IFPMA参会代表(第二排右一至四分别为:窦昌林、
安振明、李文斌、弓雪莲,第二排左二:郭晓军)

M18专家工作组参会代表(第三排右一:窦昌林)

Q6专家工作组参会代表(第三排左五:安振明)

MeDRA指导委员会参会代表(第一排右二:郭晓军)
会议期间,专家们还同中国药监局、欧洲药品管理局(EC)、美国食品药品监督管理局(FDA)、日本药品和医疗器械管理局(PMDA)及IFPMA成员单位的专家进行深入交流。作为IFPMA相关指导原则工作组的组长,五位专家履职尽责,牵头组织工作组会议,统筹推进有关工作,并亲临会议现场参加ICH大会,深度参与指导原则制修订的各项工作,为搭建全球产业界与监管机构的对话桥梁,推动中国产业标准与国际标准全面接轨做出了积极贡献,提升了中国在全球医药规则制定中的参与度和影响力,为促进全球医药创新注入中国智慧。
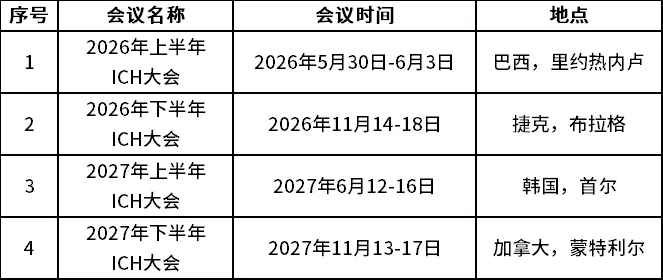
截至2025年11月,我会已向IFPMA 32个ICH工作组推荐了70位专家(包括13位组长,10位候补组长),占IFPMA全球专家总数的43%。ICH大会上也公布了未来两年的会议安排,我会也将继续积极组织协调相关工作组专家参会,深度参与国际标准的制修订进程,持续代表中国药促会和中国医药产业界传递行业声音,推动全球医药产业高质量发展!

 国际交流
国际交流
 中国医药创新促进会
中国医药创新促进会  2026-02-10
2026-02-10
 5379
5379

 国际交流
国际交流
 中国医药创新促进会
中国医药创新促进会  2026-02-06
2026-02-06
 5173
5173

 国际交流
国际交流
 中国医药创新促进会
中国医药创新促进会  2026-01-15
2026-01-15
 5298
5298
 热门资讯
热门资讯