 产业资讯
产业资讯
 丁香园Insight数据库
丁香园Insight数据库  2026-05-16
2026-05-16
 308
308
5 月 15 日,NMPA 官网显示,艾伯维申报的艾可瑞妥单抗获批上市,联合利妥昔单抗和来那度胺适用于治疗复发或难治性滤泡性淋巴瘤(FL)成人患者。(受理号:JXSS2500127/8)。此前该申请曾被纳入优先审评。

截图来源:NMPA 官网
艾可瑞妥单抗最初由 Genmab 公司开发 ,艾伯维在 2020 年与 Genmab 达成一项总额达 39 亿美元的合作,以共同开发和商业化 Genmab 的三种下一代双抗产品,其中就包括艾可瑞妥单抗(Epcoritamab)。

截图来源:Insight 数据库
作为一款 IgG1 双特异性抗体,艾可瑞妥单抗可同时与 T 细胞上的 CD3 和 B 细胞上的 CD20 结合,并诱发 T 细胞介导的淋巴瘤 B 细胞杀伤。CD20 是经过临床验证的治疗靶点,并且在许多 B 细胞恶性肿瘤上表达,包括弥漫性大 B 细胞淋巴瘤、滤泡性淋巴瘤、套细胞淋巴瘤和慢性淋巴细胞白血病。
艾可瑞妥单抗于 2023 年 5 月迎来全球首批。截至目前,其已在美国、欧盟、日本等多个国家和地区获批上市,适应症包括大 B 细胞淋巴瘤、滤泡性淋巴瘤。2025 年,艾可瑞妥单抗的全球销售额已达到 4.68 亿美元。本次为艾可瑞妥单抗在中国的首次获批。
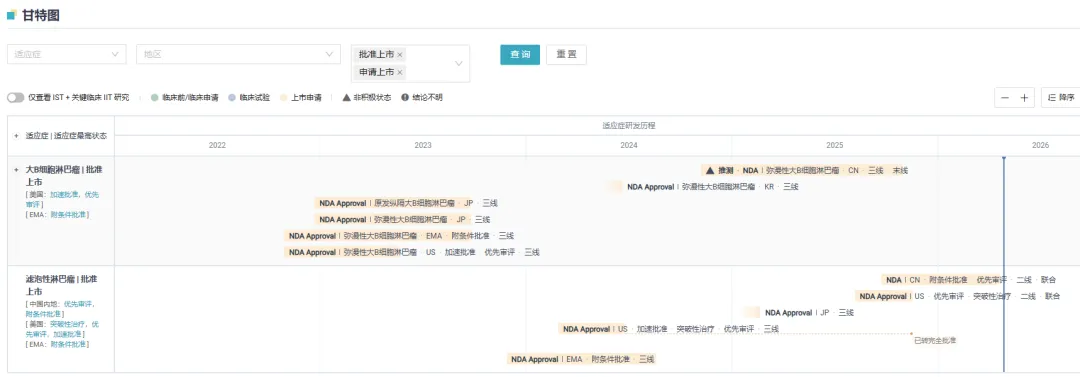
截图来源:Insight 数据库
关键 III 期临床研究 EPCORE FL-1(CTR20230864/CTR20234072)中,研究人员在复发/难治性 FL 患者中评估了艾可瑞妥单抗+利妥昔单抗+来那度胺和利妥昔单抗+来那度胺相比的安全性和有效性,对照组为利妥昔单抗+来那度胺。试验的双重主要终点是 ORR 和 PFS,其研究数据在 2025 年 ASH 大会亮相。
数据显示,与利妥昔单抗+来那度胺治疗相比,艾可瑞妥单抗+利妥昔单抗+来那度胺治疗可使疾病进展或死亡风险降低 79%(HR 0.21,p<0.0001)。此外,接受艾可瑞妥单抗+利妥昔单抗+来那度胺治疗的患者 ORR 为 95%,而接受利妥昔单抗+来那度胺治疗治疗的患者 ORR 为 79%。
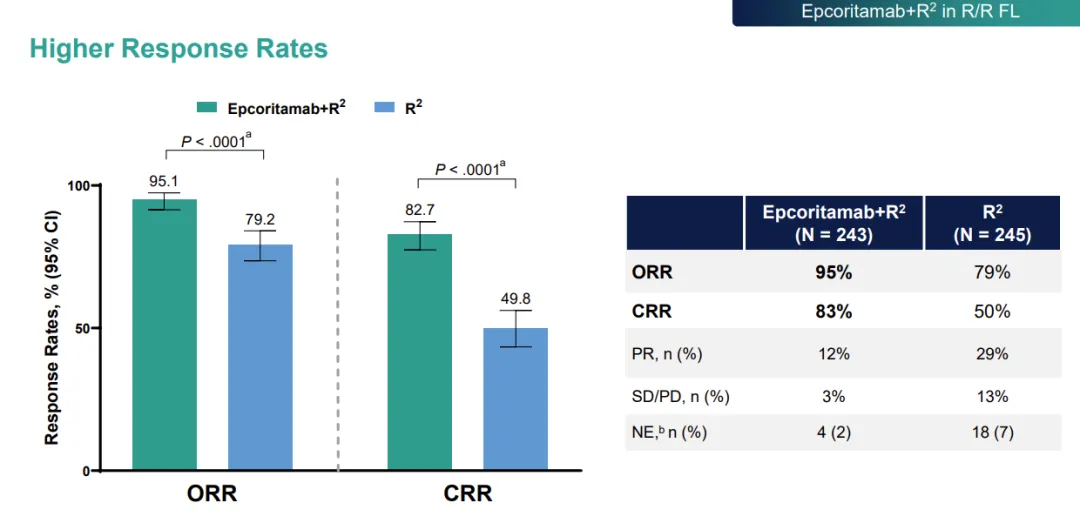
截图来源:Genmab 官网
在国内,除了 EPCORE FL-1 以外,艾伯维还针对该药开展 4 项 III 期临床试验:
艾可瑞妥单抗对比研究者选择的化疗治疗复发性/难治性弥漫大 B 细胞淋巴瘤(CTR20221558);
艾可瑞妥单抗联合 R-CHOP 治疗新诊断的弥漫大 B 细胞淋巴瘤(CTR20231626/CTR20231627);
艾可瑞妥单抗联合利妥昔单抗和来那度胺(R2)用于既往未接受过治疗的滤泡性淋巴瘤(CTR20243120);
艾可瑞妥单抗联合联合口服来那度胺片用于复发性或难治性弥漫大 B 细胞淋巴瘤(CTR20244540/CTR20244542)。
结语
CD20×CD3 双抗是血液瘤领域的热门药物。Insight 数据库显示,全球范围内现有 4 款 CD20×CD3 双抗获批,分别为罗氏/渤健的莫妥珠单抗、罗氏的格罗菲妥单抗、艾伯维/Genmab 的艾可瑞妥单抗、再生元/再鼎医药的奥德罗奈昔单抗.
在国内,目前除了奥德罗奈昔单抗(国内处于临床 II 期),其余 3 款均已获批。除此之外,还有 10 余款 CD20×CD3 双抗已进入临床阶段,来自正大天晴(临床 III 期)、神州细胞(临床 III 期)、君实生物(临床 II 期)、康诺亚(临床 I/II 期)等。

 产业资讯
产业资讯
 丁香园Insight数据库
丁香园Insight数据库  2026-05-16
2026-05-16
 308
308

 产业资讯
产业资讯
 动脉网
动脉网  2026-05-16
2026-05-16
 398
398

 产业资讯
产业资讯
 E药经理人
E药经理人  2026-05-16
2026-05-16
 412
412
 热门资讯
热门资讯