 产业资讯
产业资讯
 猎药人俱乐部
猎药人俱乐部  2025-01-10
2025-01-10
 2530
2530
FiercePharma近期报道,GlobalData已将心力衰竭列为下一个GLP-1类药物的掘金地。分析师预计,包括礼来替尔泊肽(Zepbound)和诺和诺德司美格鲁肽( Wegovy)在内药物的上市将在十年内帮助心衰市场规模增加200亿美元。
分析师称,2022年美国、欧洲五大市场和日本的心力衰竭药物销售额总计为135亿美元。他们预测,到2032年,该市场价值将达到337亿美元。

01
未满足需求仍存,慢性心衰用药蓝海市场
心力衰竭(Heart Failure,HF)是由于多种原因导致的心脏结构和/或功能异常,使心脏在静息或运动时难以有效地收缩和/或充盈,导致心输出量下降或心腔内压力增高,引起相关症状(如呼吸困难、疲乏)和/或体征(如颈静脉压力升高、肺部啰音和外周水肿)。心衰是多种心血管病的严重表现或中晚期阶段,是严重危及生命的临床综合征,具有高发病率、高死亡、不良预后等特点。
2024版中国心衰诊断和治疗指南根据左心室射血分数(LVEF)的不同和治疗后的变化,将心衰分为射血分数降低的心衰(HFrEF)、射血分数轻度降低的心衰(HFmrEF)和射血分数保留的心衰(HFpEF)三大类别。如果从发病时间和进展速度上来分类,心衰包括慢性心衰和急性心衰两种,多数急性心衰患者经住院治疗后症状部分缓解,而转入慢性心衰,慢性心衰患者常因各种诱因急性加重而需住院治疗。
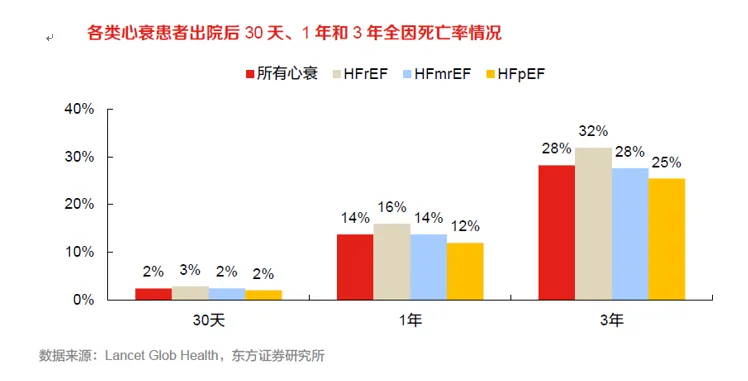
根据WangH等的全国队列研究,中国心衰患者出院后3年全因死亡率为28.2%,其中HFrEF患者3年全因死亡率高达31.9%,所有死亡中71.5%归因为心血管死亡,这表明慢性心衰治疗仍然存在较大未满足需求。
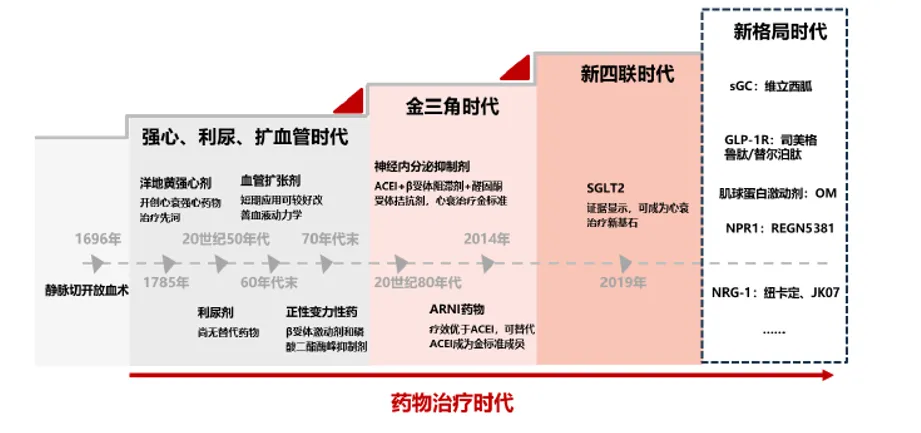
20世纪80年代以来随着基础研究证实,神经内分泌系统的异常激活参与和促进了心肌重构,随后一系列的大样本RCT证实具有抑制神经内分泌激活作用的药物可改善心衰的预后,心衰药物治疗进入“金三角”时代。最开始的金三角药物包括肾素‐血管紧张素系统(RAS)阻滞剂、β‐受体阻滞剂、盐皮质激素受体拮抗剂(MRA)三种药物。2014年诺华发布沙库巴曲缬沙坦(诺欣妥)III期研究数据,头对头击败依那普利后,全球各国指南开始陆续将ARNI药物加入指南,并建议使用在ARNI替代ACEI或ARB药物,因而成为新一版“金三角”。近年来,维立西胍、GLP-1R(司美格鲁肽、替尔泊肽)等药物也在临床研究中展现对慢性心衰的获益,同时还有肌球蛋白激动剂、NPR1、NRG-1等众多研究方向。
02
海外药企主导慢性心衰在研管线,GLP-1R类药物有望成为慢性心衰治疗新选择
心衰药物研发的难点不仅在于复杂的病理机理,同时临床设计也具有挑战性。根据2024年CDE发布《治疗慢性心力衰竭药物临床试验技术指导原则》,慢性心衰的主要治疗目标是降低心血管死亡率以及预防临床状态恶化和住院,这些目标应作为慢性心衰新药开发的主要疗效评价指标。因此在确定性临床中一般需要选择死亡率、心衰恶化临床或两者结合复合终点。
基于此,慢性心衰药物需要开展长期、大规模和昂贵的临床试验,一般企业难以承担大规模、国际多中心RCT临床的费用和时间成本,这也是近年来上市的心衰新药均归属于大型跨国药企的原因之一。其中诺华于2009年启动诺欣妥慢性心衰的III期临床项目PARADIGM-HF,PARADIGM-HF研究历时5年时间,纳入8442例患者。阿斯利康的达格列净DAPA-HF项目入组4744例患者,BI的恩格列净EMPEORReduced项目入组3730例患者。
据不完全统计,针对慢性心衰适应症,全球II期及以后的临床开发阶段品种28个,其中有5款为国产,信立泰独占2款,恒瑞医药,天士力和泽生科技分别有1款。
礼来:替尔泊肽
替尔泊肽作为全球首款上市的GLP-1/GIP双重受体激动剂,目前已经获批降糖和减重适应症。从全球销售数据看,2024年前三季度,减重版替尔泊肽(Zepound)收入30.18亿美元,降糖版(Mounjaro)收入80.1亿美元,两者合计贡献了110.28亿美元营收,占礼来前三季度总收入的34%左右。
值得注意的是,2024年12月FDA批准Zepbound(tirzepatide)治疗肥胖人群的中度至重度阻塞性睡眠呼吸暂停(OSA)的新适应症,成为首个获得FDA批准用于直接治疗OSA的药物,打破了该疾病长期无明确适应症药物获批的困境,标志着OSA治疗将步入新时代。
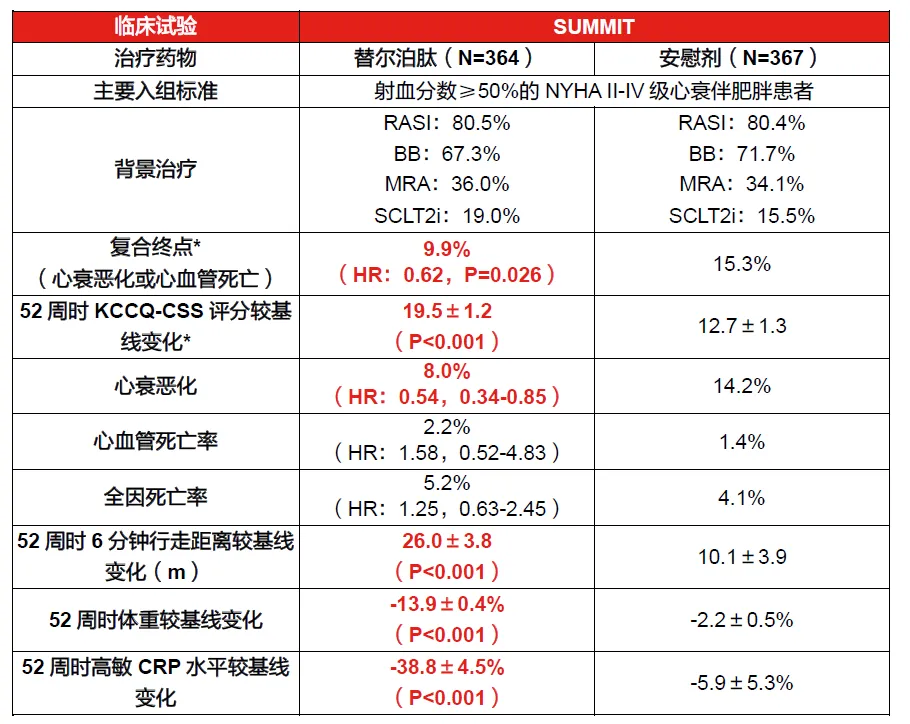
基于SUMMIT(替尔泊肽对HFpEF合并肥胖患者的研究)III期临床研究取得了积极结果:Tirzepatide在复合终点评估中相比安慰剂显示出心衰事件风险降低38%,并显著减少心衰住院风险56%。此外,与安慰剂组的15分改善相比,tirzepatide治疗组的患者在堪萨斯城心肌病问卷临床总结评分(KCCQ-CSS)中取得了近25分的提升,该问卷用于评估心衰相关症状和身体活动受限情况。礼来也于去年11月份向全球监管机构递交替尔泊肽治疗射血分数保留的心力衰竭(HFpEF)合并肥胖患者的适应症上市申请,有望成为该类患者的治疗新选择。
诺和诺德:司美格鲁肽
司美格鲁肽(Semaglutide)由糖尿病制药巨头诺和诺德开发,是一种新型的长效胰高糖素样肽‑1受体激动剂(GLP‑1RA )。2017年12月,司美格鲁肽首次在美国FDA获批上市,2018年2月于欧盟获批上市,2021年4月在我国批准上市。2024年前三季度,司美格鲁肽合计销售额达203.06亿美元,占到诺和诺德营收的69%。
与达格列净适应症从糖尿病逐渐扩展至慢性肾脏病、全射血分数心衰患者心血管死亡等领域一样,司美格鲁肽也在多个适应症有所布局。
值得关注的是,去年9月,诺和诺德宣布2.4mg Wegovy(司美格鲁肽)获欧洲药品管理局人用药品委员会(CHMP)推荐批准用于治疗肥胖相关射血分数保留型心衰(HFpEF),也成为第一款被推荐批准用于治疗心衰的GLP-1药物。
CHMP此次推荐批准主要是基于两项III期研究(STEP HFpEF和STEP HFpEF-DM)的积极结果:
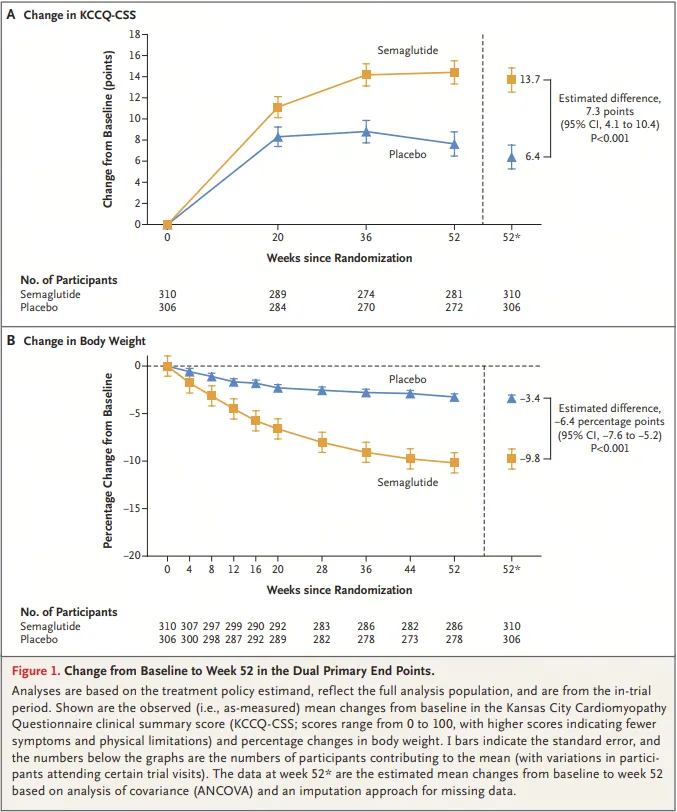
在安慰剂对照的STEP HFpEF研究(n=529)中,治疗52周后,2.4mg Wegovy既可减轻不伴2型糖尿病的肥胖合并HFpEF患者的体重(-13.3% vs. -2.6%,p<0.001),也可减轻这类患者的心衰相关症状(p=0.001)。此外,患者的运动功能也显著改善。
在安慰剂对照的STEP HFpEF-DM研究(n=616)中,治疗52周后,2.4mg Wegovy既可减轻伴2型糖尿病的肥胖合并HFpEF患者的体重(-9.8% vs. -3.4%,p<0.001),也可减轻这类患者的心衰相关症状(p<0.001)。此外,患者的运动功能同样显著改善。
信立泰:阿利沙坦酯+沙库巴曲-S086
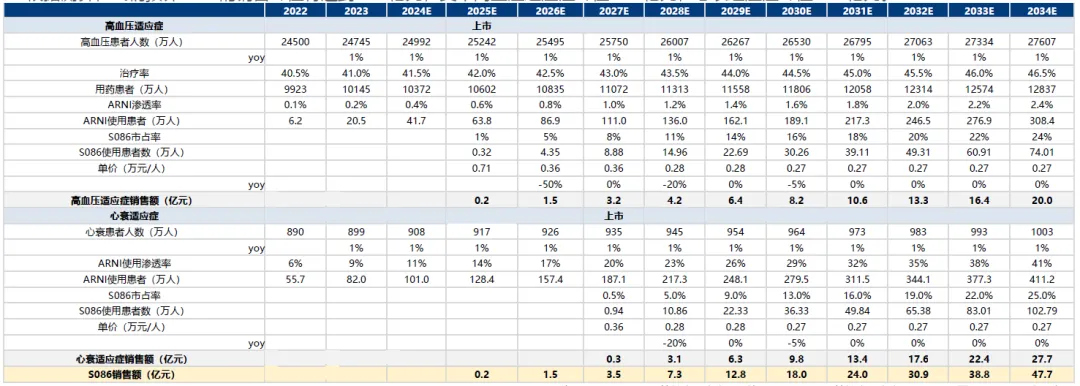
信立泰的沙库巴曲阿利沙坦钙(S086)是继诺欣妥后全球第二款血管紧张素受体-脑啡肽酶双重抑制剂(ARNI),S086由沙库巴曲和阿利沙坦酯共晶形成,拟用于原发性高血压患者和慢性心衰患者的治疗。目前,S086高血压适应症已向NMPA申报上市,预计2025H1获批上市,心衰适应症正在进行III期临床试验的入组,预计2025H1完成入组。
根据华创证券的测算,预计S086的销售峰值将达到47.7亿元,其中高血压适应症峰值20.0亿元,心衰适应症峰值27.7亿元。
信立泰:SAL007(JK07)
JK07是信立泰美国子公司SalubrisBio自主研发的神经调节蛋白-1(NRG-1)融合抗体药物,拟开发适应症为射血分数减少的慢性心衰(HFrEF)和射血分数保留的慢性心衰(HFpEF),是公司首个中美双报的创新品种。
根据JK07公布的专利来看(CN113166218A),JK07将NRG-1片段(NRG-1β2a型)通过连接子与HER3抗体重链的C端融合。相比于rhNRG-1,JK07融合了NRG-1片段和抗HER3抗体两个蛋白片段,既降低了患癌风险和胃肠道毒性,同时也解决了NRG-1半衰期短的问题。通过独特的分子设计,解决了rhNRG-1蛋白疗法的局限性,提高成药性和安全性。

根据Ib临床(NCT04210375)数据显示,JK07美国Ib临床研究包括三个剂量组(0.03mg/kg、0.09mg/kg和0.27mg/kg),共纳入14名NYHAII/III级心衰患者(入组标准剔除NYHA
IV级患者),其中每个剂量组第1例患者为哨兵数据,之后4例受试者按照3:1比例随机分配JK07和安慰剂。
试验结果显示,JK07单次给药(静脉注射60分钟)可使LVEF呈现具有临床意义的改善,且靶点相关的替代生物标志物(NT pro-BNP)呈剂量依赖性改变。D180后,中、高剂量组LVEF平均改善≥31%,其中中剂量组LVEF平均改善达49%,左心室射血分数绝对水平重回40%,提示对HFrEF治愈潜力。
JK07 II期临床分为0.045mg/kg低剂量组和0.09mg/kg高剂量组,每四周静脉注射一次,两个队列患者将随机接受低剂量JK07、高剂量JK07和安慰剂治疗。2024年4月底美国首例患者入组,截至6月底已入组8-10人,预计国内8、9月也将启动入组,年底前计划合计入组人数达60-70人并读出中期数据。在低剂量确认安全性后,2025年将开启高剂量组入组。
泽生科技:重组人纽兰格林
纽兰格林(Neuregulin-1,神经调节蛋白-1)是体内参与细胞分化、增殖、生长、存活和凋亡的信号蛋白,通过与其在体内受体(主要为酪氨酸激酶受体家族ErbB4/2的异源二聚体)的相互作用来传递细胞信号。NRG-1/ErbB配体与受体的结合与激动可启动细胞内信号传导级联反应,从而调节各种生理和病理过程。
泽生科技周明东团队在全球范围内最先发现,NRG-1与受体蛋白ErbB4/2结合并激活的下游生物学信号通路,对心脏发育及维持心肌细胞结构与功能十分关键,破坏信号可以导致心脏发育缺陷乃至胚胎死亡。进一步研究表明,重组人纽兰格林可使受损心肌细胞恢复肌节排列、促进心肌细胞收缩单元的组装、改善心肌细胞纤维结构和功能1。在此基础上,泽生科技研发出重组人纽兰格林(纽卡定,rhNRG-1),其来源于人体内自然存在的纽兰格林活性多肽片段,全长61个氨基酸,拟开发成为全球首个通过改善心肌细胞结构和功能治疗慢性心力衰竭的生物药。
2024 年11 月18 日,泽生科技发布公告称ZS-01-308B 试验未达到预设的统计目标,将继续推进用于支持药物常规完整获批的生存率获益确证性临床 III 期试验(ZS-01-306),该试验目前已入组受试者 243 例。重组人纽兰格林在既往以全因死亡率为终点的临床试验中,在全体人群中较安慰剂组降低死亡风险但未达统计学显著。通过事后亚组分析确定了目标患者亚组,在该群体中除301试验均取得显著结果。
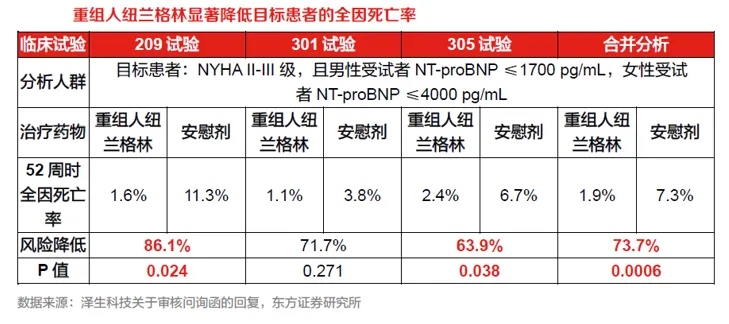
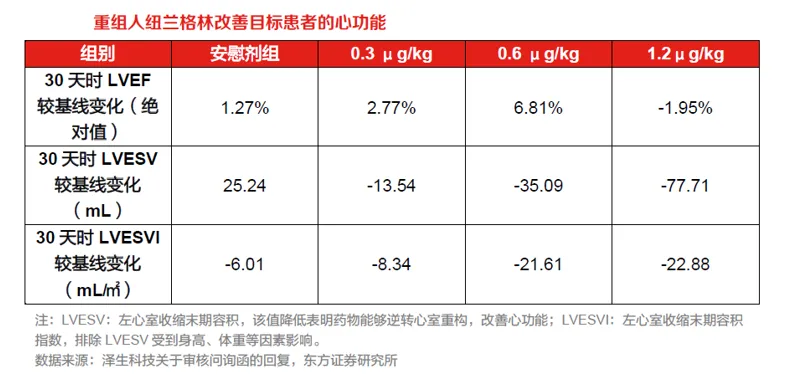
重组人纽兰格林在既往II 期临床试验(ZS-01-206)中同样表现出改善目标患者心功能的作用,但相对安慰剂组未达统计学显著。

 产业资讯
产业资讯
 研发客
研发客  2026-03-24
2026-03-24
 13
13

 产业资讯
产业资讯
 深蓝观
深蓝观  2026-03-24
2026-03-24
 17
17

 产业资讯
产业资讯
 药智网
药智网  2026-03-24
2026-03-24
 50
50