 产业资讯
产业资讯
 药融圈
药融圈  2025-03-18
2025-03-18
 2166
2166
药融圈获悉:2024财年诺华制药(Novartis)方面数据显示,所负责区域的自身免疫领域Xolair(茁乐)/奥马珠单抗(Omalizumab)业绩为16.43亿美元,同比增长12%。原研药由诺华和罗氏(Roche,负责美国市场)等企业合作开发(最早由华人公司Tanox发明)。(Tanox出来了很多抗体领域科学家,回国创业的也不少)
2024年2月,美国FDA批准了Xolair(奥马珠单抗)用于IgE介导的食物过敏,这是全球首款也是唯一一款获得FDA批准的食物过敏药物,基于OUtMATCH(NCT03881696)临床试验数据。罗氏负责的区域2024年业绩涨幅为5%,达63亿瑞士法郎,约合27.09亿美元。2024财年,Xolair(茁乐)/奥马珠单抗(Omalizumab)累计销售约43.52亿美元。2家业绩2023年全球销售额约合38.95亿美元。

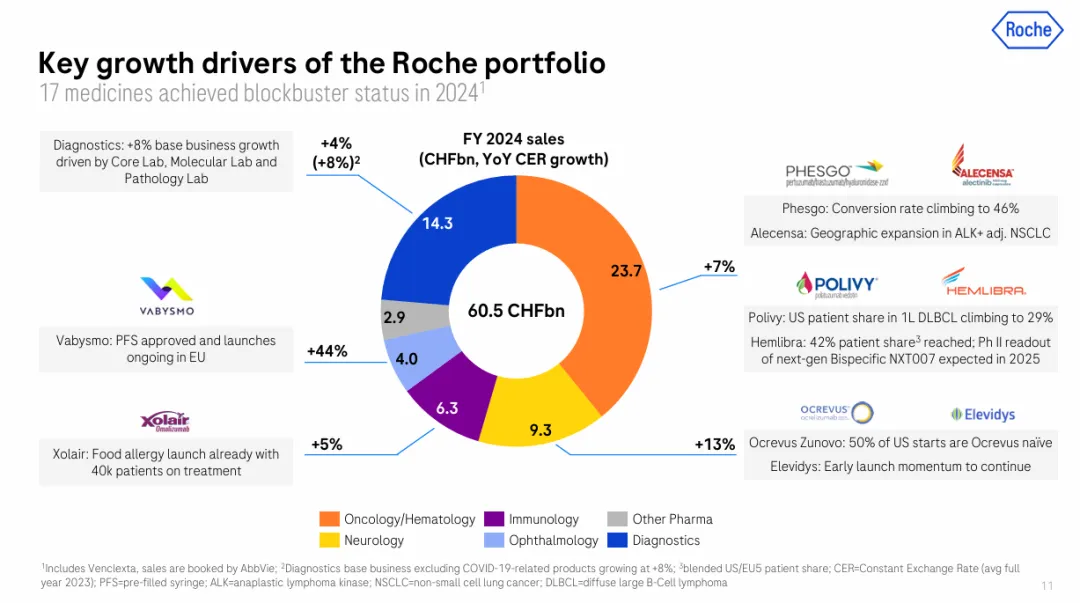
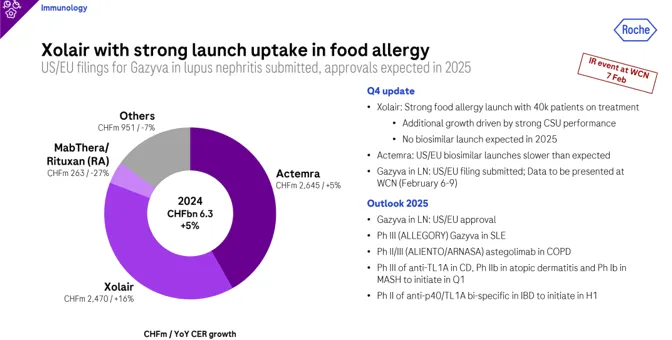
(Cosentyx/IL-17靶点销售额61.41亿美元,同比增长25%;下图诺华2024业绩)
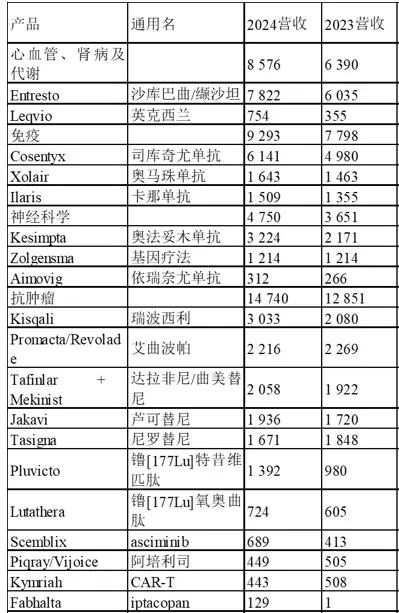
原研药在中国获批的适应症有:
1.过敏性哮喘
注射用奥马珠单抗仅适用于治疗确诊为IgE(免疫球蛋白E)介导的哮喘患者。
本品适用于成人和青少年(12岁及以上)患者,用于经吸入型糖皮质激素和长效吸入型β2-肾上腺素受体激动剂治疗后,仍不能有效控制症状的中至重度持续性过敏性哮喘。本品能降低这些患者的哮喘加重率。
2.慢性自发性荨麻疹(CSU)
本品适用于采用H1抗组胺药治疗后仍有症状的成人和青少年(12岁及以上)慢性自发性荨麻疹患者。
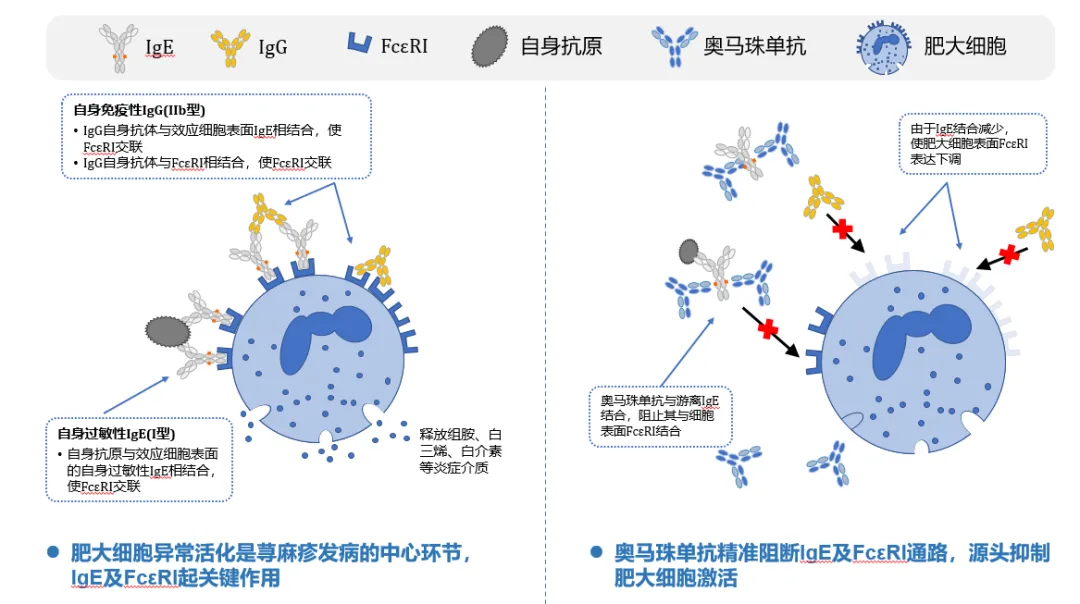
2025年2月10日,石药创新制药股份有限公司控股子公司石药集团巨石生物制药有限公司于近日收到国家药品监督管理局通知,注射用奥马珠单抗(商品名:恩益坦®)(3.3类注册分类的生物类似药/biosimilar)用于治疗中至重度持续性过敏性哮喘的适应症获得批准。这是恩益坦®在中国获批的第二个适应症。据悉,该产品遵循生物类似药相关的研究指南,通过药学、非临床、并且采用“头对头”的药代动力学比对和慢性自发性荨麻疹患者人群的临床等效性试验等一系列逐步递进的研究。本品最早由兴盟生物开发,代号为SYN008。2019年8月,石药license
in获得奥马珠单抗生物类似药SYN008的独家权利,以于中国大陆进行该产品有关的所有适应症开发与商业化。BD条款为向兴盟生物支付人民币1000万元的首付款,最多5000万元的开发里程碑付款,以及一定销售提成。
2023年5月23日,上海和泰州的迈博药业注射用奥马珠单抗的上市注册申请获得国家药监局批准,为中国首个递交新药申请的国产过敏性哮喘治疗性抗体新药,商品名“奥迈舒”。本品后由济民可信进行商业化等等。此前研发代号为CMAB007。
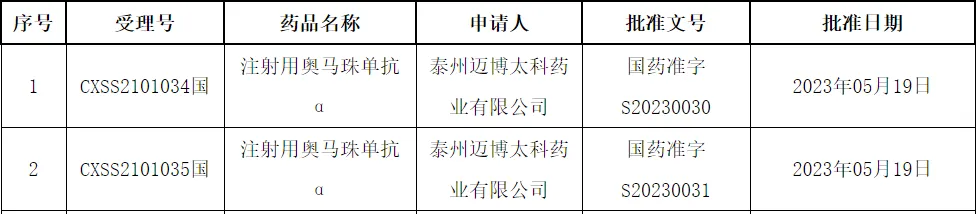
其他的国内生物类似药布局还有 远大医药/蜀阳 的产品在后期阶段。
值得注意的是,2025年3月,首款奥马珠单抗生物类似药在美国获批,且可互换。来自韩国巨头生物制药公司 Celltrion 的 Omlyclo(omalizumab-igec)。(参考:巨头Celltrion:韩国制药行业主导力量,向全球进发)

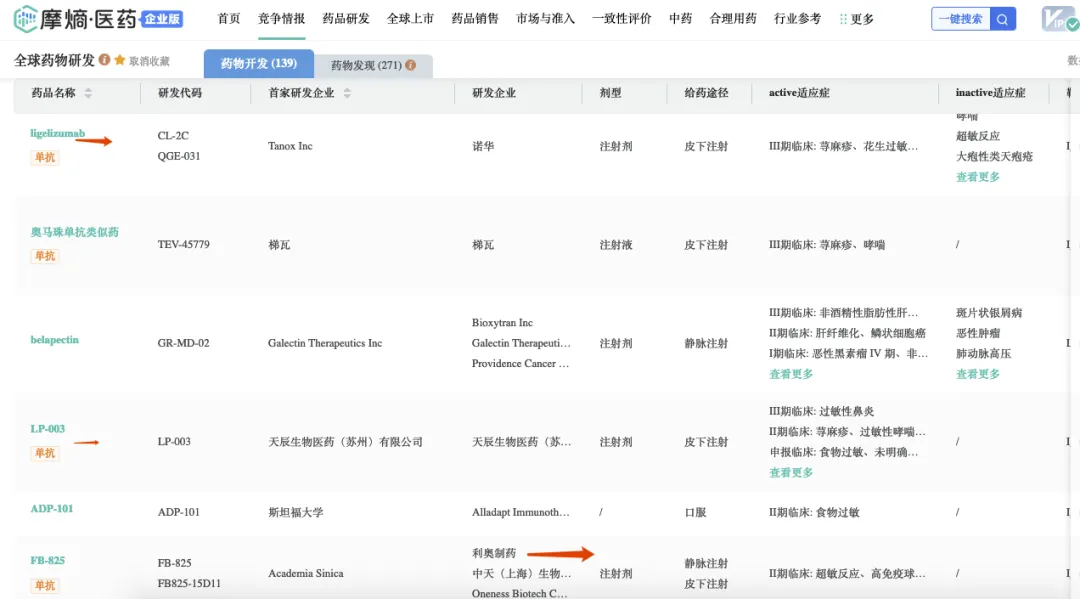
部分IgE新药开发
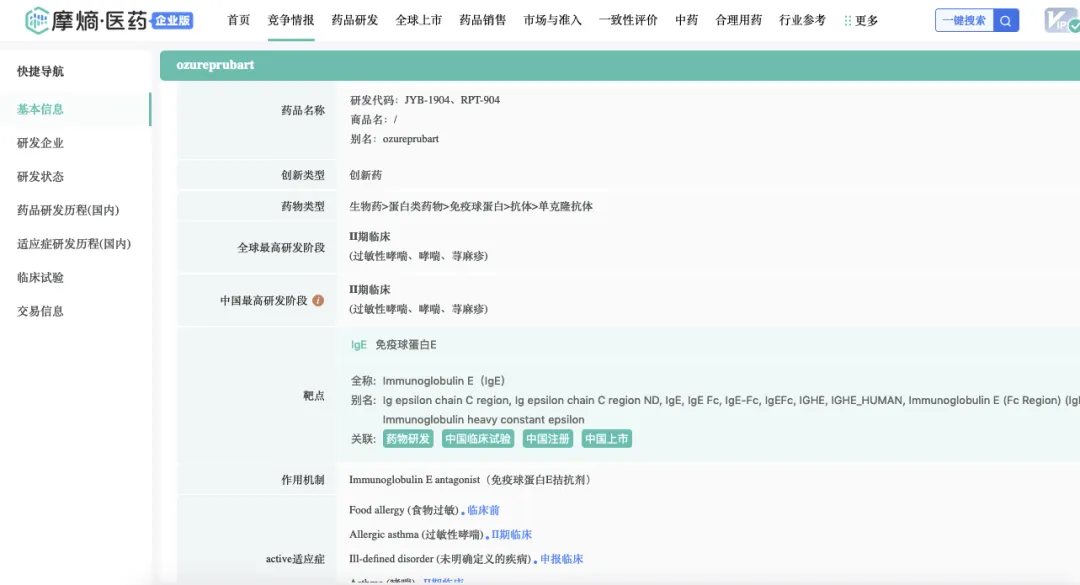
药融云数据,www.pharnexcloud.com;改名后为摩熵医药数据
2024年12月23日,济民可信旗下新药公司济煜医药与RAPT宣布双方已签订JYB1904独家许可协议(RAPT产品代号RPT904)。JYB904是济煜医药开发的一款具有更高亲和力及更长半衰期的抗IgE单克隆抗体。根据许可协议的条款,RAPT被授予除大中华区以外的全球开发和商业化JYB1904的权利。作为回报,济煜医药将获得3500万美元首付款,最高达6.725亿美元的里程碑付款,以及未来的梯度销售提成。
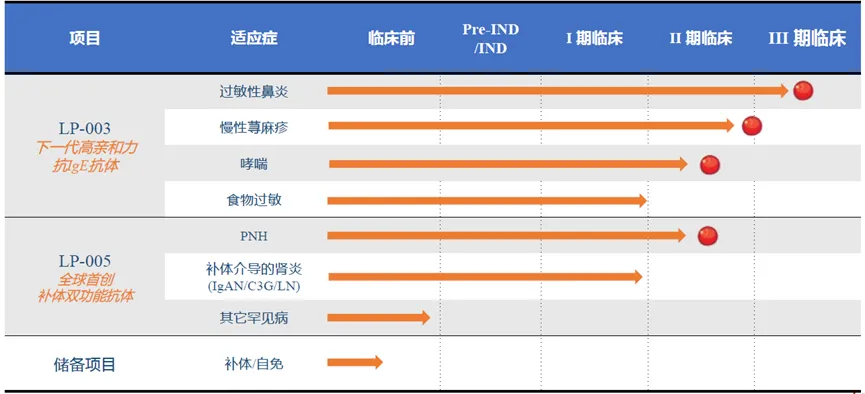
天辰生物,开发的下一代抗IgE抗体LP-003在治疗过敏性鼻炎的II期临床试验中,LP-003展现出良好的疗效和安全性。LP-003的III期临床正在积极推进,预计将于2025年下半年启动BLA,迈向上市。此外,LP-003在慢性荨麻疹、哮喘等适应症的II期临床试验正在开展中。
附:诺华最新1.2.3期临床在研产品线

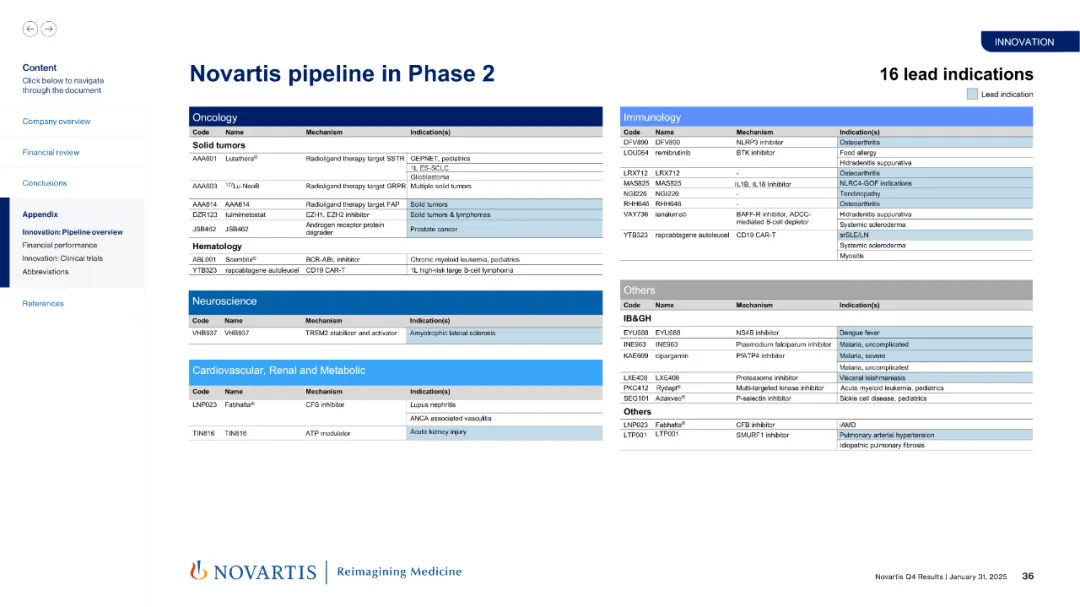
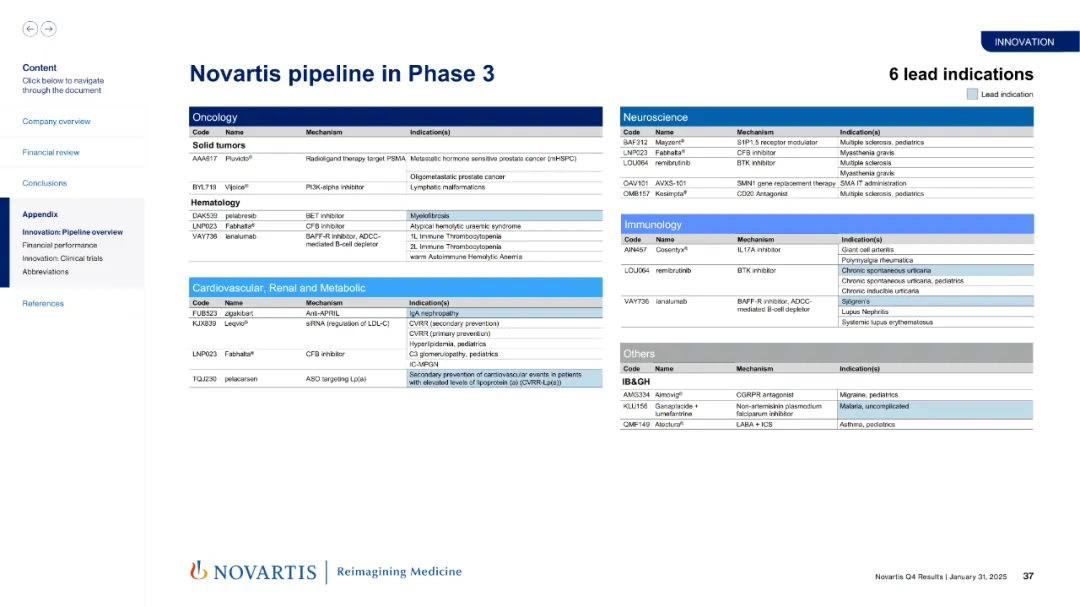

 产业资讯
产业资讯
 Innodrugs
Innodrugs  2026-03-23
2026-03-23
 164
164

 产业资讯
产业资讯
 药渡
药渡  2026-03-23
2026-03-23
 155
155

 产业资讯
产业资讯
 药融圈
药融圈  2026-03-23
2026-03-23
 147
147